พลูโทเนียม
หน้านี้มีเนื้อหาเป็นภาษาต่างประเทศ คุณสามารถช่วยพัฒนาหน้านี้ได้ด้วยการแปล ยกเว้นหากเนื้อหาเกือบทั้งหมดไม่ใช่ภาษาไทย ให้แจ้งลบแทน |
พลูโทเนียม (อังกฤษ: Plutonium) เป็นธาตุที่มีเลขอะตอม 94 และสัญลักษณ์ คือ Pu เป็นธาตุโลหะกัมมันตรังสี เป็นโลหะแอกทิไนด์สีขาวเงิน และจะมัวลงเมื่อสัมผัสอากาศซึ่งเกิดจากการรวมตัวกับออกซิเจน โดยปกติ พลูโทเนียมมี 6 ไอโซโทป และ 4 สถานะออกซิเดชัน สามารถเกิดปฏิกิริยาทางเคมีกับคาร์บอน ฮาโลเจน ไนโตรเจน และซิลิกอน เมื่อสัมผัสอากาศชื้นจะสร้างสารประกอบออกไซด์และไฮไดรด์มากกว่า 70 % ของปริมาตรซึ่งจะแตกออกเป็นผงแป้งที่สามารถติดไฟได้เอง พลูโทเนียมมีพิษที่เกิดจากการแผ่รังสีที่จะสะสมที่ไขกระดูก นอกจากนี้ยังมีคุณสมบัติอื่น ๆ ที่ทำให้การจัดการพลูโทเนียมเป็นเรื่องที่อันตรายมาก
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Plutonium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pronunciation | /pluːˈtoʊniəm/ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Allotropes | see Allotropes of plutonium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Appearance | โลหะสีขาวเงิน จะเปลี่ยนสีเป็นเทาเข้มเมื่ออยู่ในอากาศ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mass number | [244] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Plutonium in the periodic table | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic number (Z) | 94 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Group | f-block groups (no number) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Period | period 7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Block | f-block | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electron configuration | [Rn] 5f6 7s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrons per shell | 2, 8, 18, 32, 24, 8, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase at STP | solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point | 912.5 K (639.4 °C, 1182.9 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Boiling point | 3505 K (3228 °C, 5842 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Density (near r.t.) | 19.85 g/cm3 (239Pu)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| when liquid (at m.p.) | 16.63 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Heat of fusion | 2.82 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Heat of vaporization | 333.5 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar heat capacity | 35.5 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
Vapor pressure
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidation states | +2, +3, +4, +5, +6, +7, +8 (an amphoteric oxide) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativity | Pauling scale: 1.28 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionization energies |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic radius | empirical: 159 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Covalent radius | 187±1 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Other properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Natural occurrence | from decay | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Crystal structure | monoclinic | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Speed of sound | 2260 m/s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal expansion | 46.7 µm/(m⋅K) (at 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal conductivity | 6.74 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrical resistivity | 1.460 µΩ⋅m (at 0 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetic ordering | paramagnetic | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young's modulus | 96 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Shear modulus | 43 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson ratio | 0.21 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Number | 7440-07-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| History | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Naming | after dwarf planet Pluto, itself named after classical god of the underworld Pluto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Discovery | Glenn T. Seaborg, Arthur Wahl, Joseph W. Kennedy, Edwin McMillan (1940–1941) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes of plutonium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
ไอโซโทปที่สำคัญของพลูโทเนียม คือ พลูโทเนียม-239 ซึ่งมีครึ่งชีวิต 24,100 ปี พลูโทเนียม-239 และ 241 เป็นวัสดุฟิสไซล์ ซึ่งหมายความว่านิวเคลียสของอะตอมสามารถแตกตัว โดยการชนของนิวตรอนความร้อนเคลื่อนที่ช้า ซึ่งจะปลดปล่อยพลังงาน รังสีแกมมา และนิวตรอนจำนวนมาก ด้วยเหตุนี้ จึงสามารถเกิดปฏิกิริยาลูกโซ่นิวเคลียร์ได้ นำไปสู่การประยุกต์สร้างอาวุธนิวเคลียร์และเครื่องปฏิกรณ์นิวเคลียร์ ไอโซโทปที่เสถียรที่สุด คือ พลูโทเนียม-244 ซึ่งมีครึ่งชีวิตประมาณ 80 ล้านปี นานพอที่จะสามารถพบได้ในธรรมชาติ พลูโทเนียม-238 มีครึ่งชีวิต 88 ปี และปลดปล่อยอนุภาคแอลฟาออกมา มันเป็นแหล่งความร้อนของเครื่องผลิตไฟฟ้าด้วยความร้อนจากไอโซโทปรังสี ซึ่งใช้ในการให้พลังงานในยานอวกาศ พลูโทเนียม-240 มีอัตราของการแตกตัวของนิวเคลียสของอะตอมด้วยตัวเองสูง เป็นการเพิ่มอัตรานิวตรอนพื้นฐานของตัวอย่างที่มีไอโซโทปนี้ประกอบอยู่ด้วย การมีอยู่ของ Pu-240 เป็นข้อจำกัดสมรรถภาพของพลูโทเนียมที่ใช้ในอาวุธหรือแหล่งพลังงานและเป็นตัวกำหนดเกรดของพลูโทเนียม: อาวุธ (< 7%), เชื้อเพลิง (7–19%) และเกรดเครื่องปฏิกรณ์ (> 19%)
ธาตุลำดับที่ 94 สังเคราะห์ได้เป็นครั้งแรกในปี ค.ศ. 1940 โดยทีมของ เกลนน์ ที. ซีบอร์ก และ เอดวิน แมกมิลแลน ที่ห้องวิจัยในมหาวิทยาลัยแคลิฟอร์เนีย เบิร์กลีย์โดยการระดมยิงยูเรเนียม-238 ด้วยดิวเทอรอน แมกมิลแลนตั้งชื่อธาตุนี้ตามดาวพลูโต และซีบอร์กเสนอสัญลักษณ์เป็น Pu ซึ่งเป็นเรื่องตลกเล็ก ๆ ต่อมามีการพบพลูโทเนียมในธรรมชาติ การค้นพบพลูโทเนียมถูกรักษาไว้เป็นความลับซึ่งเป็นส่วนหนึ่งของโครงการแมนฮัตตันเพื่อพัฒนาระเบิดปรมาณูในระหว่างสงครามโลกครั้งที่สอง การทดลองอาวุธนิวเคลียร์ครั้งแรกคือ "ทรินนิที" (กรกฎาคม ค.ศ. 1945) และระเบิดปรมาณูที่นำไปใช้ทำลายเมืองในครั้งที่สอง (นะงะซะกิ ญี่ปุ่น สิงหาคม ค.ศ. 1945) คือ "แฟตแมน" ระเบิดทั้งสองใช้แกนเป็น Pu-239 นอกจากนี้ยังมีการทดลองผลของพลูโทเนียมต่อมนุษย์โดยไม่มีการแจ้งยินยอม และอุบัติเหตุมวลถึงระดับวิกฤต จนเป็นเหตุให้มีผู้เสียชีวิตนั้น เกิดขึ้นในระหว่างและหลังสงคราม การจัดการกับกากพลูโทเนียมจากโรงงานพลังงานนิวเคลียร์และอาวุธนิวเคลียร์ที่ถูกแยกส่วนทำลายซึ่งสร้างในระหว่างสงครามเย็นเป็นความกังวลหลักในเรื่องการเพิ่มขึ้นของนิวเคลียร์ สุขภาพ และสิ่งแวดล้อม แหล่งที่มาอื่น ๆ ของพลูโทเนียมในธรรมชาติคือฝุ่นรังสีนิวเคลียร์จากการทดลองนิวเคลียร์ทั้งบนดินและใต้ดินและอุบัติเหตุทางนิวเคลียร์
ลักษณะ
แก้ทางกายภาพ
แก้พลูโทเนียมมีลักษณะเป็นโลหะสีขาวเงินคล้ายนิกเกิล แต่เมื่อรวมตัวกับออกซิเจนจะเปลี่ยนเป็นสีเทามอ ๆ หรือเป็นสีเขียวเข้มปนเหลืองตามที่มีการรายงาน[4]>[5] ที่อุณหภูมิห้อง พลูโทเนียมมีกัมมันตภาพรังสีเป็นรังสีแอลฟา รูปแบบโครงสร้างที่พบได้มากที่สุดของพลูโทเนียม มีลักษณะแข็งและเปราะ แตกหักง่ายคล้ายเหล็กที่มีคาร์บอนสูง ยกเว้นเมื่อเจือกับโลหะอื่น จึงจะมีลักษณะนิ่มและดัดได้[4] แตกต่างจากโลหะส่วนใหญ่ พลูโทเนียมนำความร้อนและกระแสไฟฟ้าไม่ดี[4], มีจุดหลอมเหลวต่ำ (640 °C) และมีจุดเดือดสูง (3,327 °C) [4]
การสลายให้อนุภาคแอลฟาได้ปลดปล่อยนิวเคลียสฮีเลียมที่มีพลังงานสูงออกมา ซึ่งเป็นการแผ่รังสีชนิดก่อไอออนโดยส่วนมากของพลูโทเนียม[6] เพราะความร้อนจากการปลดปล่อยอนุภาคแอลฟานี้ ดังนั้นเมื่อสัมผัสก้อนพลูโทเนียมขนาดเท่าลูกเบสบอลจึงรู้สึกอุ่น ถ้าเป็นก้อนขนาดใหญ่สามารถต้มน้ำ 1 ลิตรให้เดือดได้ใน 2-3 นาที[7][8]
ความต้านทานไฟฟ้าของพลูโทเนียมที่อุณหภูมิห้องมีค่าสูงและสูงมากขึ้นเมื่ออุณหภูมิลดลงซึ่งตรงข้ามกับโลหะทั่วไป[9] เมื่ออุณหภูมิลดลงถึง 100 K หรือต่ำกว่าความต้านทานจะลดลงอย่างรวดเร็ว[9] และความต้านทานจะเริ่มสูงขึ้นที่อุณหภูมิ 20 K เพราะผลจากการแผ่รังสี โดยอัตราขึ้นอยู่กับส่วนประกอบไอโซโทปของตัวอย่าง[9]
พลูโทเนียมสามารถเรืองแสงได้ด้วยตัวเองจึงเกิดความล้าตลอดโครงสร้างผลึกซึ่งหมายถึงระเบียบลำดับของอะตอมมีความยุ่งเหยิงเนื่องจากการแผ่รังสี[10] อย่างไรก็ตามการเรืองแสงด้วยตัวเองสามารถนำไปสู่การอ่อนตัวที่ลดผลกระทบของความล้าตามอุณหภูมิที่เพิ่มขึ้นสูงกว่า 100 K[11]
พลูโทเนียมไม่เหมือนกับวัสดุส่วนมาก ความหนาแน่นของพลูโทเนียมจะเพิ่มขึ้นประมาณ 2.5% เมื่อละลาย แต่โลหะเหลวแสดงการลดลงเป็นเชิงเส้นตามอุณหภูมิ[9] เมื่อใกล้จุดหลอมเหลว พลูโทเนียมเหลวมีความหนืดและแรงตึงผิวสูงมากเมื่อเทียบกับโลหะอื่น[10]
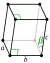
อัญรูป
แก้พลูโทเนียมมีอัญรูปที่ต่างกันโดยปกติ 6 ชนิดและชนิดที่ 7 (zeta, ζ) ภายใต้อุณหภูมิสูงและระยะความดันจำกัด[12] ทุกอัญรูปมีโครงสร้างหรือรูปแบบของธาตุที่ต่างกัน มีความหนาแน่นและโครงสร้างผลึกต่างกันแต่มีพลังงานภายในใกล้เคียงกันมาก ทำให้พลูโทเนียมไวต่อการเปลี่ยนแปลงของอุณหภูมิ, ความดัน หรือสภาวะทางเคมี และปริมาตรมีการเปลี่ยนแปลงสูงตามการเปลี่ยนสถานะจากอัญรูปหนึ่งไปสู่อัญรูปหนึ่ง[10] พลูโทเนียมจะมีความหนาแน่นเพิ่มขึ้นเมื่อหลอมละลาย ประมาณ 2.5% แต่เมื่อเป็นของเหลวความหนาแน่นจะลดลงเป็นเชิงเส้นโดยเทียบกับอุณหภูมิ[9] ความหนาแน่นในรูปแบบต่างๆจะอยู่ที่ 16.00 g/cm3 ถึง 19.86 g/cm3[13]
การมีหลายอัญรูปของพลูโทเนียมทำให้การตัดแบ่งพลูโทเนียมได้ยากเพราะมันเปลี่ยนสภาวะได้อย่างรวดเร็ว เช่นปล่อยรังสี α ที่อุณหภูมิห้องในพลูโทเนียมบริสุทธิ์ มันมีลักษณะการตัดแบ่งคล้ายเหล็กหล่อแต่จะเปลี่ยนเป็นพลาสติกและปล่อยรังสี β อ่อนๆเมื่ออุณหภูมิสูงขึ้นเล็กน้อย[14] การปล่อยรังสี α มีโครงสร้างผลึกแบบโมโนคลีนิคความสมมาตรต่ำ นอกจากนั้น มันเปราะบาง, แข็ง, อัดได้ และนำไฟฟ้าได้ไม่ดี[12]
พลูโทเนียมจะปล่อยรังสี δ นั้น ปกติจะพบที่อุณหภูมิ 310 °C ถึง 452 °C แต่จะเสถียรที่อุณหภูมิห้องเมื่อผสมแกลเลียม, อะลูมิเนียม, หรือซีเรียมเล็กน้อย, เพื่อปรับปรุงให้สามารถเชื่อมต่อกันได้[14] รูปแบบเดลตามีลักษณะคล้ายโลหะหลายอย่าง และโดยทั่วไปจะแข็งและดัดได้เหมือนอะลูมิเนียม[12]
ปฏิกิริยานิวเคลียร์แบบแตกตัว
แก้พลูโทเนียมเป็นโลหะแอกทิไนด์กัมมันตภาพรังสีซึ่งไอโซโทปพลูโทเนียม-239 (Pu-239) เป็นหนึ่งในสามไอโซโทปแรกของวัสดุฟิสไซล์[15] (อีก 2 ชนิดคือยูเรเนียม-233 และ ยูเรเนียม-235)[16] นิวเคลียสอะตอมของไอโซโทปสามารถแตกตัวหรือแบ่งแยกนิวเคลียสเมื่อถูกชนด้วยนิวตรอนที่เคลื่อนที่ช้าและปลดปล่อยนิวตรอนมาเพียงพอที่จะทำให้เกิดปฏิกิริยาลูกโซ่ทางนิวเคลียร์โดยแบ่งแยกนิวเคลียสเพิ่มมากขึ้น
Pu-239 มีค่าองค์ประกอบทวีคูณ (k) มากกว่าหนึ่งซึ่งหมายถึง ถ้าพลูโทเนียมมีมวลพอเพียงและรูปทรงที่เหมาะสม (เช่น ถูกอัดเป็นทรงกลม) มันจะมีมวลวิกฤต[17] ระหว่างการแบ่งแยกนิวเคลียส ส่วนของพลังงานยึดเหนี่ยวซึ่งยึดนิวเคลียสไว้ด้วยกันจะปลดปล่อยความร้อน, คลื่นแม่เหล็กไฟฟ้า และพลังงานจลน์ออกมาจำนวนมาก พลูโทเนียมหนึ่งกิโลกรัมสามารถสร้างแรงระเบิดเท่ากับระเบิดทีเอ็นที 20,000 ตัน[7] มันมีพลังงานมากพอที่ทำให้ Pu-239 สามารถนำไปใช้สร้างอาวุธนิวเคลียร์และใช้ในเครื่องปฏิกรณ์นิวเคลียร์
การมีอยู่ของไอโซโทปพลูโทเนียม-240 (Pu-240) นั้นเป็นสิ่งจำกัดสมรรถภาพของระเบิดนิวเคลียร์ เพราะ Pu-240 มีอัตราการแบ่งแยกนิวเคลียส (ฟิชชัน) ด้วยตนเองสูง (~440 นิวตรอนต่อวินาทีต่อกรัม—มากกว่า 1,000 นิวตรอนต่อวินาทีต่อกรัม[18]) ยิ่งมีระดับนิวตรอนสูงยิ่งเป็นเหตุให้ระเบิดเสี่ยงต่อการทำงานล้มเหลว[19] พลูโทเนียมแบ่งเป็นเกรดสำหรับทำอาวุธ,เกรดสำหรับเป็นเชื้อเพลิง และเกรดสำหรับใช้ในเครื่องปฏิกรณ์นิวเคลียร์ ซึ่งแบ่งตามอัตราร้อยละของ Pu-240 ในส่วนประกอบ เกรดสำหรับทำอาวุธจะมี Pu-240 น้อยกว่า 7% Pu-240 เกรดสำหรับเป็นเชื้อเพลิงจะมี Pu-240 7% ถึง 19% และเกรดสำหรับใช้ในเครื่องปฏิกรณ์นิวเคลียร์จะมี Pu-240 19% หรือมากกว่า[20] ไอโซโทปพลูโทเนียม-238 (Pu-238) นั้นไม่สามารถเกิดปฏิกิริยานิวเคลียร์แบบแตกตัวได้ถึงแม้มันจะมีการสลายปลดปล่อยรังสีแอลฟาก็ตาม[7]
ไอโซโทปและการสังเคราะห์
แก้พลูโทเนียมมี 12 ไอโซโทป[6] Pu-244 มีอายุมากที่สุด มีครึ่งชีวิต 80.8 ล้านปี, Pu-242 มีครึ่งชีวิต 373,300 ปี, และ Pu-239 มีครึ่งชีวิต 24,110 ปี[6] ไอโซโทปที่เหลือมีครึ่งชีวิตต่ำกว่า 7,000 ปี[6] มีสภาวะไม่เสถียร 8 สภาวะที่มีครึ่งชีวิตน้อยกว่า 1 วินาที[6]
ไอโซโทปของพลูโทเนียมมีเลขมวลระหว่าง 228 ถึง 247[6] ไอโซโทปที่เสถียรและมีเลขมวลต่ำที่สุดคือ Pu-244 มีการสลายตัวโดยเกิดฟิชชันขึ้นเองและปล่อยรังสีแอลฟาออกมา และส่วนมากกลายเป็นไอโซโทป ยูเรเนียม (92 โปรตอน) และ เนปทูเนียม (93 โปรตอน) [6] ส่วนขั้นแรกของการสลายไอโซโทปที่เลขมวลมากกว่า Pu-244 คือการปลดปล่อยรังสีเบต้าและส่วนมากจะกลายเป็นไอโซโทปอะเมริเซียม (95 โปรตอน) [6]
อนุกรมการสลายเนปทูเนียม (neptunium decay series) มี Pu-241 เป็นไอโซโทปตั้งต้นของอนุกรม สลายกลายเป็นอะเมริเซียม-241 ร่วมกับการปลดปล่อยอิเล็กตรอนหรือรังสี β[7]
Pu-238 และ Pu-239 เป็นการสังเคราะห์ไอโซโทปที่แพร่หลายมาก[7] Pu-239 ถูกสังเคราะห์โดยใช้ยูเรเนียม (U) และนิวตรอน (n) ร่วมกับการสลายปลดปล่อยรังสีบีตา (β−) เป็นเนปทูเนียม (Np) ซึ่งเป็นตัวกลาง:[21]
นั่นก็คือนิวตรอนจากการฟิชชันของ U-235 จะถูกจับโดยนิวเคลียสของ U-238 กลายเป็น U-239 จากนั้นการสลายปลดปล่อยรังสีบีตา จะเพิ่มโปรตอนกลายเป็น Np-239 (ครึ่งชีวิต 2.36 วัน) และสลายปลดปล่อยรังสีบีตาอีกครั้งกลายเป็น Pu-239[22] ผู้ที่ทำงานในโครงการทูบ อัลลอยส์ (Tube Alloys) ทำนายปฏิกิริยานี้ตามหลักทฤษฎีได้ในปี ค.ศ. 1940
Pu-238 ถูกสังเคราะห์ด้วยการยิง U-238 ด้วยดิวเทอรอน (D, ไฮโดรเจนหนัก) ตามปฏิกิริยานี้:[23]
ในสมการ ดิวเทอเรียมที่ยิงใส่ U-238 ทำให้เกิด 2 อนุภาคนิวตรอนและ Np-238 และจะแผ่กัมมันตภาพรังสีโดยปล่อยรังสีเบต้าลบออกมาแล้วกลายไปเป็น Pu-238
ความร้อนจากการสลายและคุณสมบัติการแตกตัวของนิวเคลียส
แก้ไอโซโทปของพลูโทเนียมภายใต้การสลายตัวของสารกัมมันตรังสีจะสร้างความร้อนจากการสลาย (decay heat) ขึ้น ไอโซโทปที่ต่างกันจะให้ผลรวมความร้อนต่อมวลที่ต่างกัน ความร้อนจากการสลายจะมีหน่วยเป็นวัตต์/กิโลกรัม หรือ มิลลิวัตต์/กรัม ในกรณีพลูโทเนียมที่มีขนาดใหญ่ (เช่น เบ้าอาวุธ) การระบายความร้อนที่เกิดจากตัวมันเองนั้นอาจจะเป็นเรื่องสำคัญมาก ทุกไอโซโทปจะสร้างรังสีแกมมาอ่อนๆจากการสลาย
| ไอโซโทป | รูปแบบการสลายตัวของสารกัมมันตรังสี | ครึ่งชีวิต (ปี) | ความร้อนจากการสลาย (W/kg) | นิวตรอนฟิชชันเกิดเอง (1/(g·s)) |
|---|---|---|---|---|
| Pu-238 | แอลฟา ไปเป็น U-234 | 87.7 | 560 | 2600 |
| Pu-239 | แอลฟา ไปเป็น U-235 | 24100 | 1.9 | 0.022 |
| Pu-240 | แอลฟา ไปเป็น U-236, ฟิชชันเกิดเอง | 6560 | 6.8 | 910 |
| Pu-241 | บีตา ไปเป็น Am-241 | 14.4 | 4.2 | 0.049 |
| Pu-242 | แอลฟา ไปเป็น U-238 | 376000 | 0.1 | 1700 |
สารประกอบและคุณสมบัติทางเคมี
แก้ที่อุณหภูมิห้อง พลูโทเนียมบริสุทธิ์จะมีสีเงินและจะคล้ำขึ้นเรื่อยๆเมื่อรวมตัวกับออกซิเจน[7] ไอออนของสารละลายพลูโทเนียมมี 5 สถานะออกซิเดชันในสารละลายในน้ำ:[13]
- Pu (III), Pu3+ (สีม่วงน้ำเงิน)
- Pu (IV), Pu4+ (สีน้ำตาลเหลือง)
- Pu (V), PuO2+ (ชมพู?) [note 1]
- Pu (VI), PuO22+ (สีชมพูส้ม)
- Pu (VII), PuO53− (เขียว) –ไอออนนี้พบได้น้อย
สีของสารละลายพลูโทเนียมขึ้นกับสภาวะออกซิเดชันและสภาพความเป็นกรดของไอออนที่มีประจุลบ[25] สภาพความเป็นกรดของไอออนที่มีประจุลบจะกำหนดความเข้มข้นของสารเชิงซ้อนของพลูโทเนียม
โลหะพลูโทเนียมสร้างโดยการเกิดปฏิกิริยาทางเคมีของฟลูออไรด์พลูโทเนียม (IV) กับแบเรียม, แคลเซียม, หรือลิเทียมที่อุณหภูมิ 1200 °C[26] มันทำปฏิกิริยากับกรด, ออกซิเจน, และไอน้ำแต่ไม่ทำปฏิกิริยากับอัลคาไลและละลายได้ง่ายในไฮโดรคลอริกเข้มข้น, ไฮโดรไอโอดิก และกรดเปอร์คลอริก[27] โลหะเหลวนี้ต้องถูกเก็บในสุญญากาศหรือในอากาศเฉื่อยเพื่อป้องกันการทำปฏิกิริยาทางเคมีกับอากาศ[14] ที่อุณหภูมิ 135 °C พลูโทเนียมจะติดไฟในอากาศและจะระเบิดเมื่อนำไปใส่ในคาร์บอนเตตระคลอไรด์[28]
พลูโทเนียมเป็นโลหะที่เกิดปฏิกิริยาในอากาศชื้นหรืออาร์กอนชื้น มันจะรวมตัวกับออกซิเจนอย่างรวดเร็วและสร้างส่วนผสมระหว่างออกไซด์และไฮไดรด์[4] ถ้าโลหะพลูโทเนียมถูกวางไว้ไอน้ำนานพอ จะเกิดผง PuO2 ที่ผิวหน้า[4] พลูโทเนียมไฮไดรด์ก็ถูกสร้างขึ้นมาเช่นกันแต่ไอน้ำส่วนเกินนั้นทำให้เกิดเพียง PuO2 เท่านั้น[27]
ด้วยสิ่งปกคลุมนี้ ทำให้โลหะผสมพลูโทเนียมเป็นไพโรโฟริก (pyrophoric) หมายความว่ามันสามารถติดไฟได้โดยธรรมชาติ ปกติการจัดการกับพลูโทเนียมจึงทำในก๊าซเฉื่อยและอากาศแห้งอย่างไนโตรเจนหรืออาร์กอน[4] ออกซิเจนจะหน่วงผลของความชื้นและกระทำตัวเป็นตัวกระทำแบบไม่มีปฏิกิริยา[4]
พลูโทเนียมเกิดปฏิกิริยาทางเคมีกับออกซิเจนอย่างรวดเร็ว ทำให้เกิด PuO และ PuO2 พร้อมกับออกไซด์ตัวกลาง[13] คือพลูโทเนียมออกไซด์มากกว่า 40% โดยปริมาตรโลหะพลูโทเนียม[28] มันจะทำปฏิกิริยาทางเคมีกับกับแฮโลเจนทำให้เกิดสารประกอบ อย่าง PuX3 โดยที่ X สามารถเป็น F, Cl, Br หรือ I และแม้แต่ทำให้เกิด PuF4 ด้วยเช่นกัน[13] สิ่งที่เกิดตามมาจากการสังเกตออกซิแฮไลด์: PuOCl, PuOBr และ PuOI[13] เมื่อมันทำปฏิกิริยาทางเคมีกับคาร์บอนจะสร้าง PuC, ทำปฏิกิริยาทางเคมีกับไนโตรเจนจะสร้าง PuN และทำปฏิกิริยาทางเคมีกับซิลิคอนจะสร้าง PuSi2[13]
เบ้าที่ใช้ในการบรรจุพลูโทเนียมต้องสามารถต่อต้านคุณสมบัติรีดักชั่น ที่รุนแรงได้[14] วัสดุทนไฟอย่างแทนทาลัมและทังสเตนพร้อมด้วยออกไซด์, โบไรด์, คาร์ไบด์, ไนไทรด์ และ ซิลิไซด์ที่เสถียรมากสามารถทนพลูโทเนียมได้[14] การหลอมละลายในเตาไฟฟ้าสามารถให้สร้างแท่งโลหะเล็กๆได้โดยไม่ต้องใช้เบ้าหลอม[14]
พลูโทเนียมสามารถสร้างโลหะผสมและสารประกอบตัวกลางกับโลหะอื่นมากมาย แต่ยกเว้นลิเทียม, โพแทสเซียม และ โซเดียมของโลหะแอลคาไล; แบเรียม, แคลเซียม และ สตรอนเชียม ของโลหะแอลคาไลน์เอิร์ท; และ ยูโรเพียม และ อิตเทอร์เบียมของแรร์เอิร์ท[27] รวมถึงโลหะทนไฟอย่าง โครเมียม, โมลิบดีนัม, ไนโอเบียม, แทนทาลัม และ ทังสเตนซึ่งสามารถละลายได้ในพลูโทเนียมเหลว แต่ไม่ละลายหรือละลายเพียงเล็กน้อยในพลูโทเนียมแข็ง[27]
พลูโทเนียมในธรรมชาติ
แก้พลูโทเนียมมีเพียงสองไอโซโทป (Pu-239 และ Pu-244) ที่สามารถพบได้ในธรรมชาติ พบ Pu-244 เพียงเล็กน้อย เกิดจากการสลายอนุภาคในแร่ยูเรเนียมและมีครึ่งชีวิตประมาณ 80 ล้านปี[29] และมีโอกาสเกิด Pu-239 ได้น้อยกว่า (ประมาณ 2-3 ในล้านล้าน) ซึ่งผลิตภัณฑ์จากการสลายอนุภาคของมันนั้นพบตามธรรมชาติในแร่ยูเรเนียมเข้มข้นบางก้อน[30] เช่น เครื่องปฏิกรณ์นิวเคลียร์หรือเตานิวเคลียร์ที่เกิดขึ้นเองตามธรรมชาติในโอโกล ประเทศกาบอง[31] อัตราส่วนของ Pu-239 ต่อ U ที่เหมืองทะเลสาบไซการ์ แหล่งแร่ยูเรเนียม อยู่ในช่วง 2.4×10−12 ถึง 44×10−12[32]
พบ Pu-239 ในร่างกายมนุษย์เล็กน้อย สาเหตุมาจากการทดลองอาวุธนิวเคลียร์บนพื้นดิน 550 ครั้งเท่าที่มีการรายงาน และส่วนใหญ่ หลายครั้งมาจากอุบัติเหตุทางนิวเคลียร์[28] การทดลองอาวุธนิวเคลียร์ในบรรยากาศส่วนใหญ่ยุติลงในปี ค.ศ. 1963 โดยการลงนามในสนธิสัญญาว่าด้วยการห้ามทดลองนิวเคลียร์แต่เพียงบางส่วน แต่ประเทศฝรั่งเศสนั้นยังคงทดลองต่อเนื่องไปจนถึงช่วงปี ค.ศ. 1980 และบางประเทศก็ยังมีการทดลองหลังปี ค.ศ. 1963 เพราะ Pu-239 เป็นการสร้างขึ้นโดยจำเพาะและเป็นผลของการสลายกัมมันตรังสีของแร่ยูเรเนียม Pu-239 จึงเป็นไอโซโทปที่มีมากที่สุดของพลูโทเนียม[28]
ประวัติ
แก้การค้นพบ
แก้เอนรีโก แฟร์มีและทีมนักวิทยาศาสตร์ของมหาวิทยาลัยแห่งโรมรายงานว่าพวกเขาค้นพบธาตุที่ 94 ในปี ค.ศ. 1934[33] แฟร์มีเรียกธาตุนี้ว่า เฮสพีเรียม (hesperium) และนั่นทำให้เขาได้รับรางวัลโนเบลสาขาฟิสิกส์ประจำปี ค.ศ. 1938[34] อย่างไรก็ตาม ธาตุที่เขารายงานนั้นผิดพลาด ตัวอย่างที่แตกตัวนั้นแท้จริงแล้วคือส่วนผสมของแบเรียม (รายงานเป็นธาตุที่ 93), คริปทอน (รายงานเป็นธาตุที่ 94) และธาตุอื่นๆ ซึ่งข้อผิดพลาดนั้นเกิดจาก ณ.เวลานั้นปฏิกิริยานิวเคลียร์แบบแตกตัวยังไม่มีการค้นพบ[35]
พลูโทเนียม (โดยเฉพาะ Pu-238) ถูกสร้างและสกัดได้เป็นครั้งแรกในวันที่ 14 ธันวาคม ค.ศ. 1940 และระบุคุณสมบัติทางเคมีในวันที่ 23 กุมภาพันธ์ ค.ศ. 1941 โดย ดร. เกลนน์ ที. ซีบอร์ก (Glenn T. Seaborg), เอดวิน เอ็ม. แมกมิลแลน (Edwin M. McMillan), โจเซฟ ดับเบิลยู. เคนเนดี (Joseph W. Kennedy), แซกชาร์รี เอ็ม. เททอม (Zachary M. Tatom), และอาร์เทอร์ ซี. วอล์ (Arthur C. Wahl) โดยการยิงยูเรเนียมด้วยดิวเทอรอนในเครื่องเร่งอนุภาคไซโคลทรอน (cyclotron) ขนาด 60 นิ้วที่มหาวิทยาลัยแคลิฟอร์เนีย เบิร์กลีย์[36] การทดลองในปี ค.ศ. 1940 เนปทูเนียม-238 ถูกสร้างขึ้นได้โดยตรงโดยการระดมยิงอนุภาคแต่จะสลายโดยการแผ่รังสีเบต้าในสองวันหลังจากนั้นซึ่งแสดงถึงการก่อรูปของธาตุลำดับที่ 94[28]
เอกสารการค้นพบถูกตระเตรียมและส่งไปที่วารสาร Physical Review ในเดือนมีนาคม ค.ศ. 1941[28] แต่เอกสารถูกเก็บกลับคืนก่อนที่จะถูกตีพิมพ์หลังจากพบว่าไอโซโทปของธาตุใหม่นั้น (Pu-239) สามารถเกิดการแตกตัวทางนิวเคลียร์ได้ซึ่งเป็นหนทางที่อาจใช้ในระเบิดปรมาณู การตีพิมพ์ได้ล่าช้าออกไปจนกระทั่งหนึ่งปีหลังสงครามโลกครั้งที่สองสิ้นสุดลงเพราะความกังวลในเรื่องความปลอดภัย[15]
เอดวิน แมกมิลแลนตั้งชื่อธาตุแรกที่ค้นพบที่มีจำนวนอะตอมสูงกว่าธาตุยูเรเนียมตามดาวเนปจูนและเสนอว่าธาตุที่ 94 ซึ่งเป็นธาตุถัดมา ชื่อก็ควรจะพิจารณาเป็นดาวถัดไป คือดาวพลูโต[7][note 2] แรกสุดซีบอร์กใช้ชื่อ "พลูเทียม" (plutium) แต่หลังจากนั้นเขาคิดว่า"พลูโทเนียม"ฟังดูดีกว่า[37] เขาเลือกใช้อักษร "Pu" เป็นตัวย่อซึ่งเป็นเรื่องตลกโดยไม่สนใจหมายเหตุในตารางธาตุเลย[note 3] ชื่ออื่นๆ ที่ซีบอร์กและคนอื่นๆ นำมาพิจารณาก็มี "ยูล์ทีเมียม (ultimium)" หรือ "เอ็กทรีเมียม (extremium)" เนื่องจากความเชื่อในขณะนั้นว่าพวกเขาพบธาตุที่อาจเป็นตัวสุดท้ายบนตารางธาตุ[38]
การวิจัยในช่วงแรก
แก้หลังจากสองสามเดือนแรกของการศึกษาเบื้องต้นพบว่าคุณสมบัติพื้นฐานทางเคมีของพลูโทเนียมนั้นคล้ายกับยูเรเนียม[28] การวิจัยในช่วงแรกนั้นกระทำที่ห้องปฏิบัติการโลหะวิทยาลับของมหาวิทยาลัยชิคาโก ในวันที่ 18 สิงหาคม ค.ศ. 1942 พลูโทเนียมปริมาณเล็กน้อยถูกแยกสกัดออกมาและวัดได้เป็นครั้งแรก ประมาณ 50 ไมโครกรัมของพลูโทเนียม-239 รวมตัวกับยูเรเนียมจะให้ผลผลิตการแตกตัว (fission product) เมื่อสกัดออกมามีน้ำหนักประมาณ 1 ไมโครกรัม[30][39] กระบวนการนี้ช่วยให้นักเคมีสามารถระบุน้ำหนักอะตอมของธาตุชนิดใหม่ได้[40][note 4]
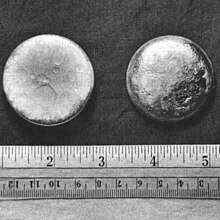
ในเดือน พฤศจิกายน ค.ศ. 1943 มีการสกัดพลูโทเนียมไตรฟลูออไรด์เพื่อสร้างตัวอย่างโลหะพลูโทเนียมเป็นครั้งแรก เป็นโลหะทรงกลมหนักเพียงสองสามกรัมเท่านั้น[30] ซึ่งพอเพียงที่จะทำให้มองเห็นด้วยตาเปล่าเป็นครั้งแรกในการสังเคราะห์[41]
มีการศึกษาคุณสมบัติทางนิวเคลียร์ของพลูโทเนียม-239 และพบว่าเมื่ออะตอมถูกกระแทกด้วยอนุภาค มันจะแตกตัวและปลดปล่อยอนุภาคและพลังงานจำนวนมาก อนุภาคเหล่านั้นสามารถไปชนอะตอมพลูโทเนียม-239 อื่นและกลายเป็นปฏิกิริยาลูกโซ่นิวเคลียร์อย่างรวดเร็ว ผลของการระเบิดนี้เพียงพอที่จะทำลายเมืองได้ถ้าไอโซโทปเข้มข้นเพียงพอที่จะทำให้เกิดมวลวิกฤต[28]
โครงการแมนฮัตตัน
แก้ระหว่างสงครามโลกครั้งที่สอง รัฐบาลสหรัฐอเมริกาได้จัดตั้งโครงการแมนฮัตตันขึ้น โดยมีจุดมุ่งหมายเพื่อพัฒนาระเบิดปรมาณู สถานที่วิจัยและผลิตสามแห่งแรกของโครงการคือ โรงงานผลิตพลูโทเนียมอยู่ที่แฮนฟอร์ด โรงงานเสริมสมรรถนะยูเรเนียมอยู่ที่โอ๊ก ริดจ์ รัฐเทนเนสซี และห้องทดลองออกแบบและวิจัยอาวุธคือสถาบันวิจัยแห่งชาติ ลอส อลามอส[42]
เครื่องปฏิกรณ์เครื่องแรกที่ผลิตพลูโทเนียม-239 ได้คือเครื่องปฏิกรณ์กราไฟท์ X-10 ซึ่งเริ่มเดินเครื่องในปี ค.ศ. 1943 สร้างขึ้นในโรงงานที่โอ๊ก ริดจ์ซึ่งภายหลังได้กลายมาเป็นสถาบันวิจัยแห่งชาติ โอ๊ก ริดจ์[28][note 5]
วันที่ 5 เมษายน ค.ศ. 1944 เอมีลีโอ เซแกระ (Emilio Segrè) ที่ลอส อลามอสได้รับตัวอย่างแรกของพลูโทเนียมที่ผลิตได้จากโอ๊ก ริดจ์[44] ภายในสิบวัน เขาพบว่าพลูโทเนียมที่ได้จากเครื่องปฏิกรณ์มีความเข้มข้นของไอโซโทป Pu-240 สูงกว่าพลูโทเนียมที่ผลิตด้วยเครื่องไซโคลตรอน Pu-240 มีอัตราการเกิดฟิชชันขึ้นเองสูงทำให้เกิดการยกระดับของระดับนิวตรอนพื้นหลังทั้งหมดของพลูโทเนียมตัวอย่าง อาวุธนิวเคลียร์แบบไกปืนรุ่นแรก ชื่อรหัส "ทินแมน (Thin Man)" ต้องถูกยกเลิกไปจากผลที่พบนี้เนื่องจากจำนวนนิวตรอนเกิดเองที่เพิ่มขึ้นอย่างมากนั้นอาจทำให้เกิดการระเบิดขึ้นได้
การออกแบบอาวุธที่ทำจากพลูโทเนียมที่ลอส อลามอสจึงถูกเปลี่ยนเป็นกลไกแบบจุดระเบิดภายในซึ่งซับซ้อนมากมีชื่อรหัสว่า "แฟตแมน" กลไกแบบจุดระเบิดภายในนั้น พลูโทเนียมทรงกลมแข็งจะถูกอัดให้มีความหนาแน่นสูงด้วยการระเบิดเข้าสู่ศูนย์กลาง เป็นเทคนิคที่ยากกว่าแบบไกปืนมาก แต่ก็สำคัญมากเช่นกันสำหรับอาวุธที่ต้องการใช้พลูโทเนียม (ยูเรเนียมเสริมสมรรถนะสามารถใช้วิธีนี้ได้เช่นกัน) [44]
เครื่องปฏิกรณ์-บีที่แฮนฟอร์ด ซึ่งเป็นเครื่องปฏิกรณ์นิวเคลียร์ขนาดใหญ่ใช้สำหรับผลิตวัสดุทางนิวเคลียร์ สร้างเสร็จสมบูรณ์ในเดือนมีนาคม ค.ศ. 1945[45] เครื่องปฏิกรณ์-บีได้ผลิตวัสดุฟิสไซล์สำหรับอาวุธที่ใช้พลูโทเนียมซึ่งใช้ในระหว่างสงครามโลกครั้งที่สอง[note 6] เครื่องปฏิกรณ์-บี, ดี และ เอฟ เป็นเครื่องปฏิกรณ์ชุดแรกที่สร้างขึ้นในแฮนฟอร์ด เครื่องปฏิกรณ์ที่ใช้ผลิตพลูโทเนียมอีกหกเครื่องนั้นสร้างขึ้นภายหลัง[45]
ในปี ค.ศ. 2004 มีการค้นพบตู้นิรภัยระหว่างหลุมฝังศพที่แฮนฟอร์ดนิวเคลียร์ไซต์ ภายในมีสิ่งของหลากหลายรวมถึงขวดแก้วขนาดใหญ่ที่บรรจุด้วยของเหลวคล้ายโคลนสีค่อนข้างขาวซึ่งภายหลังสามารถระบุได้ว่าเป็นตัวอย่างพลูโทเนียมเกรดอาวุธที่เก่ามาก ด้วยการวิเคราะทางไอโซโทปโดยสถาบันวิจัยแห่งชาติแปซิฟิกตะวันตกเฉียงเหนือแสดงว่าพลูโทเนียมในขวดนั้นผลิตจากเครื่องปฏิกรณ์ X-10 ที่โอ๊ก ริดจ์ระหว่างปี ค.ศ. 1944[48][49][50]
ทรินนิทีและระเบิดปรมาณูแฟตแมน
แก้การทดลองระเบิดปรมาณูครั้งแรกมีชื่อรหัสว่า "ทรินนิที" ถูกทดสอบในวันที่ 16 กรกฎาคม ค.ศ. 1945 ใกล้กับอะลาโมกอร์โด รัฐนิวเม็กซิโก ใช้พลูโทเนียมเป็นวัสดุฟิสไซล์[30] การออกแบบการระเบิดจากภายในของ "แกดเก็ต (Gadget)" ซึ่งเป็นกลุ่มกลไกที่มี 3 ชิ้นซึ่งเป็นที่มาของชื่อรหัสทรินนิทีนั้น ได้ใช้การรวมเลนส์ระเบิดเพื่อกดอัดพลูโทเนียมทรงกลมไปสู่มวลเหนือวิกฤต ซึ่งสาดด้วยนิวตรอนจำนวนมากมาพร้อมๆกันจากการสร้างตัวเริ่มต้นของพอโลเนียมและเบริลเลียม (ต้นกำเนิดนิวตรอน: (α, n) ปฏิกิริยาคายพลังงาน) [28] เพื่อรับประกันว่าจะเกิดปฏิกิริยาลูกโซ่และการระเบิดร่วมกัน โดยรวมอาวุธหนักมากกว่า 4 ตัน ถึงแม้ว่าจะใช้พลูโทเนียมเพียง 6.2 กก.เท่านั้นในส่วนแกนกลาง.[51] ประมาณ 20% ของพลูโทเนียมที่ใช้ในอาวุธในทดสอบทรินนิทีจะเกิดการแตกตัวของนิวเคลียสของอะตอม ผลของแรงระเบิดมีพลังงานเท่ากับทีเอ็นทีประมาณ 20,000 ตัน[52][note 7]
การออกแบบลักษณะเดียวกันนี้ใช้ใน "แฟตแมน" ระเบิดปรมาณูที่ถูกทิ้งเหนือเมืองนะงะซะกิ ประเทศญี่ปุ่น ในวันที่ 9 สิงหาคม ค.ศ. 1945 ฆ่าประชากรไป 70,000 คนและบาดเจ็บอีก 100,000 คน[28] ส่วนระเบิด "ลิตเติลบอย" ที่ทิ้งลงเหนือเมืองฮิโระชิมะ สามวันก่อนหน้านั้น ใช้ยูเรเนียม-235 ไม่ใช่พลูโทเนียม ญี่ปุ่นได้ยอมแพ้ในวันที่ 15 สิงหาคม ต่อนายพลดักลาส แมกอาเธอร์ส่งผลให้สงครามจบลง การมีอยู่ของพลูโทเนียมจึงเพิ่งได้เผยแพร่สู่สาธารณะหลังจากการประกาศของระเบิดปรมาณูลูกแรกนั่นเอง
สงครามเย็น
แก้ทั้งสหภาพโซเวียตและสหรัฐอเมริกาต่างสร้างคลังเก็บพลูโทเนียมเกรดสำหรับทำอาวุธขนาดใหญ่ในระหว่างยุคสงครามเย็น เตาแยกปฏิกรณ์ปรมาณูของสหรัฐอเมริกาที่แฮนฟอร์ดในรัฐวอชิงตันและแม่น้ำซาวานนาห์ในรัฐเซาท์แคโรไลนาสามารถผลิตพลูโทเนียมเกรดสำหรับทางทหารได้ 103 ตัน[54] และอีกประมาณ 170 ตันนั้นถูกผลิตในรัสเซีย[55][note 8] ในแต่ละปียังคงมีธาตุเกิดขึ้นจากผลพลอยได้ของอุตสาหกรรมพลังงานนิวเคลียร์ประมาณ 20 ตัน[13] พลูโทเนียมมากกว่า 1000 ตันอาจอยู่ในสถานที่เก็บรักษาซึ่งอาจมีมากกว่า 200 ตันที่อยู่ภายในหรือนำออกมาจากอาวุธนิวเคลียร์[28]
ตั้งแต่สงครามเย็นจบลง คลังเหล่านี้กลายเป็นจุดศูนย์รวมของความกังวลในการเพิ่มจำนวนอย่างรวดเร็วของนิวเคลียร์ ในสหรัฐอเมริกาพลูโทเนียมบางส่วนถูกถอดออกจากอาวุธนิวเคลียร์ที่ปลดประจำการถูกหลอมเป็นแท่งแก้วพลูโทเนียมออกไซด์ที่มีน้ำหนักถึง 2 ตัน[28] แก้วนั้นทำด้วยแก้วโบโรซิลิเคทผสมด้วยแคดเมียมและแกโดลิเนียม[note 9] แท่งแก้วเหล่านี้ถูกห่อหุ้มด้วยสเตนเลสและเก็บไว้ใต้ดินลึกกว่า 4 กม.ในหลุมที่ปิดทับด้วยคอนกรีต[28] ในปี ค.ศ. 2008 สหรัฐอเมริกาได้วางแผนที่จะเก็บพลูโทเนียมด้วยวิธีนี้ซึ่งหนทางที่ง่ายที่สุดในที่เก็บกากนิวเคลียร์เทือกเขายุกคาซึ่งประมาณ 160 กม.ทางตะวันออกเฉียงเหนือของลาสเวกัส รัฐเนวาดา[57] การต่อต้านจากท้องถิ่นและรัฐทำให้แผนที่จะเก็บกากนิวเคลียร์ไว้ที่เทือกเขายุกคาเลื่อนออกไป
การทดลองทางการแพทย์
แก้ในระหว่างและหลังสงครามโลกครั้งที่ 2 นักวิทยาศาสตร์ที่ทำงานอยู่ในโครงการแมนฮัตตันและโครงการวิจัยอาวุธนิวเคลียร์กลุ่มอื่น ได้ศึกษาผลของพลูโทเนียมต่อสัตว์ทดลองและต่อมนุษย์[58] ในสัตว์พบว่าพลูโทเนียม 2-3 มิลลิกรัมต่อเนื้อเยื่อ 1 กิโลกรัมนั้นสามารถทำให้ถึงตายได้[59]
ส่วนในกรณีที่ศึกษาในมนุษย์นั้น ได้มีการฉีดสารละลายพลูโทเนียม 5 ไมโครกรัมเข้าไปในร่างกายผู้ป่วยในโรงพยาบาล ที่เจ็บป่วยในระยะสุดท้ายจากสาเหตุอื่น หรือผู้ที่เจ็บป่วยเรื้อรังและคาดว่าจะมีชีวิตอยู่ได้อีกไม่เกิน 10 ปี[58] และลดเหลือ 1 ไมโครกรัมในเดือนกรกฎาคม ค.ศ. 1945 หลังจากการทดลองในสัตว์พบว่ามีการสะสมของพลูโทเนียมในกระดูกซึ่งมีอันตรายมากกว่าเรเดียม[59]
ผู้ป่วย 18 ราย ที่ไม่ได้รับแจ้งให้เจ้าตัวทราบ[58] ถูกใช้เพื่อใช้ในการวินิจฉัยสร้างข้อกำหนดในการดูดซึมพลูโทเนียมเข้าสู่ร่างกายเพื่อมาตรฐานความปลอดภัยสำหรับการทำงานกับพลูโทเนียม[58]
ในกรณีนี้ถือว่าเป็นการทำลายจริยธรรมและคำปฏิญาณทางการแพทย์อย่างร้ายแรง มีข้อคิดเห็นมากมายที่แสดงความคิดเห็นว่าแม้การกระทำนั้นจะถือว่าเป็นการทำลายต่อความเชื่อถือและจริยธรรม "ผลของพลูโทเนียมที่ฉีดเข้าไปในร่างกายผู้ป่วยไม่ได้ทำให้เกิดความเสียหายหรือเจ็บป่วยอย่างที่ถูกเสริมแต่งกันในข่าวตอนแรก จึงไม่มีนักวิทยาศาสตร์ใส่ใจและเชื่อเรื่องนี้มากนักทั้งใน ณ ขณะนั้นและในปัจจุบันนี้"[60]
การประยุกต์ใช้
แก้ระเบิด
แก้Pu-239 เป็นวัสดุฟิสไซล์ที่สำคัญในอาวุธนิวเคลียร์ เพราะเกิดการแตกตัวของนิวเคลียสอะตอมได้ง่าย พลูโทเนียมทรงกลมในระเบิดที่ห่อหุ้มด้วยตัวกระตุ้นนั้นลดผลรวมความต้องการของพลูโทเนียมให้เข้าสู่มวลวิกฤตโดยการสะท้อนนิวตรอนที่ถูกปลดปล่อยออกมากลับเข้าไปสู่แกนพลูโทเนียม การกระทำนี้ช่วยลดความต้องการเข้าสู่ค่าวิกฤต จากที่ต้องใช้พลูโทเนียม 16 กก. เหลือเพียง 10 กก.ที่มีเส้นผ่านศูนย์กลางประมาณ 10 ซม.[61] ค่ามวลวิกฤตนี้มีค่าประมาณหนึ่งในสามของ U-235[7]
"แฟตแมน"-ระเบิดที่ใช้พลูโทเนียมที่สร้างขึ้นในระหว่างโครงการแมนฮัตตัน ใช้การระเบิดบีบอัดของพลูโทเนียมที่มีความหนาแน่นสูงร่วมกับต้นกำเนิดนิวตรอนตรงกลางเพื่อเริ่มปฏิกิริยาและเพิ่มประสิทธิภาพ ดังนั้นจึงเหลือพลูโทเนียมเพียง 6.2 กก.ที่ต้องการสำหรับระเบิดที่มีแรงระเบิดเท่ากับทีเอ็นที 20 กิโลตัน[52][62] มีสมมุติฐานที่ว่าสำหรับผู้เชี่ยวชาญ พลูโทเนียมเพียง 4 กก.ก็สามารถสร้างระเบิดนิวเคลียร์ได้หนึ่งลูก[62]
การใช้ประโยชน์จากกากเชื้อเพลิงนิวเคลียร์
แก้PUREX เป็นกระบวนการที่นำกากเชื้อเพลิงนิวเคลียร์มาสกัดยูเรเนียมและพลูโทเนียมเพื่อให้กลายเป็นเชื้อเพลิงที่มีสารประกอบออกไซด์รวมอยู่ด้วย (MOX) สำหรับนำกลับมาใช้ใหม่ในเครื่องปฏิกรณ์นิวเคลียร์ พลูโทเนียมเกรดอาวุธสามารถนำไปเติมในเชื้อเพลิงผสมนั้นได้ เชื้อเพลิง MOX ที่ใช้ในเครื่องปฏิกรณ์นิวเคลียร์แบบน้ำมวลเบาประกอบไปด้วยพลูโทเนียม 60 กก.ต่อเชื้อเพลิงหนึ่งตัน หลังจากผ่านไป 4 ปี สามในสี่ส่วนของพลูโทเนียมจะเปลี่ยนกลายเป็นธาตุอื่นไป[28] เครื่องปฏิกรณ์ที่เพาะเชื้อเพลิงในตัวเองนั้นจะออกแบบเป็นพิเศษให้สามารถสร้างวัสดุฟิชชันได้มากกว่าที่ใช้ไป[63]
เชื้อเพลิง MOX เริ่มมีการใช้ตั้งแต่ในช่วงปี ค.ศ. 1980 และใช้กันอย่างกว้างขวางทั่วยุโรป[64] ในเดือนกันยายน ปี ค.ศ. 2000 สหรัฐอเมริกาและสหพันธรัฐรัสเซียทำข้อตกลงว่าด้วยการบริหารจัดการพลูโทเนียม ซึ่งมีใจความหนึ่งว่าจะทำลายพลูโทเนียมเกรดอาวุธจำนวนทั้งสิ้น 34 ตัน[65] กระทรวงพลังงานสหรัฐอเมริกามีแผนที่จะกำจัดพลูโทเนียมเกรดอาวุธ 34 ตันในสหรัฐอเมริกาก่อนสิ้นปี ค.ศ. 2019 โดยเปลี่ยนไปเป็นเชื้อเพลิง MOX เพื่อใช้ในเครื่องกำเนิดไฟฟ้าพลังงานนิวเคลียร์ในเชิงพานิชย์[65]
การเพิ่มประสิทธิภาพของเชื้อเพลิงสามารถทำได้ในกระบวนการนำกลับมาใช้ใหม่ด้วยเช่นกัน ในกระบวนการจะมีการจำกัดของเสียออกจากแท่งเชื้อเพลิงหลังจากใช้งานมาสามปี ประมาณ 3% จากน้ำหนักทั้งหมดของแท่งเชื้อเพลิง[28] ไอโซโทปต่าง ๆ ของยูเรเนียมและพลูโทเนียมที่สร้างขึ้นในระหว่างการใช้งานในสามปีนั้นจะถูกกำจัดออกและแท่งเชื้อเพลิงจะกลับนำเข้าสู่กระบวนการผลิตใหม่[note 10] อย่างไรก็ตาม แกลเลียมประมาณ 1% ต่อน้ำหนักพลูโทเนียมเกรดอาวุธมีศักยภาพในการแทรกแซงในระยะยาวของเครื่องปฏิกรณ์นิวเคลียร์แบบน้ำมวลเบา[66]
เมื่อเร็ว ๆ นี้มีการเสนอให้ใช้ 241Am เป็นตัวปรับโครงสร้างในแท่งเชื้อเพลิงพลูโทเนียมเพื่อทำให้ไม่สามารถนำแท่งเชื้อเพลิงนั้นไปผลิตเป็นอาวุธนิวเคลียร์ได้[67]
แหล่งพลังงานและความร้อน
แก้ไอโซโทปพลูโทเนียม-238 (Pu-238) มีครึ่งชีวิต 87.5 ปี ซึ่งปลดปล่อยพลังงานความร้อนออกมาจำนวนมากในระดับต่ำ เป็นรังสีแกมมา/อนุภาคและรังสีนิวตรอนที่เกิดขึ้นเองตามธรรมชาติ/อนุภาค[68] รังสีอนุภาคแอลฟาเป็นการรวมกันของการแผ่รังสีพลังงานสูงซึ่งมีการผ่านทะลุต่ำ และด้วยเหตุนั้นจึงป้องกันได้ง่าย เพียงแค่กำแพงกระดาษก็สามารถป้องกันการทะลุทะลวงของอนุภาคแอลฟาได้ โดย Pu-238 หนึ่งกิโลกรัมสามารถสร้างพลังงานความร้อนประมาณ 570 วัตต์[7][68]
ด้วยลักษณะพิเศษนี้ทำให้พลูโทเนียมเหมาะสมในการใช้สร้างอุปกรณ์กำเนิดพลังงานไฟฟ้าที่ไม่ต้องการการซ่อมบำรุงตลอดเวลาหนึ่งชั่วอายุคน ดังนั้นจึงมีการใช้พลูโทเนียมในเครื่องผลิตไฟฟ้าด้วยความร้อนจากไอโซโทปรังสีและหน่วยผลิตความร้อนด้วยไอโซโทปแผ่รังสี เช่นในยานแคสซีนี, โครงการวอยเอจเจอร์ และยานนิวฮอไรซันส์ เทคโนโลยีพลังงานแบบเดียวกันแรกสุดถูกใช้ในระบบ ALSEP และ EASEP รวมถึงการทดลองเรื่องแผ่นดินไหวในปฏิบัติการบนดวงจันทร์ของยานอะพอลโล 14[28]
พลูโทเนียม-238 เป็นแหล่งพลังงานของหัวใจเทียมเพซเมกเคอร์ (pacemaker:อุปกรณ์ไฟฟ้าที่ช่วยให้อัตราการเต้นของหัวใจสม่ำเสมอ) ที่ประสบความสำเร็จมาก เพราะช่วยลดความเสี่ยงต่อการผ่าตัดซ้ำๆเพื่อเปลี่ยนแหล่งพลังงาน[69][70] ก่อนจะถูกแทนที่ด้วยเซลล์ปฐมภูมิที่ใช้ลิเทียมเป็นพื้นฐาน แต่ใน ค.ศ. 2003 ยังมีเพซเมกเคอร์ 50 ถึง 100 ชิ้นที่ใช้พลูโทเนียมเป็นแหล่งพลังงาน ถูกฝังอยู่ในร่างกายผู้ป่วยที่ยังมีชีวิตอยู่[71] นอกจากนี้ยังมีการศึกษา Pu-238 เพื่อใช้ในการให้ความร้อนในการดำน้ำแบบสคูบา[72] พลูโทเนียม-238 ผสมกับเบริลเลียมถูกใช้ในการสร้างนิวตรอนเพื่อใช้ในงานวิจัย[28]
ข้อควรระวัง
แก้ความเป็นพิษ
แก้ไอโซโทปและสารประกอบพลูโทเนียมเป็นสารพิษที่มีความเป็นพิษสูงซึ่งมีสาเหตุมาจากภาวะกัมมันตภาพรังสี การปนเปื้อนของพลูโทเนียมออกไซด์ (พลูโทเนียมรวมตัวกับออกซิเจนด้วยตนเอง) เป็นผลมาจากอุบัติเหตุนิวเคลียร์ทางทหารเมื่ออาวุธนิวเคลียร์ถูกเผา[73]
พลูโทเนียมจะเป็นอันตรายมากถ้าเราหายใจเอาพลูโทเนียมเข้าไป อันตรายมากกว่าการรับประทานพลูโทเนียมเข้าไปเสียอีก ความเสี่ยงที่จะเป็นมะเร็งปอดจะเพิ่มขึ้นเมื่อรับรังสีในหนึ่งครั้งมีค่าปริมาณรังสีสมมูลของการหายใจเอารังสีเข้าไปเกินกว่า 400 mSv[74] กระทรวงพลังงานแห่งสหรัฐอเมริกาประมาณว่าความเสี่ยงต่อการเป็นมะเร็งในช่วงชีวิตเมื่อสูดเอาพลูโทเนียมเข้าไป 5,000 อนุภาคซึ่งแต่ละอนุภาคมีขนาด 3 ไมครอน จะมีความเสี่ยงเพิ่มขึ้น 1% จากค่าเฉลี่ยในสหรัฐอเมริกา[75] ร่างกายคนเราจะไม่ดูดซึมพลูโทเนียมจากการรับประทานเข้าไป (ร่างกายจะดูดซึมพลูโทเนียมออกไซด์เพียง 0.04% เท่านั้นจากการรับประทาน) [28] เมื่อพลูโทเนียมถูกดูดซึมเข้าสู่ร่างกาย จะถูกขับออกจากร่างกายอย่างช้าๆ ซึ่งมีครึ่งชีวิตทางชีวภาพ 200 ปี[76]
รังสีแอลฟาที่พลูโทเนียมปล่อยออกมาไม่สามารถทะลุผิวหนังเข้าไปได้ แต่สามารถฉายเข้าไปในอวัยวะภายในได้เมื่อรับประทานหรือสูดดมพลูโทเนียมเข้าไป[28] โดยเฉพาะกระดูกซึ่งดูดซับพลูโทเนียมอยู่บริเวณผิวหน้าของกระดูกและตับซึ่งจะสะสมพลูโทเนียมเข้มข้นขึ้นเรื่อยๆ[27]
เมื่อพิจารณาภาพรวมแล้วพลูโทเนียมอาจเป็นเหตุของการรับพิษรังสีอย่างรุนแรงจนถึงตายได้ถ้าสูดดมหรือรับประทานเข้าไป อย่างไรก็ตาม ยังไม่มีใครตายจากการสูดดมหรือรับประทานพลูโทเนียมและพบว่ามีหลายคนที่ตรวจพบพลูโทเนียมในร่างกาย[75]
ความสามารถในการเกิดวิกฤต
แก้สิ่งที่ต้องระวังอีกอย่างหนึ่งคือ ต้องระวังไม่ให้พลูโทเนียมสะสมจนถึงค่าของมวลวิกฤต เนื่องจากมวลวิกฤตของพลูโทเนียมมีค่าหนึ่งในสามของยูเรเนียม-235 เท่านั้น[7] พลูโทเนียมที่เกิดวิกฤตจะปลดปล่อยนิวตรอนและรังสีแกมมาออกมาทำให้ถึงตายได้[77] พลูโทเนียมในสารละลายสามารถมีมวลถึงระดับของมวลวิกฤตได้ง่ายกว่าของแข็งเพราะจากสารหน่วงนิวตรอนโดยไฮโดรเจนในน้ำ[13]
ในอดีตพลูโทเนียมเคยมีมวลถึงระดับวิกฤตโดยอุบัติเหตุมาแล้ว โดยบางครั้งทำให้เกิดอันตรายจนถึงแก่ชีวิต การจัดการกับแท่งสารประกอบคาร์บอน-ทังสเตนที่ล้อมรอบพลูโทเนียมทรงกลมหนักประมาณ 6.2 กก.ซึ่งเป็นระดับทำให้เป็นอันตรายถึงชีวิต อย่างขาดความระมัดระวังที่ลอส อลามอส ในวันที่ 21 สิงหาคม ค.ศ. 1945 เป็นผลให้ แฮรี่ เค เดกเลี่ยน จูเนียร์ (Harry K. Daghlian, Jr) นักวิทยาศาสตร์ โดยได้รับรังสีประมาณ 5.1 ซีเวอร์ต (510 rems) และตายใน 25 วันให้หลัง[78][79] เก้าเดือนถัดมา ลูอิส สโลทิน (Louis Slotin) นักวิทยาศาสตร์อีกคนหนึ่งของลอส อลามอส ก็เสียชีวิตในอุบัติเหตุลักษณะเดียวกัน โดยเกิดจากตัวสะท้อนเบริลเลียมและแกนพลูโทเนียม (หรือที่เรียกว่า "แก่นปีศาจ") ชุดเดียวกันกับที่ทำให้เดกเลี่ยนเสียชีวิต[80] เหตุการณ์นี้ถูกจำลองอยู่ในภาพยนตร์ ปี ค.ศ. 1989 เรื่อง แฟตแมนแอนด์ลิตเติลบอย
ในเดือนธันวาคม ปี ค.ศ. 1958 ระหว่างกระบวนการทำให้พลูโทเนียมบริสุทธิ์ที่ลอส อลามอสนั้น มวลในถังผสมได้เพิ่มขึ้นจนถึงระดับวิกฤต ทำให้ผู้ควบคุมเครนเสียชีวิต อุบัติเหตุในลักษณะเดียวกันนี้ได้เกิดขึ้นอีกในสหภาพโซเวียต ญี่ปุ่น สหรัฐอเมริกา และอีกหลายประเทศ[81]
ความสามารถในการติดไฟ
แก้โลหะพลูโทเนียมเป็นวัตถุติดไฟอันตราย โดยเฉพาะอย่างยิ่งถ้าเป็นผงละเอียด ในสิ่งแวดล้อมที่มีความชื้น พลูโทเนียมจะสร้างสารประกอบไฮโดรเจนบนผิวหน้าซึ่งอาจเกิดการลุกไหม้เองได้ในอากาศที่อุณหภูมิห้อง พลูโทเนียมเมื่อรวมตัวกับออกซิเจน ปริมาตรจะขยายมากกว่า 70% ของปริมาตรเดิม อาจทำให้หีบห่อที่บรรจุพลูโทเนียมนั้นแตกหักได้[82] กัมมันตภาพรังสีจากการไหม้ของวัสดุพลูโทเนียมจะยิ่งเพิ่มความอันตราย ทรายแม็กนีเซียมออกไซด์เป็นวัสดุที่ดีที่สุดในการใช้ดับไฟที่เกิดจากพลูโทเนียม โดยจะทำหน้าที่กันความร้อนและออกซิเจน วัสดุที่ช่วยระบายความร้อน เช่น ฮีตซิงก์ สามารถช่วยปิดกั้นออกซิเจนได้อีกด้วย ควรระมัดระวังเป็นพิเศษในการเก็บหรือใช้พลูโทเนียมในทุกรูปแบบ โดยทั่วไปแล้วจะเก็บในที่แห้งโดยมีบรรยากาศเป็นก๊าซเฉื่อย[82][note 11]
ดูเพิ่ม
แก้เชิงอรรถ
แก้- ↑ PuO2+ ไอออนนี้ไม่เสถียรจะเปลี่ยนไปเป็น Pu4+ และ PuO22+; Pu4+ จะรวมตัวกับออกซิเจนของ PuO2+ ที่เหลือ ไปเป็น PuO22+, ซึ่งจะลดทอนไปเป็น Pu3+ ดังนั้นสารละลายพลูโตเนียมที่เก็บไว้ระยะหนึ่งจึงมีส่วนผสมของ Pu3+ และ PuO22+
- Crooks, William J. (2002). "Nuclear Criticality Safety Engineering Training Module 10 – Criticality Safety in Material Processing Operations, Part 1" (PDF). คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ March 20, 2006. สืบค้นเมื่อ February 15, 2006.
- ↑ นี้ไม่ใช่ครั้งแรกที่มีผู้เสนอชื่อธาตุว่า "พลูโทเนียม" หนึ่งทศวรรษหลังแบเรียมถูกค้นพบ ศาสตราจารย์แห่งมหาวิทยาลัยเคมบริดจ์เสนอว่าแบเรียมควรเปลี่ยนชื่อเป็น"พลูโทเนียม"เพราะธาตุไม่ได้เป็นธาตุหนัก (ตามการเสนอจากรากศัพท์ภาษากรีกของชื่อที่ตั้งขึ้น barys = หนัก) เขาให้เหตุผลว่าตั้งแต่มันถูกสร้างโดยเทคนิคใหม่ของการสกัดสารเคมีด้วยกระแสไฟฟ้า ชื่อของมันควรเกี่ยวข้องกับไฟ ดังนั้นเขาจึงเสนอว่าควรเป็นชื่อเทพเจ้าแห่งยมโลกของชาวโรมัน เทพพลูโต
- ↑ ตามบทความที่มี อ้างถึงข้อมูลที่ซีบอร์กกล่าว: "จริงๆแล้วสัญลักษณ์ควรจะเป็น Pl แต่ตลกดีเมื่อซีบอร์กเสนอให้เป็น Pu ซึ่งเหมือนคำที่เด็กร้องอุทาน 'Pee-yoo! (พี-ยู) ' เมื่อได้กลิ่นบางอย่างที่แย่ๆ ซีบอร์กคิดว่าเขาจะได้รับการวิจารณ์ที่เผ็ดร้อนในการเสนอสัญลักษณ์นี้ แต่คณะกรรมการการตั้งชื่อได้ยอมรับโดยปราศจากข้อโต้แย้ง"[37]
- ↑ ห้อง 405 ของห้องปฏิบัติการจอร์จ เฮอร์เบิร์ต โจนส์ (George Herbert Jones) ซึ่งเป็นสถานที่แรกที่สามารถสกัดพลูโทเนียมได้ ได้ชื่อเป็นสิ่งสำคัญทางประวัติศาสตร์แห่งชาติเมื่อเดือนพฤษภาคม ค.ศ. 1967
- ↑ ระหว่างโครงการแมนฮัตตัน มักเรียกพลูโทเนียมกันอย่างง่ายๆว่า "49" โดยหมายเลข 4 มาจากเลขตัวสุดท้ายของ 94 (เลขอะตอมของพลูโทเนียม) และ 9 คือเลขตัวสุดท้ายของ Pu-239 ซึ่งเป็นไอโซโทปของวัสดุฟิสไซล์เกรดอาวุธที่ใช้ทำระเบิดนิวเคลียร์[43]
- ↑ The American Society of Mechanical Engineers (ASME, สมาคมวิศวกรเครื่องกลแห่งอเมริกา) กำหนดให้เครื่องปฏิกรณ์-บีเป็นสิ่งสำคัญเชิงวิศวกรรมเครื่องกลทางประวัติศาสตร์แห่งชาติในเดือนกันยายน ค.ศ. 1976[46] ในเดือนสิงหาคม ค.ศ. 2008 เครื่องปฏิกรณ์-บีได้ชื่อเป็นสิ่งสำคัญทางประวัติศาสตร์แห่งชาติของสหรัฐอเมริกา[47]
- ↑ การคำนวณประสิทธิภาพอยู่บนพื้นฐานของข้อเท็จจริงที่ว่า Pu-239 (หรือ U-235) 1 กก. ผลการแตกตัวของนิวเคลียสของอะตอม ปลดปล่อยพลังงานประมาณ 17 kt ถ้าพลูโทเนียมทรงกลมประมาณ 1.2 กก. การแตกตัวของนิวเคลียสของอะตอมจะให้ผลลัพธ์ 20 kt[53]
- ↑ พลูโทเนียมจำนวนมากนี้ถูกใช้สร้างแกนซึ่งแตกตัวได้ของอาวุธนิวเคลียร์ความร้อนที่ใช้การออกแบบเทลเลอร์-อูลาม (Teller–Ulam design) หรือที่เรียกว่า 'ระเบิดไฮโดรเจน' เป็นอาวุธนิวเคลียร์ชนิดหนึ่งที่ใช้การระเบิดแบบแตกตัวไปกระตุ้นนิวเคลียร์ฟิวชั่นของไอโซโทปไฮโดรเจนหนัก ผลการทำลายโดยทั่วไปในความแรงเทียบเท่าระเบิดทีเอ็นทีหนึ่งล้านตันเปรียบเทียบได้กับกลไกแตกตัวความแรงเทียบเท่าระเบิดทีเอ็นทีหนึ่งพันตันเท่านั้น[56]
- ↑ แกโดลิเนียม เซอร์โคเนียม ออกไซด์ (Gd2Zr2O7) ถูกพิจารณาเพราะมันสามารถหน่วงพลูโทเนียมได้มากกว่า 30 ล้านปี
- ↑ Breakdown of plutonium in a spent nuclear fuel rod: plutonium-239 (~58%), 240 (24%), 241 (11%), 242 (5%), and 238 (2%).[56]
- ↑ มีไฟไหม้ที่เกิดจากพลูโทเนียมที่รอกกี แฟลตส์ แพลนต์ (Rocky Flats Plant) ใกล้กับโบลเดอร์, รัฐโคโลราโด ในปี ค.ศ. 1969[83]
อ้างอิง
แก้- ↑ Calculated from the atomic weight and the atomic volume. The unit cell, containing 16 atoms, has a volume of 319.96 cubic Å, according to Siegfried S. Hecker (2000). "Plutonium and its alloys: from atoms to microstructure" (PDF). Los Alamos Science. 26: 331.. This gives a density for 239Pu of (1.66053906660×10−24g/dalton×239.0521634 daltons/atom×16 atoms/unit cell)/(319.96 Å3/unit cell × 10−24cc/Å3) or 19.85 g/cc.
- ↑ Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). "The NUBASE2020 evaluation of nuclear properties" (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ↑ Magurno & Pearlstein 1981, pp. 835 ff.
- ↑ 4.0 4.1 4.2 4.3 4.4 4.5 4.6 4.7 "Plutonium, Radioactive". Wireless Information System for Emergency Responders (WISER). Bethesda (MD): U.S. National Library of Medicine, National Institutes of Health. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ August 22, 2011. สืบค้นเมื่อ November 23, 2008. (public domain text)
- ↑ "Nitric acid processing". Actinide Research Quarterly. Los Alamos (NM): Los Alamos National Laboratory (3rd quarter). 2008. เก็บจากแหล่งเดิมเมื่อ September 18, 2016. สืบค้นเมื่อ February 9, 2010.
While plutonium dioxide is normally olive green, samples can be various colors. It is generally believed that the color is a function of chemical purity, stoichiometry, particle size, and method of preparation, although the color resulting from a given preparation method is not always reproducible.
- ↑ 6.0 6.1 6.2 6.3 6.4 6.5 6.6 6.7 Sonzogni, Alejandro A. (2008). "Chart of Nuclides". Upton: National Nuclear Data Center, Brookhaven National Laboratory. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ July 21, 2011. สืบค้นเมื่อ September 13, 2008.
- ↑ 7.00 7.01 7.02 7.03 7.04 7.05 7.06 7.07 7.08 7.09 Heiserman 1992, p. 338
- ↑ Rhodes 1986, pp. 659–660 Leona Marshall: "When you hold a lump of it in your hand, it feels warm, like a live rabbit"
- ↑ 9.0 9.1 9.2 9.3 9.4 Miner 1968, p. 544
- ↑ 10.0 10.1 10.2 Hecker, Siegfried S. (2000). "Plutonium and its alloys: from atoms to microstructure" (PDF). Los Alamos Science. 26: 290–335. เก็บ (PDF)จากแหล่งเดิมเมื่อ February 24, 2009. สืบค้นเมื่อ February 15, 2009.
- ↑ Hecker, Siegfried S.; Martz, Joseph C. (2000). "Aging of Plutonium and Its Alloys" (PDF). Los Alamos Science. Los Alamos, New Mexico: Los Alamos National Laboratory (26): 242. เก็บ (PDF)จากแหล่งเดิมเมื่อ April 28, 2021. สืบค้นเมื่อ February 15, 2009.
- ↑ 12.0 12.1 12.2 12.3 Baker, Richard D.; Hecker, Siegfried S.; Harbur, Delbert R. (1983). "Plutonium: A Wartime Nightmare but a Metallurgist's Dream" (PDF). Los Alamos Science. Los Alamos National Laboratory: 148, 150–151. เก็บ (PDF)จากแหล่งเดิมเมื่อ October 17, 2011. สืบค้นเมื่อ February 15, 2009.
- ↑ 13.0 13.1 13.2 13.3 13.4 13.5 13.6 13.7 Lide 2006, pp. 4–27
- ↑ 14.0 14.1 14.2 14.3 14.4 14.5 Miner 1968, p. 542
- ↑ 15.0 15.1 Stwertka 1998
- ↑ "Glossary – Fissile material". United States Nuclear Regulatory Commission. November 20, 2014. เก็บจากแหล่งเดิมเมื่อ February 4, 2015. สืบค้นเมื่อ February 5, 2015.
- ↑ Asimov 1988, p. 905
- ↑ Glasstone, Samuel; Redman, Leslie M. (June 1972). "An Introduction to Nuclear Weapons" (PDF). Atomic Energy Commission Division of Military Applications. p. 12. WASH-1038. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ August 27, 2009.
- ↑ Gosling 1999, p. 40
- ↑ "Plutonium: The First 50 Years" (PDF). U.S. Department of Energy. 1996. DOE/DP-1037. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ February 18, 2013.
- ↑ Kennedy, J. W.; Seaborg, G. T.; Segrè, E.; Wahl, A. C. (1946). "Properties of Element 94". Physical Review. 70 (7–8): 555–556. Bibcode:1946PhRv...70..555K. doi:10.1103/PhysRev.70.555.
- ↑ Greenwood 1997, p. 1259
- ↑ Seaborg, Glenn T.; McMillan, E.; Kennedy, J. W.; Wahl, A. C. (1946). "Radioactive Element 94 from Deuterons on Uranium". Physical Review. 69 (7–8): 366. Bibcode:1946PhRv...69..366S. doi:10.1103/PhysRev.69.366.
- ↑ "Can Reactor Grade Plutonium Produce Nuclear Fission Weapons?". Council for Nuclear Fuel Cycle Institute for Energy Economics, Japan. May 2001. เก็บจากแหล่งเดิมเมื่อ February 24, 2021. สืบค้นเมื่อ January 30, 2010.
- ↑ Matlack, George (2002). A Plutonium Primer: An Introduction to Plutonium Chemistry and its Radioactivity. Los Alamos National Laboratory. LA-UR-02-6594.
- ↑ Eagleson 1994, p. 840
- ↑ 27.0 27.1 27.2 27.3 27.4 Miner 1968, p. 545
- ↑ 28.00 28.01 28.02 28.03 28.04 28.05 28.06 28.07 28.08 28.09 28.10 28.11 28.12 28.13 28.14 28.15 28.16 28.17 28.18 28.19 Emsley 2001, pp. 324–329
- ↑ Hoffman, D. C.; Lawrence, F. O.; Mewherter, J. L.; Rourke, F. M. (1971). "Detection of Plutonium-244 in Nature". Nature. 234 (5325): 132–134. Bibcode:1971Natur.234..132H. doi:10.1038/234132a0. S2CID 4283169. Nr. 34.
- ↑ 30.0 30.1 30.2 30.3 Miner 1968, p. 541
- ↑ "Oklo: Natural Nuclear Reactors". U.S. Department of Energy, Office of Civilian Radioactive Waste Management. 2004. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ October 20, 2008. สืบค้นเมื่อ November 16, 2008.
- ↑ Curtis, David; Fabryka-Martin, June; Paul, Dixon; Cramer, Jan (1999). "Nature's uncommon elements: plutonium and technetium". Geochimica et Cosmochimica Acta. 63 (2): 275–285. Bibcode:1999GeCoA..63..275C. doi:10.1016/S0016-7037(98)00282-8. เก็บจากแหล่งเดิมเมื่อ June 27, 2021. สืบค้นเมื่อ June 29, 2019.
- ↑ Holden, Norman E. (2001). "A Short History of Nuclear Data and Its Evaluation". 51st Meeting of the USDOE Cross Section Evaluation Working Group. Upton (NY): National Nuclear Data Center, Brookhaven National Laboratory. เก็บจากแหล่งเดิมเมื่อ August 22, 2011. สืบค้นเมื่อ January 3, 2009.
- ↑ Fermi, Enrico (December 12, 1938). "Artificial radioactivity produced by neutron bombardment: Nobel Lecture" (PDF). Royal Swedish Academy of Sciences. เก็บ (PDF)จากแหล่งเดิมเมื่อ August 5, 2011. สืบค้นเมื่อ January 4, 2009.
- ↑ Darden, Lindley (1998). "The Nature of Scientific Inquiry". College Park: Department of Philosophy, University of Maryland. เก็บจากแหล่งเดิมเมื่อ August 17, 2012. สืบค้นเมื่อ January 3, 2008.
- ↑ Seaborg, Glenn T. "An Early History of LBNL: Elements 93 and 94". Advanced Computing for Science Department, Lawrence Berkeley National Laboratory. เก็บจากแหล่งเดิมเมื่อ November 5, 2014. สืบค้นเมื่อ September 17, 2008.
- ↑ 37.0 37.1 Clark, David L.; Hobart, David E. (2000). "Reflections on the Legacy of a Legend: Glenn T. Seaborg, 1912–1999" (PDF). Los Alamos Science. 26: 56–61, on 57. เก็บ (PDF)จากแหล่งเดิมเมื่อ June 3, 2016. สืบค้นเมื่อ February 15, 2009.
- ↑ "Frontline interview with Seaborg". Frontline. Public Broadcasting Service. 1997. เก็บจากแหล่งเดิมเมื่อ June 29, 2018. สืบค้นเมื่อ December 7, 2008.
- ↑ Glenn T. Seaborg (1977). "History of MET Lab Section C-I, April 1942 – April 1943". Office of Scientific & Technical Information Technical Reports. California Univ., Berkeley (USA). Lawrence Berkeley Lab. doi:10.2172/7110621. เก็บจากแหล่งเดิมเมื่อ March 15, 2020. สืบค้นเมื่อ June 29, 2019.
- ↑ "Room 405, George Herbert Jones Laboratory". National Park Service. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ February 8, 2008. สืบค้นเมื่อ December 14, 2008.
- ↑ Miner 1968, p. 540
- ↑ "Site Selection". LANL History. Los Alamos, New Mexico: Los Alamos National Laboratory. เก็บจากแหล่งเดิมเมื่อ September 13, 2011. สืบค้นเมื่อ December 23, 2008.
- ↑ Hammel, E. F. (2000). "The taming of "49" – Big Science in little time. Recollections of Edward F. Hammel, In: Cooper N.G. Ed. Challenges in Plutonium Science" (PDF). Los Alamos Science. 26 (1): 2–9. เก็บ (PDF)จากแหล่งเดิมเมื่อ January 20, 2017. สืบค้นเมื่อ February 15, 2009.
- Hecker, S. S. (2000). "Plutonium: an historical overview. In: Challenges in Plutonium Science". Los Alamos Science. 26 (1): 1–2. เก็บจากแหล่งเดิมเมื่อ January 18, 2017. สืบค้นเมื่อ February 15, 2009.
- ↑ 44.0 44.1 Sublette, Carey. "Atomic History Timeline 1942–1944". Washington (DC): Atomic Heritage Foundation. เก็บจากแหล่งเดิมเมื่อ January 4, 2009. สืบค้นเมื่อ December 22, 2008.
- ↑ 45.0 45.1 Wahlen 1989, p. iv, 1
- ↑ Wahlen 1989, p. 1.
- ↑ "Weekly List Actions". National Park Service. August 29, 2008. เก็บจากแหล่งเดิมเมื่อ October 31, 2008. สืบค้นเมื่อ August 30, 2008.
- ↑ Rincon, Paul (March 2, 2009). "BBC NEWS – Science & Environment – US nuclear relic found in bottle". BBC News. เก็บจากแหล่งเดิมเมื่อ March 2, 2009. สืบค้นเมื่อ March 2, 2009.
- ↑ Gebel, Erika (2009). "Old plutonium, new tricks". Analytical Chemistry. 81 (5): 1724. doi:10.1021/ac900093b.
- ↑ Schwantes, Jon M.; Matthew Douglas; Steven E. Bonde; James D. Briggs; และคณะ (2009). "Nuclear archeology in a bottle: Evidence of pre-Trinity U.S. weapons activities from a waste burial site". Analytical Chemistry. 81 (4): 1297–1306. doi:10.1021/ac802286a. PMID 19152306.
- ↑ Sublette, Carey (July 3, 2007). "8.1.1 The Design of Gadget, Fat Man, and "Joe 1" (RDS-1)". Nuclear Weapons Frequently Asked Questions, edition 2.18. The Nuclear Weapon Archive. สืบค้นเมื่อ January 4, 2008.
- ↑ 52.0 52.1 Malik, John (September 1985). "The Yields of the Hiroshima and Nagasaki Explosions" (PDF). Los Alamos. p. Table VI. LA-8819. เก็บ (PDF)จากแหล่งเดิมเมื่อ February 24, 2009. สืบค้นเมื่อ February 15, 2009.
- ↑ บนตัวเลขของ 1 กก. = 17 kt, ดู Garwin, Richard (October 4, 2002). "Proliferation of Nuclear Weapons and Materials to State and Non-State Actors: What It Means for the Future of Nuclear Power" (PDF). University of Michigan Symposium. Federation of American Scientists. เก็บ (PDF)จากแหล่งเดิมเมื่อ February 24, 2009. สืบค้นเมื่อ January 4, 2009.
- ↑ "Historic American Engineering Record: B Reactor (105-B Building)". Richland: U.S. Department of Energy. 2001. p. 110. DOE/RL-2001-16. เก็บจากแหล่งเดิมเมื่อ December 26, 2008. สืบค้นเมื่อ December 24, 2008.
- ↑ Cochran, Thomas B. (1997). Safeguarding nuclear weapons-usable materials in Russia (PDF). International Forum on Illegal Nuclear Traffic. Washington (DC): Natural Resources Defense Council, Inc. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ July 5, 2013. สืบค้นเมื่อ December 21, 2008.
- ↑ 56.0 56.1 Emsley 2001.
- ↑ Press Secretary (July 23, 2002). "President Signs Yucca Mountain Bill". Washington (DC): Office of the Press Secretary, White House. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ March 6, 2008. สืบค้นเมื่อ February 9, 2015.
- ↑ 58.0 58.1 58.2 58.3 Moss, William; Eckhardt, Roger (1995). "The Human Plutonium Injection Experiments" (PDF). Los Alamos Science. Los Alamos National Laboratory. 23: 188, 205, 208, 214. เก็บ (PDF)จากแหล่งเดิมเมื่อ January 14, 2009. สืบค้นเมื่อ June 6, 2006.
- ↑ 59.0 59.1 Voelz, George L. (2000). "Plutonium and Health: How great is the risk?". Los Alamos Science. Los Alamos (NM): Los Alamos National Laboratory (26): 78–79.
- ↑ Yesley, Michael S. (1995). "'Ethical Harm' and the Plutonium Injection Experiments" (PDF). Los Alamos Science. 23: 280–283. เก็บ (PDF)จากแหล่งเดิมเมื่อ February 24, 2009. สืบค้นเมื่อ February 15, 2009.
- ↑ Martin 2000, p. 532.
- ↑ 62.0 62.1 "Nuclear Weapon Design". Federation of American Scientists. 1998. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ December 26, 2008. สืบค้นเมื่อ December 7, 2008.
- ↑ Till & Chang 2011, p. 15.
- ↑ "Mixed Oxide (MOX) Fuel". London (UK): World Nuclear Association. 2006. เก็บจากแหล่งเดิมเมื่อ March 1, 2013. สืบค้นเมื่อ December 14, 2008.
- ↑ 65.0 65.1 "Plutonium Storage at the Department of Energy's Savannah River Site: First Annual Report to Congress" (PDF). Defense Nuclear Facilities Safety Board. 2004. pp. A–1. เก็บ (PDF)จากแหล่งเดิมเมื่อ February 17, 2017. สืบค้นเมื่อ February 15, 2009.
- ↑ Besmann, Theodore M. (2005). "Thermochemical Behavior of Gallium in Weapons-Material-Derived Mixed-Oxide Light Water Reactor (LWR) Fuel". Journal of the American Ceramic Society. 81 (12): 3071–3076. doi:10.1111/j.1151-2916.1998.tb02740.x. เก็บจากแหล่งเดิมเมื่อ March 17, 2020. สืบค้นเมื่อ June 29, 2019.
- ↑ "BGU combats nuclear proliferation". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2011-06-24. สืบค้นเมื่อ 2009-03-05.
- ↑ 68.0 68.1 "From heat sources to heart sources: Los Alamos made material for plutonium-powered pumper". Actinide Research Quarterly. Los Alamos: Los Alamos National Laboratory (1). 2005. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ February 16, 2013. สืบค้นเมื่อ February 15, 2009.
- ↑ Venkateswara Sarma Mallela; V. Ilankumaran & N.Srinivasa Rao (2004). "Trends in Cardiac Pacemaker Batteries". Indian Pacing Electrophysiol. 4 (4): 201–212. PMC 1502062. PMID 16943934.
- ↑ "Plutonium Powered Pacemaker (1974)". Oak Ridge Associated Universities. เก็บจากแหล่งเดิมเมื่อ October 29, 2021. สืบค้นเมื่อ October 11, 2021.
- ↑ "Plutonium Powered Pacemaker (1974)". Oak Ridge: Orau.org. 2021. เก็บจากแหล่งเดิมเมื่อ October 29, 2021. สืบค้นเมื่อ October 11, 2021.
- ↑ Bayles, John J.; Taylor, Douglas (1970). SEALAB III – Diver's Isotopic Swimsuit-Heater System (Report). Port Hueneme: Naval Civil Engineering Lab. AD0708680. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ March 12, 2020.
- ↑ "Toxicological Profile for Plutonium" (PDF). U.S. Department of Health and Human Services, Agency for Toxic Substances and Disease Registry (ATSDR). November 2010. เก็บ (PDF)จากแหล่งเดิมเมื่อ May 28, 2012. สืบค้นเมื่อ February 9, 2015.
- ↑ Brown, Shannon C.; Margaret F. Schonbeck; David McClure; และคณะ (July 2004). "Lung cancer and internal lung doses among plutonium workers at the Rocky Flats Plant: a case-control study". American Journal of Epidemiology. Oxford Journals. 160 (2): 163–172. doi:10.1093/aje/kwh192. PMID 15234938.
- ↑ 75.0 75.1 "ANL human health fact sheet—plutonium" (PDF). Argonne National Laboratory. 2001. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ February 16, 2013. สืบค้นเมื่อ June 16, 2007.
- ↑ "Radiological control technical training" (PDF). U.S. Department of Energy. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ June 30, 2007. สืบค้นเมื่อ December 14, 2008.
- ↑ Miner 1968, p. 546
- ↑ Roark, Kevin N. (2000). "Criticality accidents report issued". Los Alamos (NM): Los Alamos National Laboratory. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ October 8, 2008. สืบค้นเมื่อ November 16, 2008.
- ↑ Hunner 2004, p. 85.
- ↑ "Raemer Schreiber". Staff Biographies. Los Alamos: Los Alamos National Laboratory. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ January 3, 2013. สืบค้นเมื่อ November 16, 2008.
- ↑ McLaughlin, Monahan & Pruvost 2000, p. 17.
- ↑ 82.0 82.1 "Primer on Spontaneous Heating and Pyrophoricity – Pyrophoric Metals – Plutonium". Washington (DC): U.S. Department of Energy, Office of Nuclear Safety, Quality Assurance and Environment. 1994. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ April 28, 2007.
- ↑ Albright, David; O'Neill, Kevin (1999). "The Lessons of Nuclear Secrecy at Rocky Flats". ISIS Issue Brief. Institute for Science and International Security (ISIS). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ July 8, 2008. สืบค้นเมื่อ December 7, 2008.
บรรณานุกรม
แก้- Asimov, Isaac (1988). "Nuclear Reactors". Understanding Physics. New York: Barnes & Noble Publishing. ISBN 0-88029-251-2.
- Bernstein, Jeremy (2007). Plutonium: a History of the World's most Dangerous Element. Washington, D.C.: Joseph Henry Press. ISBN 978-0-309-10296-4. OCLC 76481517.
- Clark, Ronald (1961). The Birth of the Bomb: The Untold Story of Britain's Part in the Weapon That Changed the World. London: Phoenix House. OCLC 824335.
- Eagleson, Mary (1994). Concise Encyclopedia Chemistry. Berlin: Walter de Gruyter. ISBN 978-3-11-011451-5.
- Emsley, John (2001). "Plutonium". Nature's Building Blocks: An A–Z Guide to the Elements. Oxford (UK): Oxford University Press. ISBN 0-19-850340-7.
- Gosling, F. G. (1999). The Manhattan Project: Making the Atomic Bomb (PDF). Oak Ridge: United States Department of Energy. ISBN 0-7881-7880-6. DOE/MA-0001-01/99. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ February 24, 2009. สืบค้นเมื่อ February 15, 2009.
- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (2nd ed.). Oxford (UK): Butterworth-Heinemann. ISBN 0-7506-3365-4.
- Heiserman, David L. (1992). "Element 94: Plutonium". Exploring Chemical Elements and their Compounds. New York (NY): TAB Books. pp. 337–340. ISBN 0-8306-3018-X.
- Hoddeson, Lillian; Henriksen, Paul W.; Meade, Roger A.; Westfall, Catherine L. (1993). Critical Assembly: A Technical History of Los Alamos During the Oppenheimer Years, 1943–1945. New York: Cambridge University Press. ISBN 0-521-44132-3. OCLC 26764320.
- Hunner, Jon (2004). Inventing Los Alamos. University of Oklahoma Press. ISBN 978-0-8061-3891-6.
- Hurst, D. G.; Ward, A. G. (1956). Canadian Research Reactors (PDF). Ottawa: Atomic Energy of Canada Limited. OCLC 719819357. เก็บ (PDF)จากแหล่งเดิมเมื่อ February 5, 2015. สืบค้นเมื่อ February 6, 2015.
- Jha, D. K. (2004). Nuclear Energy. Discovery Publishing House. ISBN 81-7141-884-8. เก็บจากแหล่งเดิมเมื่อ January 6, 2022. สืบค้นเมื่อ January 6, 2022.
- Kaku, Michio; Trainer, Jennifer (1983). Nuclear Power, Both Sides: The Best Arguments for and Against the Most Controversial Technology. W. W. Norton & Company. ISBN 9780393301281. เก็บจากแหล่งเดิมเมื่อ January 6, 2022. สืบค้นเมื่อ December 8, 2013.
- Kay, A. E. (1965). plutonium 1965. Taylor & Francis. เก็บจากแหล่งเดิมเมื่อ January 6, 2022. สืบค้นเมื่อ January 6, 2022.
- Lide, David R., บ.ก. (2006). Handbook of Chemistry and Physics (87th ed.). Boca Raton: CRC Press, Taylor & Francis Group. ISBN 0-8493-0487-3.
- Magurno, B. A.; Pearlstein, S., บ.ก. (1981). Proceedings of the conference on nuclear data evaluation methods and procedures. BNL-NCS 51363 (PDF). Vol. II. Upton: Brookhaven National Laboratory. เก็บ (PDF)จากแหล่งเดิมเมื่อ March 8, 2021. สืบค้นเมื่อ August 6, 2014.
- Martin, James E. (2000). Physics for Radiation Protection. Wiley-Interscience. ISBN 0-471-35373-6.
- McLaughlin, Thomas P.; Monahan, Shean P.; Pruvost, Norman L. (2000). A Review of Criticality Accidents (PDF). Los Alamos: Los Alamos National Laboratory. LA-13638. เก็บ (PDF)จากแหล่งเดิมเมื่อ January 18, 2017. สืบค้นเมื่อ February 6, 2015.
- Miner, William N.; Schonfeld, Fred W. (1968). "Plutonium". ใน Clifford A. Hampel (บ.ก.). The Encyclopedia of the Chemical Elements. New York (NY): Reinhold Book Corporation. pp. 540–546. LCCN 68029938.
- Moody, Kenton James; Hutcheon, Ian D.; Grant, Patrick M. (2005). Nuclear forensic analysis. CRC Press. ISBN 0-8493-1513-1. เก็บจากแหล่งเดิมเมื่อ January 6, 2022. สืบค้นเมื่อ January 6, 2022.
- Rhodes, Richard (1986). The Making of the Atomic Bomb. New York: Simon & Schuster. ISBN 0-671-65719-4.
- Seaborg, G. T.; Seaborg, E. (2001). Adventures in the Atomic Age: From Watts to Washington. Farrar, Straus and Giroux. ISBN 0-374-29991-9.
- Sklar, Morty (1984). Nuke-Rebuke: Writers & Artists Against Nuclear Energy & Weapons. The Contemporary anthology series. The Spirit That Moves Us Press.
- Stockholm International Peace Research Institute (2007). SIPRI Yearbook 2007: Armaments, Disarmament, and International Security. Oxford University Press. ISBN 978-0-19-923021-1. เก็บจากแหล่งเดิมเมื่อ January 6, 2022. สืบค้นเมื่อ January 6, 2022.
- Till, C. E.; Chang, Y. I. (2011). Plentiful Energy: The Story of the Integral Fast Reactor, the Complex History of a Simple Reactor Technology, with Emphasis on Its Scientific Basis for Non-specialists. Charles E. Till and Yoon Il Chang. ISBN 978-1-4663-8460-6.
- Wahlen, R. K. (1989). History of 100-B Area (PDF). Richland, Washington: Westinghouse Hanford Company. WHC-EP-0273. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ March 27, 2009. สืบค้นเมื่อ February 15, 2009.
- Welsome, Eileen (2000). The Plutonium Files: America's Secret Medical Experiments in the Cold War. New York: Random House. ISBN 0-385-31954-1.
แหล่งข้อมูลอื่น
แก้- "Alsos Digital Library for Nuclear Issues – Plutonium". Washington and Lee University. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ February 3, 2009. สืบค้นเมื่อ February 15, 2009.
- Sutcliffe, W. G.; และคณะ (1995). "A Perspective on the Dangers of Plutonium". Lawrence Livermore National Laboratory. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ September 29, 2006.
- "Physical, Nuclear, and Chemical, Properties of Plutonium". IEER. 2005. สืบค้นเมื่อ February 15, 2009.
- "A History of Plutonium" (ภาษาอังกฤษ). Los Alamos National Laboratory. สืบค้นเมื่อ 8 July 2023.
- Bhadeshia, H. "Plutonium crystallography".
- Samuels, D. (2005). "End of the Plutonium Age". Discover Magazine. 26 (11).
- Pike, J.; Sherman, R. (2000). "Plutonium production". Federation of American Scientists. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ February 3, 2009. สืบค้นเมื่อ February 15, 2009.
- "Plutonium Manufacture and Fabrication".
- Ong, C. (1999). "World Plutonium Inventories". Nuclear Files.org. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ August 5, 2014. สืบค้นเมื่อ February 15, 2009.
- "Challenges in Plutonium Science". Los Alamos Science. I & II (26). 2000. สืบค้นเมื่อ February 15, 2009.
- "Plutonium". Royal Society of Chemistry. สืบค้นเมื่อ February 6, 2015.
- "Plutonium". The Periodic Table of Videos. University of Nottingham. สืบค้นเมื่อ February 6, 2015.