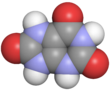
กรดยูริก
กรดยูริก (อังกฤษ: Uric acid) เป็นสารประกอบเฮเทอโรไซคลิก (heterocyclic) ที่มีคาร์บอน ไนโตรเจน ออกซิเจน และไฮโดรเจน โดยมีสูตรเคมีเป็น C5H4N4O3 มันมีรูปแบบทั้งเป็นไอออนและเกลือที่เรียกว่าเกลือยูเรต (urate) และเกลือกรดยูเรต (acid urate) เช่น ammonium acid urate กรดยูริกเป็นผลของกระบวนการสลายทางเมแทบอลิซึมของนิวคลีโอไทด์คือพิวรีน (purine) และเป็นองค์ประกอบปกติของปัสสาวะ การมีกรดยูริกในเลือดสูงอาจทำให้เกิดโรคเกาต์ และสัมพันธ์กับโรคอื่น ๆ รวมทั้งโรคเบาหวาน และนิ่วในไตที่เกิดจาก ammonium acid urate
| |||
 ผลึกของเกลือยูเรตในแสงโพลาไรซ์
| |||
| ชื่อ | |||
|---|---|---|---|
| Preferred IUPAC name
7,9-Dihydro-1H-purine-2,6,8(3H)-trione | |||
| ชื่ออื่น
2,6,8-Trioxypurine; 2,6,8-Trihydroxypurine; 2,6,8-Trioxopurine; 1H-Purine-2,6,8-trione
| |||
| เลขทะเบียน | |||
3D model (JSmol)
|
| ||
| 3DMet | |||
| 156158 | |||
| ChEBI | |||
| ChEMBL | |||
| เคมสไปเดอร์ | |||
| ดรักแบงก์ | |||
| ECHA InfoCard | 100.000.655 | ||
| EC Number |
| ||
| KEGG | |||
| MeSH | Uric+Acid | ||
ผับเคม CID
|
|||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| คุณสมบัติ | |||
| C5H4N4O3 | |||
| มวลโมเลกุล | 168.112 g·mol−1 | ||
| ลักษณะทางกายภาพ | ผลึกสีขาว | ||
| จุดหลอมเหลว | 300 องศาเซลเซียส (572 องศาฟาเรนไฮต์; 573 เคลวิน) | ||
| 6 mg/100 mL (at 20 °C) | |||
| log P | −1.107 | ||
| pKa | 5.6 | ||
| Basicity (pKb) | 8.4 | ||
| −6.62×10−5 cm3 mol−1 | |||
| อุณหเคมี | |||
ความจุความร้อน (C)
|
166.15 J K−1 mol−1 (at 24.0 °C) | ||
Std molar
entropy (S⦵298) |
173.2 J K−1 mol−1 | ||
Std enthalpy of
formation (ΔfH⦵298) |
−619.69 to −617.93 kJ mol−1 | ||
Std enthalpy of
combustion (ΔcH⦵298) |
−1921.2 to −1919.56 kJ mol−1 | ||
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |||
สภาพทางเคมี
แก้กรดยูริกเป็นกรดไดพร็อกติก (diprotic acid)[A] ประเภทหนึ่ง โดยมี pKa1 = 5.4 และ pKa2 = 10.3[3] ดังนั้น ในภาวะที่เป็นด่างมากคือมีค่า pH สูง มันจะอยู่ในรูปแบบไอออนยูเรตเต็มตัวและมีประจุสองหน่วย แต่ที่ค่า pH ในระบบชีวภาพ หรือเมื่อมีไอออนไบคาร์บอเนตอยู่ด้วย มันก็อยู่ในรูปแบบไฮโดรเจนยูเรต (hydrogen urate) หรือไอออนกรดยูเรต ซึ่งมีประจุหน่วยเดียว เนื่องจากการแตกตัวเป็นไอออนโดยประจุที่สองเกิดได้ง่ายมาก เกลือยูเรตแบบเต็มตัวจึงแยกสลายด้วยน้ำเป็นไฮโดรเจนยูเรตที่ค่า pH ประมาณกลาง ๆ มันเป็นสารประกอบแอโรแมติกเพราะการมี pi bonding ในวงแหวนทั้งสอง
เพราะเป็นสารอนุพันธ์ของพิวรีน (purine) แบบเฮเทอโรไซคลิก (heterocyclic) และไบไซคลิก (bicyclic) กรดยูริกจะไม่ให้โปรตอนคือ H+ (protonation) จากออกซิเจน (คือจากด้าน −OH) เหมือนกับกรดคาร์บอกซิลิก งานศึกษาด้วยการเลี้ยวเบนของรังสีเอกซ์กับไอออนของไฮโดรเจนยูเรตของผลึกแอมโมเนียมไฮโดรเจนยูเรต (ammonium hydrogen urate) ซึ่งเกิดในร่างกาย (in vivo) โดยเป็นตะกอนสะสมเนื่องจากโรคเกาต์ แสดงว่า ออกซิเจนแบบคีโทนในตำแหน่งที่ 2 ของโครงสร้างพิวรีน (บนคาร์บอนระหว่างไนโตรเจนสองอะตอมในวงแหวนที่มีสมาชิก 6 หน่วย) อยู่ในรูปแบบของ OH group ในขณะที่ออกซิเจนที่อยู่ข้าง ๆ ไนโตรเจนในตำแหน่งที่ 1 และ 3 มีประจุไอออนร่วมกันในวงแหวนแบบ pi-resonance-stabilized ที่มีสมาชิก 6 หน่วย
ดังนั้น ในขณะที่กรดอินทรีย์โดยมากจะให้โปรตอน (deprotonated) เนื่องกับการแตกตัวเป็นไอออนของพันธะเคมีไฮโดรเจน-ออกซิเจนที่มีขั้ว ปกติพร้อมกับการเกิด resonance stabilization โดยมีผลเป็นไอออนคาร์บอกซิเลต กรดยูริกจะให้โปรตอนจากอะตอมไนโตรเจน และจะใช้หมู่ keto/hydroxy ที่เป็นเทาโทเมอร์[B] สำหรับถอนอิเล็กตรอนเพื่อเพิ่มค่า pK1 วงแหวนที่มี 5 หน่วยยังมีหมู่ keto (ในตำแหน่งที่ 8) ล้อมรอบด้วยหมู่อะมิโนทุติยภูมิสองหน่วย (ในตำแหน่ง 7 และ 9) และการเสียโปรตอนของหน่วยเหล่านี้ที่ค่า pH สูงก็จะสามารถอธิบายค่า pK2 และปฏิกิริยาโดยเป็นกรดไดพร็อกติก[A] การจัดระเบียบใหม่เป็นเทาโทเมอร์[B] และ pi-resonance stabilization ในรูปแบบที่คล้ายกัน ก็จะทำให้ไอออนนี้เสถียรโดยระดับหนึ่ง
การคำนวณดูจะบ่งว่า ในสารละลาย (และในเฟสที่เป็นแก๊ส) รูปแบบที่มีประจุเดียวจะไม่มีไฮโดรเจนบนออกซิเจน และจะไม่มีไฮโดรเจนหนึ่งไม่ว่าจะเป็นบนไนโตรเจนตำแหน่ง 9 หรือบนไนโตรเจนตำแหน่ง 3 เทียบกับกรดยูริกที่ไม่ได้แตกประจุซึ่งจะมีไฮโดรเจนอยู่ที่ไนโตรเจนหมดทั้งสี่ตำแหน่ง[7] (ในโครงสร้างที่แสดงด้านบนขวา NH ที่บนขวาบนวงแหวนที่มี 6 หน่วยคือ "1" ถ้านับตามเข็มนาฬิกาไปรอบ ๆ วงแหวน "6" ก็คือคาร์บอนแบบคีโทนที่ยอดของวงแหวน ส่วน NH บนยอดของวงแหวนมี 5 หน่วยนับเป็น "7" เมื่อนับย้อนเข็มนาฬิกาตามวงแหวน NH ด้านล่างก็จะเป็น "9")
กรดยูริกแยกออกจากนิ่วไตเป็นครั้งแรกในปี ค.ศ. 1776 โดยนักเคมีชาวสวีเดน (Carl Wilhelm Scheele)[8] ต่อมาในปี 1882 นักเคมีชาวยูเครน (Ivan Horbaczewski) จึงเป็นคนแรกที่สังเคราะห์กรดยูเรตโดยหลอมละลายยูเรียกับไกลซีน[9]
สภาพละลายได้
แก้โดยทั่วไปแล้ว การละลายได้ของกรดยูริกและเกลือของมันที่เป็นโลหะแอลคาไลและโลหะแอลคาไลน์เอิร์ท จะค่อนข้างต่ำ เกลือทั้งหมดเหล่านี้ละลายในน้ำร้อนได้ดีกว่าน้ำเย็น ทำให้สามารถตกผลึกใหม่ได้ง่าย การละลายได้ไม่ดีเป็นสมุฏฐานสำคัญอย่างหนึ่งของโรคเกาต์ การละลายได้ของกรดและเกลือต่าง ๆ ของมันในเอทานอลจะต่ำมากหรือไม่สำคัญ เมื่ออยู่ในเอทานอลหรือในน้ำ เอทานอลและน้ำแทบจะมีค่าเป็นสารบริสุทธิ์
สภาพละลายได้ของเกลือยูเรต
(กรัมของน้ำ/กรัมของสาร)สารประกอบ น้ำเย็น น้ำเดือด กรดยูริก 15,000 2,000 Ammonium hydrogen urate — 1,600 Lithium hydrogen urate 370 39 Sodium hydrogen urate 1,175 124 Potassium hydrogen urate 790 75 Magnesium dihydrogen diurate 3,750 160 Calcium dihydrogen diurate 603 276 Disodium urate 77 — Dipotassium urate 44 35 Calcium urate 1,500 1,440 Strontium urate 4,300 1,790 Barium urate 7,900 2,700
ตัวเลขในตารางบ่งมวลน้ำที่จำเป็นเพื่อละลายมวลสารดังที่กำหนด ตัวเลขยิ่งต่ำเท่าไร ก็แสดงว่ายิ่งละลายได้มากขึ้นเท่านั้น[10][11][12]
ชีววิทยา
แก้เอนไซม์ xanthine oxidase จะเร่งปฏิกิริยาการสร้างกรดยูริกจาก xanthine และ hypoxanthine ซึ่งก็เป็นผลผลิตจากพิวรีนประเภทอื่น ๆ xanthine oxidase เป็นเอนไซม์โมเลกุลใหญ่ที่มีตำแหน่งกัมมันต์ซึ่งประกอบด้วยโลหะโมลิบดีนัมยึดอยู่กับกำมะถันและออกซิเจน[13] ภายในเซลล์ xanthine oxidase อาจอยู่ในรูปแบบ xanthine dehydrogenase และ xanthine oxireductase ซึ่งสามารถกลั่นได้จากนมและม้ามของวัวและควาย[14] ร่างกายจะหลั่งกรดยูริกออกเมื่อขาดออกซิเจน[15]
ในมนุษย์และไพรเมตระดับสูง กรดยูริก ปกติในรูปแบบไอออนไฮโดรเจนยูเรต จะเป็นผลผลิตขั้นสุดท้ายจากเมแทบอลิซึมของพิวรีน และขับออกทางปัสสาวะ ในสัตว์เลี้ยงลูกด้วยนมอื่น ๆ โดยมาก จะมีเอนไซม์ uricase ที่ช่วยเติมออกซิเจนและเปลี่ยนกรดให้กลายเป็น allantoin[16] การเสีย uricase ในไพรเมตระดับสูงคล้ายกับการเสียสมรรถภาพการผลิตวิตามินซี จึงเกิดสมมติฐานว่า ยูเรตอาจแทนวิตามินซีได้เป็นบางส่วนในสปีชีส์เหล่านี้[17] ทั้งกรดยูริกและวิตามินซีเป็นตัวลดออกซิเจน (reducing agent) ที่มีกำลังโดยเป็นตัวให้อิเล็กตรอน และเป็นสารต้านอนุมูลอิสระที่ดี ในมนุษย์ สมรรถภาพต้านอนุมูลอิสระครึ่งหนึ่งภายในน้ำเลือดจะมาจากไอออนไฮโดรเจนยูเรต[18]
ระดับความเข้มข้นของกรดยูริก (หรือไอออนไฮโดรเจนยูเรต) ในเลือดมนุษย์อยู่ที่ 25-80 มิลลิกรัม/ลิตร (mg/L) ในชาย และ 15-60 mg/L ในหญิง[19] (แต่ให้ดูต่อ ๆ ไปในเรื่องการมีค่าที่ต่างกว่าบ้าง) บุคคลหนึ่ง ๆ สามารถมีค่ากรดยูริกสูงถึง 96 mg/L โดยไม่มีโรคเกาต์[20] ในมนุษย์ ไตเป็นตัวกำจัดกรดยูริก 70% ในแต่ละวัน และในมนุษย์ 5-25% ภาวะไตเสื่อมจะทำให้เกิดภาวะกรดยูริกเกินในเลือด[21] การถ่ายกรดยูริกออกในปัสสาวะอยู่ระหว่าง 250-750 mg ต่อวัน เป็นความเข้มข้น 250-750 มิลลิกรัม/ลิตร (mg/L) ถ้าผลิตปัสสาวะ 1 ลิตรต่อวัน ซึ่งเป็นการละลายที่สูงกว่าการละลายได้ของกรดก็เพราะมันอยู่ในรูปแบบของ acid urate ละลาย
สุนัขพันธุ์แดลเมเชียนมีความบกพร่องทางพันธุกรรมในการดูดซึมกรดยูริกเข้าในตับและไต ทำให้เปลี่ยนกรดเป็น allantoin ลดลง ดังนั้น พันธุ์นี้จึงถ่ายกรดยูริกในปัสสาวะ ไม่ใช่ allantoin[22]
ในนกและสัตว์เลื้อยคลาน และในสัตว์เลี้ยงลูกด้วยนมที่อยู่ในทะเลทรายเป็นบางชนิด (เช่นสัตว์ฟันแทะในสกุล Dipodomys) กรดยูริกก็เป็นผลผลิตขั้นสุดท้ายจากเมทาบอลิซึมของพิวรีนด้วย แต่จะถ่ายออกในอุจจาระโดยเป็นของแห้ง ซึ่งจะต้องผ่านวิถีเมแทบอลิซึมที่ซับซ้อนและใช้พลังงานมากเทียบกับการแปรรูปของเสียที่เป็นไนโตรเจนอื่น ๆ เช่น ยูเรีย (จากวงจรยูเรีย) หรือแอมโมเนีย แต่ก็มีประโยชน์ลดการเสียน้ำและป้องกันภาวะขาดน้ำ[23]
ส่วนหนอนน้ำชั้นโพลีคีทาคือ Platynereis dumerilii กรดยูริกเป็นฟีโรโมนทางเพศที่ปล่อยออกในน้ำโดยตัวเมียเมื่อกำลังผสมพันธุ์ ซึ่งกระตุ้นให้ตัวผู้ปล่อยตัวอสุจิ[24]
พันธุศาสตร์
แก้คนส่วนหนึ่งจะมีการกลายพันธุ์ของโปรตีนที่มีหน้าที่ขับกรดยูริกออกผ่านไต ยีนที่มีส่วนร่วมกับการกลายพันธุ์นี้รวมทั้ง SLC2A9, ABCG2, SLC17A1, SLC22A11, SLC22A12, SLC16A9, GCKR, LRRC16A, และ PDZK1[25][26][27] โดย SLC2A9 พบว่า ขนส่งทั้งกรดยูริกและฟรักโทส[21][28][29]
การแพทย์และงานวิจัย
แก้ในน้ำเลือดมนุษย์ พิสัยอ้างอิงของกรดยูริกปกติจะอยู่ระหว่าง 3.4-7.2 mg/dL (200-430 µmol/L) สำหรับชาย และ 4-6.1 mg/dL (140-360 µmol/L) สำหรับหญิง[30] โดย 1 mg/dL จะเท่ากับ 59.48 µmol/L ความเข้มข้นกรดยูริกในเลือดที่สูงหรือต่ำกว่าพิสัยปกติเป็นอาการที่เรียกว่า ภาวะกรดยูริกเกินในเลือด (hyperuricemia) และภาวะกรดยูริกต่ำในเลือด (hypouricemia) โดยนัยเดียวกัน กรดยูริกที่สูงหรือต่ำกว่าปกติในปัสสาวะเรียกว่า ภาวะกรดยูริกเกินในปัสสาวะ (hyperuricosuria) และภาวะกรดยูริกต่ำในปัสสาวะ (hypouricosuria) ระดับกรดยูริกในน้ำลายอาจสัมพันธ์กับระดับกรดในเลือด[31]
กรดยูริกสูง
แก้ภาวะกรดยูริกเกินในเลือด (hyperuricemia) ซึ่งกระตุ้นให้เกิดโรคเกาต์ อาจมีแหล่งกำเนิดหลายเหตุ
- อาหารอาจเป็นปัจจัย คือ การทานอาหารจำนวนมากที่มีสารประกอบอินทรีย์คือพิวรีน ที่มีน้ำเชื่อมข้าวโพดซึ่งมีฟรักโทสสูง และที่มีน้ำตาล อาจเพิ่มระดับกรดยูริก[32][33] (ดูเพิ่มที่ ภาวะกรดยูริกเกินในเลือด#การผลิตกรดยูริกเพิ่ม)
- กรดยูริกในเลือดอาจเพิ่มเพราะไตขับกรดออกน้อยลง[34]
- การอดอาหารหรืออการลดน้ำหนักอย่างรวดเร็วสามารถเพิ่มระดับกรดยูริกอย่างชั่วคราว[35]
- ยาบางชนิด เช่น ยาขับปัสสาวะกลุ่ม thiazide สามารถเพิ่มระดับกรดยูริกในเลือดโดยขัดขวางการกำจัดกรดของไต[36]
- กลุ่มอาการอาการเนื้องอกสลาย (Tumor lysis syndrome) ซึ่งเป็นภาวะแทรกซ้อนของมะเร็งหรือเคมีบำบัดบางอย่าง เกิดจากการขับ nucleobase[C] และโพแทสเซียมของเซลล์ที่ตายออกในกระแสเลือด[37]
โรคเกาต์
แก้การมีกรดยูริกเกินในเลือดสามารถกระตุ้นให้เกิดโรคเกาต์[38] ซึ่งเป็นโรคสร้างความเจ็บปวดโดยมีผลเป็นกรดยูริกตกผลึกเป็นรูปเข็มที่ข้อต่อ หลอดเลือดฝอย ผิวหนัง และเนื้อเยื่ออื่น ๆ[39] โรคเกาต์สามารถเกิดเมื่ระดับกรดยูริกในเลือดอาจถึงค่าเพียงแค่ 6 mg/dL (~357 µmol/L) แต่บุคคลหนึ่ง ๆ ก็อาจมีค่าถึง 9.6 mg/dL (~565 µmol/L) และก็ยังไม่เกิดโรค[20]
ในมนุษย์ พิวรีนจะผ่านเมแทบอลิซึมกลายเป็นกรดยูริกแล้วก็จะขับออกทางปัสสาวะ การบริโภคอาหารที่มีพิวรีนสูงบางประเภท โดยเฉพาะเนื้อสัตว์และอาหารทะเล จะเพิ่มโอกาสเสี่ยง[40]
การจำกัดอาหารอาจช่วยลดระดับกรดยูริกในเลือด แม้จะไม่ใช่วิธีรักษาให้หาย แต่ก็อาจช่วยลดความเสี่ยงที่โรคจะแย่ลงจนถึงกับเจ็บ และช่วยชลอความเสียหายต่อข้อต่อที่เป็นไปอย่างต่อเนื่อง อาหารบางอย่างควรหลีกเลี่ยงแต่ก็ไม่ใช่อาหารที่มีพิวรีนทั้งหมด เป้าหมายของโปรแกรมอาหารก็เพื่อลดความเสี่ยง ช่วยรักษาโรค มีน้ำหนักที่พอดี และทานอาหารถูกสุขภาพ อาหารที่ควรเลี่ยงรวมทั้งเครื่องในสัตว์รวมทั้ง ตับ ไต ต่อมไทมัส ตับอ่อน และอาหารทะเลบางชนิดรวมทั้งปลาแอนโชวี่ ปลาเฮร์ริง ปลาซาร์ดีน หอยแมลงภู่ หอยเชลล์ ปลาเทราท์ ปลาแฮดด็อก ปลาแมกเคอเรล และปลาทูน่า[41] การทานผักที่มีพิวรีนสูงโดยทั่วไป[34] หรือโดยพอประมาณ[40] ไม่สัมพันธ์กับความเสี่ยงโรคที่สูงขึ้น
การรักษาโรคอย่างหนึ่งในคริสต์ศตวรรษที่ 19 ก็คือการให้ทานเกลือลิเทียม[42] เพราะ lithium urate จะละลายน้ำได้ดีกว่า ทุกวันนี้ ความบวมในช่วงที่เจ็บมักจะรักษาด้วยยาแก้อักเสบชนิดไม่ใช่สเตอรอยด์ (NSAID) โคลชิซีน หรือ corticosteroid และจะบริหารระดับยูเรตด้วย allopurinol[43] ซึ่งมีฤทธิ์ระงับ xanthine oxidase อย่างอ่อน ๆ และมีฤทธิ์คล้าย ๆ (คือเป็น analog) ของ hypoxanthine โดย xanthine oxidoreductase จะเป็นตัวเพิ่มหมู่ไฮดรอกซิลผ่านกระบวนการ hydroxylation ที่ตำแหน่งที่สองทำให้กลายเป็น oxipurinol[44]
กลุ่มอาการเนื้องอกสลาย (Tumor lysis syndrome)
แก้กลุ่มอาการเนื้องอกสลาย (Tumor lysis syndrome) เป็นอาการฉุกเฉินที่เป็นผลมาจากมะเร็งเม็ดเลือด ที่ก่อให้เกิดกรดยูริกระดับสูงในเลือด โดยเซลล์เนื้องอกปล่อยสารในเซลล์ออกในเลือด ไม่ว่าจะเกิดเองหรือหลังจากได้เคมีบำบัด[45] อาการอาจทำให้ไตเสียหายอย่างเฉียบพลันเมื่อกรดยูริกตกผลึกที่ไต[45] การรักษารวมทั้งการให้น้ำ (hyperhydration) เพื่อทำให้กรดยูริกเจือจางแล้วขับออกทางปัสสาวะ ให้ยา rasburicase เพื่อลดระดับกรดยูริกที่ไม่ละลายในเลือด หรือให้ allopurinol เพื่อห้ามกระบวนการแคแทบอลิซึมของพิวรีนเพื่อไม่ให้เพิ่มระดับกรดยูริก[45]
Lesch-Nyhan syndrome
แก้Lesch-Nyhan syndrome เป็นโรคทางพันธุกรรมที่มีน้อย และสัมพันธ์กับระดับกรดยูริกในเลือดสูง[46] และมีอาการอื่น ๆ รวมทั้งภาวะกล้ามเนื้อหดเกร็ง การเคลื่อนไหวนอกอำนาจใจ ปัญญาอ่อน (cognitive retardation) และอาการต่าง ๆ ของโรคเกาต์[47]
โรคหลอดเลือดเลี้ยงหัวใจ
แก้ภาวะกรดยูริกเกินในเลือดอาจเพิ่มปัจจัยเสี่ยงให้เกิดโรคหลอดเลือดเลี้ยงหัวใจ[48]
โรคเบาหวานแบบ 2
แก้ภาวะกรดยูริกเกินในเลือดอาจเป็นผลของการดื้ออินซูลินเพราะโรคเบาหวาน โดยไม่ใช่อาการตั้งต้นของโรค[49] งานศึกษาหนึ่งแสดงว่า ระดับกรดยูริกในเลือดสูงจะสัมพันธ์กับความเสี่ยงโรคเบาหวานแบบ 2 ที่สูงกว่า ต่างหากจากโรคอ้วน สัมพันธ์กับภาวะไขมันในเลือดผิดปกติ (dyslipidemia) และความดันโลหิตสูง[50] ภาวะกรดยูริกเกินในเลือดยังสัมพันธ์กับองค์ประกอบต่าง ๆ ของกลุ่มอาการทางเมแทบอลิซึม (metabolic syndrome) รวมทั้งในเด็ก[51][52]
การเกิดนิ่วกรดยูริก
แก้นิ่วไตสามารถเกิดโดยการสะสมจุลผลึกของโซเดียมยูเรต[53][54]
ความอิ่มตัวของกรดยูริกในเลือดอาจมีผลเป็นรูปแบบหนึ่งของนิ่วในไตเมื่อยูเรตตกผลึกในไต นิ่วกรดยูริกเหล่านี้โปร่งรังสี ดังนั้น จึงไม่ปรากฏในภาพเอกซ์เรย์ท้องธรรมดา ๆ[55] ผลึกกรดยูริกยังส่งเสริมให้เกิดนิ่วแบบแคลเซียมออกซาเลต โดยเป็นเหมือนกับผลึกล่อ/เริ่มต้น[56]
กรดยูริกต่ำ
แก้ภาวะกรดยูริกต่ำในเลือด (hypouricemia) มีเหตุหลายอย่าง การได้สังกะสีจากอาหารน้อยจะทำให้กรดยูริกต่ำ ผลเช่นนี้อาจชัดขึ้นในหญิงที่ทานยาคุมกำเนิด[57] ยาที่ใช้ป้องกันภาวะฟอสเฟตเกินในเลือด (hyperphosphataemia) ที่บ่งใช้ในคนไข้โรคไตเรื้อรัง ก็สามารถลดระดับกรดยูริกในเลือดอย่างสำคัญ[58]
โรคปลอกประสาทเสื่อมแข็ง
แก้งานวิเคราะห์อภิมานในงานศึกษาที่มีกลุ่มควบคุม 10 งานแสดงว่า ระดับกรดยูริกในเลือดของคนไข้โรคปลอกประสาทเสื่อมแข็งจะต่ำกว่ากลุ่มควบคุมปกติอย่างสำคัญ ซึ่งอาจชี้ว่า นี่เป็นอาการส่อทางชีวภาพของโรคนี้[59]
การทำระดับกรดยูริกต่ำให้ปกติ
แก้การแก้ปัญหาสังกะสีต่ำหรือได้ไม่พอ อาจช่วยเพิ่มระดับกรดยูริกในเลือด[60]
เชิงอรรถ
แก้- ↑ 1.0 1.1 ในสาขาเคมี กรดไดพร็อกติก (diprotic acid) เป็นกรด Arrhenius ชั้นหนึ่งที่สามารถให้โปรตอนหรือแคตไอออนไฮโดรเจนสองหน่วยต่อโมเลกุลเมื่อละลายในสารละลาย[1][2] ลักษณะทางเคมีที่สำคัญที่สุดของโมเลกุลกรดไดพร็อกติกหนึ่ง ๆ ก็คือสมรรถภาพในการให้โปรตอน (deprotonation) สองหน่วยเป็นลำดับต่อ ๆ กันสองต่อเมื่อละลาย นอกจากเป็นกรดสามัญที่ใช้ทุกวันในกิจต่าง ๆ ก็ยังมีอยู่ทั่วไปในธรรมชาติ เช่นในร่างกายมนุษย์
- ↑ 2.0 2.1 เทาโทเมอร์ (tautomer) เป็นไอโซเมอร์โดยโครงสร้าง (structural isomer) ต่าง ๆ ของสารประกอบอินทรีย์ที่สามารถเปลี่ยนเป็นกันและกันได้ง่าย ๆ[4][5][6] ปฏิกิริยาเช่นนี้มักจะมีผลเปลี่ยนตำแหน่งโปรตอนหนึ่ง ๆ แม้จะเป็นเรื่องซับซ้อน แต่ tautomerism ก็สำคัญต่อปฏิกิริยาของกรดอะมิโนและกรดนิวคลีอิก ซึ่งเป็นโครงสร้างพื้นฐานในสิ่งมีชีวิต
- ↑ Nucleobases เป็นสารประกอบชีวภาพที่สร้าง nucleosides ซึ่งก็เป็นองค์ประกอบของ nucleotides ทั้งหมดเป็นมอนอเมอร์ (monomer) ที่เป็นโครงสร้างพื้นฐานของกรดนิวคลีอิก บ่อยครั้งจะเรียกเฉย ๆ ว่า เบส เช่นในสาขาพันธุศาสตร์ สมรรถภาพของ nucleobases เพื่อสร้าง base pair และในการนำมาต่อ ๆ กัน นำไปสู่โครงสร้างฮีลิกซ์รูปเกลียวเป็นโซ่ยาว เช่นที่พบในอาร์เอ็นเอและดีเอ็นเอ
อ้างอิง
แก้- ↑ "Diprotic Acid Definition". About.com Education. สืบค้นเมื่อ 2016-01-22.
- ↑ "What is a Diprotic Acid?". wiseGEEK. สืบค้นเมื่อ 2016-01-23.
- ↑ McCrudden, Francis H. (2008). Uric Acid. BiblioBazaar. ISBN 978-0554619910.
- ↑ Antonov, L (2011). Tautomerism: Methods and Theories (1st ed.). Weinheim: Wiley-VCH. ISBN 978-3-527-33294-6.
- ↑
Smith, MB; March, J (2001). Advanced Organic Chemistry (5th ed.). New York: Wiley Interscience. pp. 1218–1211. ISBN 0-471-58589-0.
{{cite book}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑
Katritzky, AR; Elguero, J; และคณะ (1971). The Tautomerism of heterocycles. New York: Academic Press. ISBN 0-12-020651-X.
{{cite book}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jiménez, Verónica; Alderete, Joel B (2005-11-30). "Theoretical calculations on the tautomerism of uric acid in gas phase and aqueous solution". Journal of Molecular Structure: THEOCHEM. 755: 209–214. doi:10.1016/j.theochem.2005.08.001.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Scheele, C. W. (1776). "Examen Chemicum Calculi Urinari" [A chemical examiniation of kidney stones]. Opuscula. 2: 73.
- ↑ Horbaczewski, Johann (1882). "Synthese der Harnsäure" [Synthesis of uric acid]. Monatshefte für Chemie und verwandte Teile anderer Wissenschaften. 3: 796–797.
- ↑ CRC Handbook of Chemistry and Physics (62nd ed.).
- ↑ Merck Index (9th ed.).
- ↑ McCrudden, Francis H. Uric acid. p. 58.
- ↑ Hille, R. (2005). "Molybdenum-containing hydroxylases". Archives of Biochemistry and Biophysics. 433 (1): 107–116. doi:10.1016/j.abb.2004.08.012. PMID 15581570.
- ↑ Hori, N.; Uehara, K.; Mikami, Y. (1992). "Enzymatic Synthesis of 5-Methyluridine from Adenosine and Thymine with High Efficiency". Biosci. Biotechnol. Biochem. 56 (4): 580–582. doi:10.1271/bbb.56.580.
- ↑ Baillie, J. K.; Bates, M. G.; Thompson, A. A.; Waring, W. S.; Partridge, R. W.; Schnopp, M. F.; Simpson, A.; Gulliver-Sloan, F.; Maxwell, S. R.; Webb, D. J. (May 2007). "Endogenous urate production augments plasma antioxidant capacity in healthy lowland subjects exposed to high altitude". Chest. 131 (5): 1473–1478. doi:10.1378/chest.06-2235. PMID 17494796.
- ↑ Angstadt, Carol N. (1997-12-04). "Purine and Pyrimidine Metabolism: Purine Catabolism". NetBiochem.
- ↑ Proctor, P. (November 1970). "Similar functions of uric acid and ascorbate in man?". Nature. 228 (5274): 868. Bibcode:1970Natur.228..868P. doi:10.1038/228868a0. PMID 5477017. S2CID 4146946.
- ↑ Maxwell, S. R. J.; Thomason, H.; Sandler, D.; Leguen, C.; Baxter, M. A.; Thorpe, G. H. G.; Jones, A. F.; Barnett, A. H. (1997). "Antioxidant status in patients with uncomplicated insulin-dependent and non-insulin-dependent diabetes mellitus". European Journal of Clinical Investigation. 27 (6): 484–490. doi:10.1046/j.1365-2362.1997.1390687.x. PMID 9229228.
- ↑ Harrison's Principles of Internal Medicine (11th ed.). 1987. p. A-3.
- ↑ 20.0 20.1 Tausche, A. K.; Unger, S.; Richter, K.; และคณะ (May 2006). "Hyperurikämie und Gicht" [Hyperuricemia and gout: diagnosis and therapy]. Der Internist (ภาษาเยอรมัน). 47 (5): 509–521. doi:10.1007/s00108-006-1578-y. PMID 16586130. S2CID 11480796.
- ↑ 21.0 21.1 Vitart, V.; Rudan, I.; Hayward, C.; และคณะ (April 2008). "SLC2A9 is a newly identified urate transporter influencing serum urate concentration, urate excretion and gout". Nature Genetics. 40 (4): 437–442. doi:10.1038/ng.106. PMID 18327257. S2CID 6720464.
- ↑ Friedman, M. & Byers, S. O. (1 September 1948). "Observations concerning the causes of the excess excretion of uric acid in the Dalmatian dog". The Journal of Biological Chemistry. 175 (2): 727–735. doi:10.1016/S0021-9258(18)57191-X. PMID 18880769.
- ↑ Hazard, L. C. (2004). Sodium and Potassium Secretion by Iguana Salt Glands. Iguanas: Biology and Conservation. University of California Press. pp. 84–85. ISBN 978-0-520-23854-1.
- ↑ Zeeck, E.; Harder, T.; Beckmann, M. (1998). "Uric acid: the sperm-release pheromone of the marine polychaete Platynereis dumerilii". Journal of Chemical Ecology. 24 (1): 13–22. doi:10.1023/A:1022328610423. S2CID 42318049.
- ↑ Aringer, M.; Graessler, J. (December 2008). "Understanding deficient elimination of uric acid". Lancet. 372 (9654): 1929–1930. doi:10.1016/S0140-6736(08)61344-6. PMID 18834627. S2CID 1839089.
- ↑ Kolz, M.; Johnson, T.; และคณะ (June 2009). Allison, David B. (บ.ก.). "Meta-analysis of 28,141 individuals identifies common variants within five new loci that influence uric acid concentrations". PLOS Genet. 5 (6): e1000504. doi:10.1371/journal.pgen.1000504. PMC 2683940. PMID 19503597.
- ↑ Köttgen, A.; และคณะ (February 2013). "Genome-wide association analyses identify 18 new loci associated with serum urate concentrations" (PDF). Nature Genetics. 45 (2): 145–154. doi:10.1038/ng.2500. PMC 3663712. PMID 23263486.
- ↑ Döring, A.; Gieger, C.; Mehta, D.; และคณะ (April 2008). "SLC2A9 influences uric acid concentrations with pronounced sex-specific effects". Nature Genetics. 40 (4): 430–436. doi:10.1038/ng.107. PMID 18327256. S2CID 29751482.
- ↑ Mandal, Asim K.; Mount, David B. (February 2015). "The molecular physiology of uric acid homeostasis". Annual Review of Physiology. 77: 323–345. doi:10.1146/annurev-physiol-021113-170343. PMID 25422986.
- ↑ "Harmonisation of Reference Intervals" (PDF). Pathology Harmony (UK). คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2 August 2013. สืบค้นเมื่อ 13 August 2013.
- ↑ Zhao, J; Huang, Y (2015). "Salivary uric acid as a noninvasive biomarker for monitoring the efficacy of urate-lowering therapy in a patient with chronic gouty arthropathy". Clinica Chimica Acta. 450: 115–20. doi:10.1016/j.cca.2015.08.005. PMID 26276048.
- ↑ Cirillo, P.; Sato, W.; Reungjui, S.; และคณะ (December 2006). "Uric acid, the metabolic syndrome, and renal disease" (PDF). Journal of the American Society of Nephrology. 17 (12 Suppl. 3): S165–S168. doi:10.1681/ASN.2006080909. PMID 17130256.
- ↑ Angelopoulos, T. J.; Lowndes, J.; Zukley, L.; Melanson, K. J.; Nguyen, V.; Huffman, A.; Rippe, J. M. (June 2009). "The Effect of High-Fructose Corn Syrup Consumption on Triglycerides and Uric Acid". The Journal of Nutrition. 139 (6): 1242S–1245S. doi:10.3945/jn.108.098194. PMID 19403709.
- ↑ 34.0 34.1 "High uric acid level". Mayo Clinic. 11 September 2010. สืบค้นเมื่อ 24 April 2011.
- ↑ Howard, A. N. (1981). "The historical development, efficacy and safety of very-low-calorie diets". International Journal of Obesity. 5 (3): 195–208. PMID 7024153.
- ↑ "Diuretic-Related Side Effects: Development and Treatment". Medscape. สืบค้นเมื่อ 17 May 2013.
- ↑ Howard, Scott C.; Jones, Deborah P.; Pui, Ching-Hon (2011-05-12). "The Tumor Lysis Syndrome". The New England Journal of Medicine. 364 (19): 1844–1854. doi:10.1056/NEJMra0904569. ISSN 0028-4793. PMC 3437249. PMID 21561350.
- ↑ Heinig, M.; Johnson, R. J. (December 2006). "Role of uric acid in hypertension, renal disease, and metabolic syndrome". Cleveland Clinic Journal of Medicine. 73 (12): 1059–1064. doi:10.3949/ccjm.73.12.1059. PMID 17190309. S2CID 45409308.
- ↑ Richette, P.; Bardin, T. (January 2010). "Gout". Lancet. 375 (9711): 318–328. doi:10.1016/S0140-6736(09)60883-7. PMID 19692116. S2CID 208793280.
- ↑ 40.0 40.1 Choi, H. K.; Atkinson, K.; Karlson, E. W.; Willett, W.; Curhan, G. (March 2004). "Purine-rich foods, dairy and protein intake, and the risk of gout in men". The New England Journal of Medicine. 350 (11): 1093–1103. doi:10.1056/NEJMoa035700. PMID 15014182.
- ↑ "Gout diet: What's allowed, what's not". Mayo Clinic. July 2, 2020.
{{cite web}}: CS1 maint: url-status (ลิงก์) - ↑ Schrauzer, Gerhard N. (2002). "Lithium: Occurrence, Dietary Intakes, Nutritional Essentiality". Journal of the American College of Nutrition. 21 (1): 14–21. doi:10.1080/07315724.2002.10719188. PMID 11838882. S2CID 25752882.
- ↑ "NHS Clinical Knowledge Summaries". UK National Health Service. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 4 March 2012.
- ↑ Pacher, P.; Nivorozhkin, A.; Szabó, C. (2006). "Therapeutic effects of xanthine oxidase inhibitors: Renaissance half a century after the discovery of allopurinol". Pharmacological Reviews. 58 (1): 87–114. doi:10.1124/pr.58.1.6. PMC 2233605. PMID 16507884.
- ↑ 45.0 45.1 45.2 Howard, S. C.; Jones, D. P.; Pui, C.-H. (12 May 2011). "The Tumor Lysis Syndrome". The New England Journal of Medicine. 364 (19): 1844–1854. doi:10.1056/NEJMra0904569. ISSN 0028-4793. PMC 3437249. PMID 21561350.
- ↑ Luo, Y. C.; Do, J. S.; Liu, C. C. (October 2006). "An amperometric uric acid biosensor based on modified Ir–C electrode". Biosensors & Bioelectronics. 22 (4): 482–488. doi:10.1016/j.bios.2006.07.013. PMID 16908130.
- ↑ Nyhan, W. L. (March 2005). "Lesch-Nyhan Disease". Journal of the History of the Neurosciences. 14 (1): 1–10. doi:10.1080/096470490512490. PMID 15804753. S2CID 37934468.
- ↑ Borghi, C.; Verardi, F. M.; Pareo, I.; Bentivenga, C.; Cicero, A. F. (2014). "Hyperuricemia and cardiovascular disease risk". Expert Review of Cardiovascular Therapy. 12 (10): 1219–1225. doi:10.1586/14779072.2014.957675. PMID 25192804. S2CID 42023170.
- ↑ Cappuccio, F. P.; Strazzullo, P.; Farinaro, E.; Trevisan, M. (July 1993). "Uric acid metabolism and tubular sodium handling. Results from a population-based study". Journal of the American Medical Association. 270 (3): 354–359. doi:10.1001/jama.270.3.354. PMID 8315780.
- ↑ Dehghan, A.; van Hoek, M.; Sijbrands E. J., Hofman A.; Witteman, J. C. (February 2008). "High serum uric acid as a novel risk factor for type 2 diabetes". Diabetes Care. 31 (2): 361–362. doi:10.2337/dc07-1276. PMID 17977935.
- ↑ De Oliveira, E. P.; และคณะ (2012). "High plasma uric acid concentration: Causes and consequences". Diabetology & Metabolic Syndrome. 4: 12. doi:10.1186/1758-5996-4-12. PMC 3359272. PMID 22475652.
- ↑ Wang, J. Y.; และคณะ (2012). "Predictive value of serum uric acid levels for the diagnosis of metabolic syndrome in adolescents". The Journal of Pediatrics. 161 (4): 753–6.e2. doi:10.1016/j.jpeds.2012.03.036. PMID 22575243.
- ↑ Banach, K.; Bojarska, E.; Kazimierczuk, Z.; Magnowska, L.; Bzowska, A. (2005). "Kinetic Model of Oxidation Catalyzed by Xanthine Oxidase—The Final Enzyme in Degradation of Purine Nucleosides and Nucleotides". Nucleic Acids. 24 (5–7): 465–469. doi:10.1081/ncn-200060006. PMID 16247972. S2CID 42906456.
- ↑ "What is Gout: What Causes Gout?". MedicalBug. 6 January 2012. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2 April 2019. สืบค้นเมื่อ 6 May 2012.
- ↑ Worcester, E. M.; Coe, F. L. (2008). "Nephrolithiasis". Primary Care: Clinics in Office Practice (ภาษาอังกฤษ). 35 (2): 369–391. doi:10.1016/j.pop.2008.01.005. PMC 2518455. PMID 18486720.
- ↑ Pak, C. Y. (September 2008). "Medical stone management: 35 years of advances". The Journal of Urology. 180 (3): 813–819. doi:10.1016/j.juro.2008.05.048. PMID 18635234.
- ↑ Hess, F. M.; King, J. C.; Margen, S. (1 December 1977). "Effect of low zinc intake and oral contraceptive agents on nitrogen utilization and clinical findings in young women". The Journal of Nutrition. 107 (12): 2219–2227. doi:10.1093/jn/107.12.2219. PMID 925768.
- ↑ Garg, J. P.; Chasan-Taber, S.; Blair, A.; และคณะ (January 2005). "Effects of sevelamer and calcium-based phosphate binders on uric acid concentrations in patients undergoing hemodialysis: a randomized clinical trial". Arthritis and Rheumatism. 52 (1): 290–295. doi:10.1002/art.20781. PMID 15641045.
- ↑ Wang, L.; Hu, W.; Wang, J.; Qian, W.; Xiao, H. (2016). "Low serum uric acid levels in patients with multiple sclerosis and neuromyelitis optica: An updated meta-analysis". Multiple Sclerosis and Related Disorders. 9: 17–22. doi:10.1016/j.msard.2016.05.008. PMID 27645338.
- ↑ Umeki, S.; Ohga, R.; Konishi, Y.; Yasuda, T.; Morimoto, K.; Terao, A. (November 1986). "Oral zinc therapy normalizes serum uric acid level in Wilson's disease patients". The American Journal of the Medical Sciences. 292 (5): 289–292. doi:10.1097/00000441-198611000-00007. PMID 3777013. S2CID 39995735.