ปลายประสาทรับร้อน
ปลายประสาทรับร้อน[1] หรือ ตัวรับอุณหภูมิ (อังกฤษ: thermoreceptor) เป็นปลายประสาทของเซลล์ประสาทรับความรู้สึกในผิวหนังและในเยื่อเมือกบางชนิด ที่ตอบสนองต่อการเปลี่ยนแปลงของอุณหภูมิหรือการแลกเปลี่ยนความร้อนได้ดีที่สุด[2][3][4] คือ ตัวรับอุณหภูมิ ไม่ว่าจะรับเย็นหรืออุ่น จะตอบสนองต่ออุณหภูมิโดยเฉพาะ ๆ หรือต่อการเปลี่ยนแปลงของอุณหภูมิ โดยเป็นฟังก์ชันของการแลกเปลี่ยนความร้อนระหว่างผิวหนังกับวัตถุที่สัมผัส[5] และโดยหลักในพิสัยที่ไม่มีอันตราย เพราะโนซิเซ็ปเตอร์รับอุณหภูมิจะเป็นตัวส่งข้อมูลในพิสัยที่อาจเป็นอันตราย[6]
| ปลายประสาทรับร้อน (thermoreceptor) | |
|---|---|
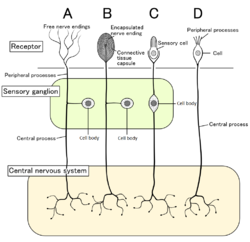 เซลล์ประสาทรับความรู้สึก 4 อย่างพร้อมกับตัวรับความรู้สึกที่คู่กัน ปลายประสาทรับร้อนเป็นปลายประสาทอิสระที่แสดงเป็นแบบ A | |
| ตัวระบุ | |
| MeSH | D013823 |
| อภิธานศัพท์กายวิภาคศาสตร์ | |
ในช่วงอุณหภูมิ 31-36°C (32-34°C[6]) ถ้าอุณหภูมิที่ผิวหนังเปลี่ยนอย่างช้า ๆ เราจะไม่รู้สึกอะไร ถ้าต่ำกว่าช่วงนี้ เราจะรู้สึกเย็นไปจนถึงหนาวและเริ่ิมที่ 10-15°C จะรู้สึกหนาวเหน็บ (เจ็บ) และถ้าสูงกว่าช่วงนี้ เราจะรู้สึกอุ่นไปจนถึงร้อนและเริ่มที่ 45°C จะรู้สึกร้อนลวก (เจ็บ)[7] ความรู้สึกอุ่นเย็นที่ไม่เจ็บมาจากตัวรับอุณหภูมิ ส่วนความรู้สึกเจ็บแบบหนาวเหน็บ/ร้อนลวกมาจากโนซิเซ็ปเตอร์ที่รับอุณหภูมิ (thermal nociceptor)[6]
ตัวรับอุณหภูมิที่ผิวหนังเชื่อว่าเป็นใยประสาทใน 3 กลุ่ม ทั้งหมดเป็นแบบปรับตัวช้า ๆ (slowly adapting) คือ ตัวรับเย็นสองชนิดที่มีใยประสาทในกลุ่ม A delta และกลุ่ม C และตัวรับอุ่นหนึ่งชนิดที่มีใยประสาทในกลุ่ม C[6]
ความอุ่นขึ้นเป็นสิ่งเร้าที่พอกระตุ้นตัวรับอุ่น ซึ่งจะเพิ่มอัตราการยิงศักยะงานของนิวรอน และความอุ่นที่ลดลงก็จะลดอัตราการยิงศักยะงาน สำหรับตัวรับเย็น อัตราการยิงศักยะงานจะสูงขึ้นเมื่ออุณหภูมิลดลง และจะต่ำลงเมื่ออุณหภูมิสูงขึ้น บางครั้งตัวรับเย็นปรากฏว่าตอบสนองต่อความร้อน (เช่นที่ 46°C) และตัวรับร้อนตอบสนองต่อความเย็น (เช่นที่ 16°C) ซึ่งเป็นการตอบสนองแบบขัดแย้ง (paradoxical response)[8] แต่กลไกที่ทำให้มีการตอบสนองเยี่ยงนี้ก็ยังระบุไม่ได้
ในมนุษย์ ความรู้สึกอุ่นเย็นจะส่งไปสู่คอร์เทกซ์รับความรู้สึกทางกาย (postcentral gyrus) ผ่านวิถีประสาทสองระบบ คือ[9]
- จากร่างกายทั้งหมดรวมทั้งศีรษะครึ่งหลัง จะส่งผ่านไขสันหลังในระบบ anterolateral system/spinothalamic tract
- จากศีรษะด้านหน้ารวมทั้งใบหน้า จะส่งผ่านก้านสมองในระบบ Trigeminothalamic tract
ตัวรับอุณหภูมิแบบพิเศษยังพบในงูบางชนิด เช่น งูในวงศ์งูแมวเซา (Viperidae) มีอวัยวะเหนือปากที่เรียกว่า pit organs ซึ่งมีตัวรับอุณหภูมิที่ไวความร้อนซึ่งเกิดจากการแผ่รังสีอินฟราเรด ซึ่งเมื่อบวกกับการเห็น ช่วยให้งูสามารถรับรู้สิ่งแวดล้อมและเหตุการณ์ที่กำลังเกิดขึ้นรอบ ๆ ตัวตลอด 24 ชม. ช่วยหาเหยื่อที่เป็นสัตว์เลือดอุ่น และช่วยหาที่อุ่น ๆ เพื่อพักและทำรัง[10]
โครงสร้าง
แก้ตัวรับอุณหภูมิได้พรรณนามาโดยดั้งเดิมว่า เป็นปลายประสาทอิสระที่ไม่มีอะไรพิเศษ แต่กลไกการทำงานตอบสนองต่อการเปลี่ยนแปลงของอุณหภูมิก็ยังไม่ชัดเจนทั้งหมด
ใยประสาทรับอุณหภูมิ 3 อย่าง
แก้ตัวรับอุณหภูมิที่ผิวหนังเชื่อว่าเป็นใยประสาทใน 3 กลุ่ม ทั้งหมดเป็นแบบปรับตัวช้า ๆ (slowly adapting) มีลานรับสัญญาณแบบเป็นจุด โดยตัวรับเย็นมีทั้งตัวเซลล์ทั้งใยประสาทมากกว่าตัวรับอุ่น คือ[6][11][12]
- ตัวรับเย็น เป็นใยประสาทกลุ่ม A delta และกลุ่ม C ทั้งสองชนิดตอบสนองต่อสารเคมีบางชนิด เช่น เมนทอล ที่ทำให้รู้สึกเย็น
- กลุ่ม A delta - พบในหนังกำพร้า มีปลอกไมอีลินบาง ๆ (เส้นผ่าศูนย์กลาง 1-6 ไมโครเมตร) จึงสื่อประสาทได้เร็วกว่า (4-36 เมตรต่อวินาที) มีขีดเริ่มเปลี่ยนต่ำและไวต่อการเปลี่ยนลดอุณหภูมิอย่างฉับพลันมากกว่าค่อย ๆ เปลี่ยนถึง 100 เท่า ทำให้สามารถรู้สึกลมพัดจากหน้าต่างที่ไกล ๆ มีการแสดงออกของช่องไอออน TRPM8
- กลุ่ม B - พบในหนังกำพร้า ไร้ปลอกไมอีลิน (เส้นผ่าศูนย์กลาง 0.2-1.5 ไมโครเมตร) จึงสื่อประสาทได้ช้ากว่า (0.4-2 เมตร/วินาที) มีขีดเริ่มเปลี่ยนสูงแต่สามารถส่งสัญญาณการเปลี่ยนอุณหภูมิแบบฉับพลันแม้ต่ำกว่า 0°C มีการแสดงออกของช่องไอออน TRPM8 และ TRPA1
- ตัวรับอุ่น ตอบสนองต่อสารเคมีบางชนิด เช่น การบูร
- กลุ่ม C - พบในหนังแท้ด้านบน (ลึกกว่าตัวรับเย็น) ไร้ปลอกไมอีลิน จึงสื่อประสาทได้ช้า ไวต่อการเปลี่ยนอุณหภูมิน้อยกว่าตัวรับเย็น การเปลี่ยนแปลงอุณหภูมิสำหรับคนไวสุดต้องอย่างน้อย 0.1°C ใยประสาทจะตอบสนองตามความอุ่นอย่างเพิ่มขึ้นเรื่อย ๆ จนถึงจุดร้อนลวก แล้วก็จะตอบสนองแบบอิ่มตัวโดยไม่เพิ่มขึ้นอีก มีการแสดงออกของช่องไอออน TRPV3
หน้าที่ ตำแหน่ง และการกระจายตัว
แก้ในสัตว์เลี้ยงลูกด้วยนม ตัวรับอุณหภูมิจะอยู่ในเนื้อเยื่อต่าง ๆ รวมทั้งผิวหนัง (cutaneous receptor) กระจกตา และกระเพาะปัสสาวะ ตัวรับอุณหภูมิทั้งแบบอุ่นแบบเย็น มีบทบาทในการรับรู้อุณหภูมิของสิ่งแวดล้อมที่ไม่มีอันตราย อุณหภูมิในระดับที่เป็นอันตรายต่อสิ่งมีชีวิต จะตรวจจับด้วยโนซิเซ็ปเตอร์แบบต่าง ๆ ที่อาจตอบสนองต่อความเย็นอันตราย ความร้อนอันตราย หรือสิ่งเร้าที่เป็นอันตรายหลายรูปแบบ (คือโนซิเซ็ปเตอร์หนึ่งอาจตอบสนองต่อสิ่งเร้าหลายรูปแบบ เพราะเป็น polymodal)
ปลายประสาทที่มักตอบสนองต่อความเย็นอยู่ที่ผิวหนังอย่างหนาแน่นระดับกลาง ๆ แต่มีอย่างหนาแน่นที่กระจกตา ลิ้น กระเพาะปัสสาวะ และผิวหนังใบหน้า คาดว่า ตัวรับความเย็นที่ลิ้นจะส่งข้อมูลที่ควบคุมการรับรสชาติ คือ อาหารบางอย่างจะอร่อยเมื่อเย็น บางอย่างก็ไม่อร่อย
ตัวรับอุณหภูมิที่ไวความเย็น จะทำให้รู้สึกเย็น หนาว และสดชื่น ส่วนที่กระจกตา ตัวรับอุณหภูมิเชื่อว่า ตอบสนองต่อความเย็นจากการระเหยของน้ำตาด้วยอัตราการยิงศักยะงานที่ถี่ขึ้น แล้วทำให้เกิดรีเฟล็กซ์กะพริบตา
ตัวรับอุณหภูมิที่มือช่วยให้รู้สึกความร้อนเย็นของวัตถุที่สัมผัส และตัวรับอุณหภูมิที่ผิวหนังที่มีขน มีบทบาทในกระบวนการปรับอุณหภูมิกาย[13] คือ
- ปลายประสาทที่ผิวหนังจะส่งข้อมูลความเย็นร้อนไปยังสมอง ซึ่งส่งสัญญาณให้เส้นเลือดตีบเพื่อลดการถ่ายเทความร้อนของร่างกายถ้าหนาว หรือให้เส้นเลือดขยายเพื่อเพิ่มการถ่ายเทความร้อนถ้าร้อน ถ้านี่ยังไม่ทำให้เป็นปกติ สมองก็จะส่งสัญญาณให้เหงื่อออก[14] ให้ขนลุก (ซึ่งไม่ช่วยอะไรในมนุษย์) ให้ตัวสั่น ให้เพิ่มเมแทบอลิซึมในฤดูหนาว และสนับสนุนให้เกิดพฤติกรรมที่ปรับความร้อนเย็น เช่น ใส่เสื้อผ้ามากขึ้น หลบออกจากแดดเป็นต้น[15]
- บริเวณ preoptic ของไฮโปทาลามัสในสมองที่อยู่ก่อนส่วนไขว้ประสาทตา (optic chiasm) ทำหน้าที่เป็นตัวรับอุณหภูมิจากเลือด โดยได้รับสัญญาณจากตัวรับอุณหภูมิที่ผิวหนังด้วย แล้วส่งสัญญาณไปในบริเวณสมองอื่นที่ลดหรือเพิ่มการเสียความร้อนของร่างกายดังกล่าวในข้อแรก โดยเป็นกระบวนการป้อนกลับแบบลบ[15]
ที่กระเพาะปัสสาวะ
แก้ในกระเพาะปัสสาวะ ช่องไอออนที่อำนวยการรับรู้อุณหภูมิพบอยู่ในที่ต่าง ๆ รวมทั้ง[16] (ดูรายละเอียดเกี่ยวกับช่องไอออนในหัวข้อ "ช่องไอออนกลุ่ม TRP")
- TRPV1 - มีตลอดวิถีประสาทนำเข้ารวมทั้ง Urothelial cells ซึ่งบุ Urinary tract, ปลายส่วนนอก (peripheral terminal) ของใยประสาทนำเข้าที่อยู่ใกล้ ๆ กับ Urothelial cell, ตัวนิวรอนในปมประสาทรากหลัง (dorsal root ganglion) ที่มีใยประสาทขนาดเล็กจนถึงกลาง, ปลายส่วนกลาง (central terminal) ของใยประสาทนำเข้า, และในปีกหลังของไขสันหลัง (dorsal horn) ชั้นแรก ๆ
- TRPV1 ในใยประสาทกลุ่ม C ที่ตรวจจับการพองของกระเพาะ (เป็นตัวรับแรงกลแบบยืดหด) หรือสารเคมีที่ระคายเคือง
- TRPV2, TRPV4, TRPM8, และ TRPA1 ใน Urothelial cells
แต่ว่า ช่องไอออนเหล่านี้อาจมีบทบาทอื่น ๆ นอกจากการรับรู้อุณหภูมิรวมทั้ง[16]
- TRPV1 มีบทบาทสำคัญเกี่ยวกับโนซิเซ็ปชันและการทำงานเป็นปกติของกระเพาะปัสสาวะ
- TRPV1 ใน Urothelial cells สัมพันธ์กับระดับแคลเซียมในเซลล์ที่สูงขึ้นและการปล่อยสารสื่อประสาทต่าง ๆ
- ในนิวรอน TRPV1 เชื่อว่ามีหน้าที่รวบรวมหรือเพิ่มการตอบสนองต่อสิ่งเร้าต่าง ๆ และมีบทบาทสำคัญในภาวะรู้สึกเจ็บมากกว่าปรกติที่เกิดจากการอักเสบ
- แม้ว่าการแสดงออกของช่อง TRPV2, TRPV4, TRPM8, และ TRPA1 จะแสดงนัยว่า Urothelial cells มีการรับรู้อุณหภูมิ แต่ว่า บทบาทหลักความจริงอาจเป็นเพื่อตรวจจับสิ่งเร้าอันตราย (noxious stimuli)
- นอกจากนั้น TRPM8 อาจมีบทบาทเกี่ยวกับการเพิ่มจำนวนเซลล์อีกด้วย
กลไกการถ่ายโอนสัญญาณประสาท
แก้งานวิจัยเรื่องนี้ได้รับความสนใจมากขึ้นเมื่อมีการระบุและการโคลนหมู่โปรตีน Transient Receptor Potential (TRP) เพราะช่อง TRPM8 เป็นตัวอำนวยการถ่ายโอนอุณหภูมิให้เป็นสัญญาณประสาทในตัวรับอุณหภูมิแบบเย็น ช่องไอออนนี้อนุญาตแคตไอออนแบบผสมให้ผ่านเข้าไปในเซลล์ประสาทได้ (โดยหลักเป็นไอออน Na+ แม้ Ca2+ ก็จะเข้าได้ด้วย) ในระดับมากน้อยโดยเป็นสัดส่วนผกผันกับอุณหภูมิ
ช่องนี้ไวต่ออุณหภูมิระหว่าง 8-28°C แต่ก็อาจทำงานเนื่องจากการยึดกับลิแกนด์นอกเซลล์ เช่น เมนทอล/การบูรอาจเริ่มการทำงานของช่อง TRPM8 แต่เนื่องจากโปรตีน TRPM8 มีการแสดงออกในนิวรอนที่ส่งสัญญาณความเย็น การบูรบนผิวหนังจึงทำให้รู้สึกเย็น ความรู้สึกสดชื่นยังสัมพันธ์กับการทำงานของตัวรับความเย็นเนื่องจากการบูร โดยเฉพาะที่ใบหน้าซึ่งมีแอกซอนของเส้นประสาทไทรเจมินัล (V) นี่เป็นเหตุของการใส่เมนทอล/การบูรในเครื่องอาบน้ำต่าง ๆ รวมทั้งยาสีฟัน โลชั่นโกนหนวด ครีมทาหน้า เป็นต้น
องค์ประกอบอีกอย่างของการถ่ายโอนความเย็น ก็คือ ช่องรั่ว (leak channel) ซึ่งปล่อยให้กระแสไฟคือประจุไอออนโพแทสเซียมไหลออกโดยขึ้นอยู่กับอุณหภูมิ ช่องรั่วบางส่วนเป็นอนุพันธุ์ของ "Tandem pore domain potassium channel" และในบรรดาช่องเหล่านี้ บางชนิดจะปิดทันทีเมื่ออุณหภูมิลดลงน้อยกว่า 28°C (เช่น TRAAK, TREK) อนึ่ง อุณหภูมิยังควบคุมการทำงานของ Na+/K+-ATPase ด้วย ซึ่งเป็นปั๊มแบบ P-type ที่ปั๊มไอออน 3Na+ ออกจากเซลล์แลกเปลี่ยนกับไอออน 2K+ โดยได้พลังงานจากการแยก ATP ที่อาศัยน้ำ ผลก็คือการไหลของประจุบวกออกจากเซลล์โดยสุทธิ คือ เป็นกระแสไฟฟ้าแบบเพิ่มขั้ว (hyperpolarizing) ซึ่งทำให้เซลล์กระตุ้นได้ยากขึ้น โดยระดับกระแสไฟจะขึ้นอยู่กับอัตราการปั๊ม
มีนักวิชาการที่เสนอว่า นิวรอนต้องอาศัยโปรตีนไวอุณหภูมิต่าง ๆ รวมกันเพื่อสร้างตัวรับอุณหภูมิ[17] คุณสมบัติแบบอุบัติ (emergence) ของนิวรอนเช่นนี้เชื่อว่าประกอบด้วยการแสดงออกของโปรตีนดังที่กล่าวแล้ว พร้อมกับช่องไวความต่างศักย์ (voltage-sensitive channel) ต่าง ๆ รวมทั้งช่อง HCN (hyperpolarization-activated cyclic nucleotide-gated), และช่อง IKA (rapidly activating and inactivating transient potassium channel)
ช่องไอออนกลุ่ม TRP
แก้งานวิจัยปี 2544[7] พบว่าความร้อนเย็นจะกระตุ้นช่องไอออนกลุ่ม TRP (Transient potential receptor) ซึ่งให้แคตไอออนซึมผ่านได้อย่างไม่เลือก (รวมทั้งแคลเซียมและแมกนีเซียม[18]) และมีโครงสร้างคล้ายกับช่องที่เปิดปิดด้วยศักย์ไฟฟ้า (voltage-gated channel) โดยช่อง TRP แต่ละอย่างจะไวความเย็นร้อนต่าง ๆ กัน คือ เมื่อถึงขีดเริ่มเปลี่ยนทางอุณหภูมิ ช่องก็จะเปิดให้แคตไอออนไหลผ่านเข้ามากขึ้น[7]
| ช่องไอออน | อุณหภูมิ (°C) | สาร/เคมี | หมายเหตุ |
|---|---|---|---|
| TRPA1 | <17 | กระเทียม (allicin), ผักกาด (allyl isothiocyanate), icilin[20],
ขิง (gingerol), cinnamic aldehyde, เมทิลซาลิไซเลต, ยูเจนอล (น้ำมันกานพลู)[21] |
พบในตัวรับเย็นที่มีขีดเริ่มเปลี่ยนสูง |
| TRPM8 | 8-28 | เมนทอล, พืชวงศ์กะเพรา (กะเพรา โหระพา แมงลักเป็นต้น), icilin[20] | พบในตัวรับเย็นทั้งมีขีดเริ่มเปลี่ยนสูงและต่ำ |
| TRPV4 | >27 | กรด[21] | รับรู้สัมผัส/แรงกล |
| TRPV3 | >31/39[A] | การบูร, ยูเจนอล, carvacrol, thymol[21] | พบในตัวรับอุ่น |
| TRPV1 | >43 | แคปไซซิน (จากพริก), กรด, Anandamide[23], | พบในโนซิเซ็ปเตอร์รับร้อนทั้งแบบ Aδ และ C[24] |
| TRPV2 | >52 | - | พบในโนซิเซ็ปเตอร์รับร้อนแบบ Aδ[24] ทำให้รู้สึกร้อนลวก |
ช่อง TRPM8 และ TRPA1 ที่เปิดเมื่อเย็นลงและปิดเมื่ออุ่นขึ้น ทั้งสองมีการแสดงออกที่ปลายประสาทรับเย็นที่มีขีดเริ่มเปลี่ยนสูง แต่ปลายประสาทรับเย็นที่มีขีดเริ่มเปลี่ยนต่ำจะมีเพียงแค่ช่อง TRPM8 เท่านั้น ส่วนปลายประสาทรับอุ่นมีช่อง TRPV3[7]
วิถีประสาท
แก้- ดูเทียบกับ "วิถีประสาทของระบบรับความรู้สึกทางกาย"
ในมนุษย์ ความรู้สึกร้อนเย็น (รวมทั้งแบบหนาวเหน็บร้อนลวก) จะส่งไปสู่ทาลามัสแล้วสู่เปลือกสมองส่วนต่าง ๆ ผ่านวิถีประสาทสองระบบ คือ[9][6]
- Trigeminothalamic tract ส่งข้อมูลต่าง ๆ รวมทั้งอุณหภูมิที่มาจากศีรษะส่วนหน้ารวมทั้งใบหน้า ผ่านก้านสมองไปยังทาลามัส แล้วต่อไปยังส่วนต่าง ๆ ของเปลือกสมอง โดย first order neuron อยู่ที่ปมประสาทของเส้นประสาทสมอง (รวมทั้ง trigeminal [V], facial [VII], glossopharyngeal [IX], และ vagus [X]) ซึ่งส่งแอกซอนลงไปยัง second order neuron ใน medulla ซีกร่างกายเดียวกันที่ spinal trigeminal nucleus ซึงก็จะส่งแอกซอนข้ามไขว้ทแยง medulla ไปสุดที่ทาลามัสส่วน ventral posterior medial nucleus (VPM)[25]
- anterolateral system/spinothalamic tract ส่งข้อมูลต่าง ๆ รวมทั้งอุณหภูมิจากร่างกายรวมศีรษะครึ่งหลัง ผ่านไขสันหลังไปยังทาลามัส แล้วต่อไปยังส่วนต่าง ๆ ของเปลือกสมอง โดย first order neuron อยู่ที่ปมประสาทรากหลัง (dorsal root ganglion) ซึ่งส่งแอกซอนขึ้น/ลงผ่าน Lissauer's tract 1-2 ข้อไขสันหลังไปยัง second order neuron ในปีกหลังของไขสันหลัง (dorsal horn) ในซีกร่างกายเดียวกันแต่อยู่ต่างระดับไขสันหลังกัน second order neuron ก็จะส่งแอกซอนข้ามไขว้ทแยงที่ไขสันหลังแล้วขึ้นไปตาม anterolateral column/spinothalamic tract ไปยังทาลามัสส่วน ventral posteriorlateral nucleus (VPL)[26]
ให้สังเกตว่า เนื่องจากว่า เป้าหมายในทาลามัสของความรู้สึกร้อนเย็นมาจากการอนุมานที่เนื่องกับวิถีประสาทของความเจ็บปวด จึงยังไม่มติร่วมกันว่า ส่วนไหนของทาลามัสเป็นเป้าหมายของความรู้สึกร้อนเย็นกันแน่[27] นอกจากที่ส่วน VPM[6][25]และ VPL[6][26] ตามที่ว่าแล้ว ยังมีนักวิชาการที่กำหนดเขตต่อไปนี้ คือ
- ใยประสาทจาก lamina I (รวมทั้งจากตัวรับอุณหภูมิทั้งสามอย่าง) ของ dorsal horn ไปสุดที่ส่วนหลังของ VPN และส่วนหลังของ ventral medial nucleus ที่อยู่ติดกัน[27]
- ใยประสาทจาก lamina I (รวมทั้งจากตัวรับอุณหภูมิทั้งสามอย่าง) ของ dorsal horn ไปสุดที่ VMpo (ventromedial posterior nucleus) ที่อยู่ทาง medial ของ VPL[6]
งานศึกษาโดยใช้ fMRI พบว่า เปลือกสมองส่วนต่าง ๆ จะทำงานเมื่อมนุษย์ได้ตัวกระตุ้นร้อนเย็น รวมทั้ง superior parietal lobule, insular cortex, และ orbitofrontal cortex[12]
ดูเพิ่ม
แก้เชิงอรรถ
แก้เชิงอรรถและอ้างอิง
แก้- ↑ "thermoreceptor", ศัพท์บัญญัติอังกฤษ-ไทย, ไทย-อังกฤษ ฉบับราชบัณฑิตยสถาน (คอมพิวเตอร์) รุ่น ๑.๑ ฉบับ ๒๕๔๕,
(แพทยศาสตร์) ปลายประสาทรับร้อน
- ↑ Purves et al 2008, Glossary, หน้า G-15 "thermoreceptors - Receptors specialized to transduce changes in temperature."
- ↑ Saladin 2010, pp. 1197 "thermoreceptor - A neuron specialized to respond to heat or cold, found in the skin and mucous membranes, for example."
- ↑ Rice & Albrecht 2008, Glossary, pp. 3 "thermoreceptor - A sensory ending that that responds optimally to heat exchange"
- ↑ Rice & Albrecht 2008, 6.01.1.3.1. (ii) Stimulus modality, pp. 5
- ↑ 6.0 6.1 6.2 6.3 6.4 6.5 6.6 6.7 6.8 Willis 2008, 6.06.2.2 Thermoreceptive Circuits, pp. 94-95
ในเรื่องการเชื่อมต่อของ lamina I STT กับ VMpo ที่อยู่ทาง medial ของ VPL อ้าง
- Craig, AD; Bushnell, MC; Zhang, ET; Blomqvist, A (1994). "A thalamic nucleus specific for pain and temperature sensation". Nature. 372: 770–773.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - Blomqvist, A; Zhang, ET; Craig, AD (2000). "Cytoarchitecture and immunohistochemical characterization of a specific pain and temperature relay, the posterior portion of the ventral medial nucleus, in the human thalamus". Brain. 123: 601–619.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - Craig, AD (2004). "Distribution of trigeminothalamic and spinothalamic lamina I terminations in the macaque monkey". J. Comp. Neurol. 477: 119–148.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)
- Craig, AD; Bushnell, MC; Zhang, ET; Blomqvist, A (1994). "A thalamic nucleus specific for pain and temperature sensation". Nature. 372: 770–773.
- ↑ 7.0 7.1 7.2 7.3 Gardner & Johnson 2013a, p. 486 อ้างอิง
- Julius, D; Basbaum, AI (2001). "Molecular mechanisms of noiception". Nature. 413: 203–210.
- ↑ Krantz 2012, Receptors, pp. 12.2-12.4 อ้างอิง
- Somino, R; Dubner, R (1981). "Response characteristics of specific thermoreceptive afferents innervating monkey facial skin and their relationship to human thermal sensitivity". Brain Research Reviews. 3 (2): 105–122.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)
- Somino, R; Dubner, R (1981). "Response characteristics of specific thermoreceptive afferents innervating monkey facial skin and their relationship to human thermal sensitivity". Brain Research Reviews. 3 (2): 105–122.
- ↑ 9.0 9.1 Gardner & Johnson 2013a, p. 488-495
- ↑ Johnson 2008, 6.16.2.4 Heat-Sensory Pit Organs of Snakes, p. 334-335
- ↑ Gardner & Johnson 2013a, p. 477, 486-487
- ↑ 12.0 12.1 Johnson 2008, 6.16.2 Thermal Sensory Systems, p. 332-335
- ↑ Goodwin & Wheat 2008, 6.03.1 Introduction, p. 39
- ↑ Saladin 2010, Chapter 6 - The Integumentary System, pp. 189 (205)
- ↑ 15.0 15.1 Saladin 2010, Chapter 26 - Nutrition and Metabolism, pp. 1040 (1056)
- ↑ 16.0 16.1 Birder 2008, 5.40.1.1 Sensor Molecules Expressed in Urothelium Which Could Contribute to Bladder Pain, pp. 585-587 อ้างอิง
- เกี่ยวกับบทบาทของ TRPV1 ในโนซิเซ็ปชันและการทำงานเป็นปกติของกระเพาะปัสสาวะ
- Szallasi, A (2001). "Vanilloid receptor ligands: hopes and realities for the future". Drugs Aging. 18: 561–573.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)
- Szallasi, A (2001). "Vanilloid receptor ligands: hopes and realities for the future". Drugs Aging. 18: 561–573.
- เกี่ยวกับ TRPV1 ที่ Urothelial cells
- Birder, L; Kanai, AJ; de Groat, WC; Kiss, S; Nealen, ML; Burke, NE; Dineley, KE; Watkins, S; Reynolds, IJ; Caterina, MJ (2001). "Vanilloid receptor expression suggests a sensory role for urinary bladder epithelial cells". Proc. Natl. Acad. Sci. U. S. A. 98: 13396–13401.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - Birder, L; Nakamura, Y; Kiss, S; Nealen, ML; Barrick, SR; Kanai, AJ; Wang, E; Ruiz, WG; de Groat, WC; Apodaca, G; Watkins, S; Caterina, MJ (2002a). "Altered urinary bladder function in mice lacking the vanilloid receptor TRPV1". Nat. Neurosci. 5: 856–860.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)
- Birder, L; Kanai, AJ; de Groat, WC; Kiss, S; Nealen, ML; Burke, NE; Dineley, KE; Watkins, S; Reynolds, IJ; Caterina, MJ (2001). "Vanilloid receptor expression suggests a sensory role for urinary bladder epithelial cells". Proc. Natl. Acad. Sci. U. S. A. 98: 13396–13401.
- เกี่ยวกับบทบาทของ TRPV1 ในนิวรอน
- Ghuang, HH; Prescott, ED; Kong, H; Shields, S; Jordt, SE; Basbaum, AI; Chao, MV; Julius, D (2001). "Bradykinin and nerve growth factor release the capsaicin receptor from PtdIns (4,5)P 2-mediated inhibition". Nature. 411: 957–962.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - Holzer, P (2004). "TRPV1 and the gut: from a tasty receptor for a painful vanilloid to a key player in hyperalgesia". Eur. J. Pharmacol. 500: 231–241.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)
- Ghuang, HH; Prescott, ED; Kong, H; Shields, S; Jordt, SE; Basbaum, AI; Chao, MV; Julius, D (2001). "Bradykinin and nerve growth factor release the capsaicin receptor from PtdIns (4,5)P 2-mediated inhibition". Nature. 411: 957–962.
- เกี่ยวกับบทบาทของ TRPV1 ในโนซิเซ็ปชันและการทำงานเป็นปกติของกระเพาะปัสสาวะ
- ↑ Viana F, de la Peña E, Belmonte C (2002). "Specificity of cold thermotransduction is determined by differential ionic channel expression". Nature Neuroscience. 5 (3): 254–260. doi:10.1038/nn809. PMID 11836533. S2CID 21291629.
- ↑ Johnson 2008, 6.16.2.1 Receptor Structure and Function, p. 333
- ↑ Gardner & Johnson 2013a, Thermo Receptors Detect Changes in Skin Temperature, pp. 485-486; Figure 22-8, pp. 487
- ↑ 20.0 20.1 20.2 Lackie, JM (2007). The Dictionary of Cell and Molecular Biology (4th ed.). Elsevier. TRP Channels, p. 433. ISBN 978-0-12-373986-5.
Capsaicin and resiniferatoxin are agonists for TRPV1, menthol for TRPM8 (cold receptor), and icilin for both TRPM8 and TRPA1.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 21.0 21.1 21.2 21.3 Simons & Carstens 2008, Table 1 Thermo- and chemosensitive transient receptor potentials (TRPs), p. 350
- ↑ Beisel et al 2008, 3.05.2.1.1 The transient receptor potential superfamily, p. 86
- ↑ Purves et al 2008b, Box 10A - Capsaisin, pp. 234
- ↑ 24.0 24.1 Purves et al 2008b, Transduction of Nociceptive Signals, pp. 233
- ↑ 25.0 25.1 Purves et al 2008b, pp. 241–242
- ↑ 26.0 26.1 Purves et al 2008b, p. 233-238, 242
- ↑ 27.0 27.1 Gardner & Johnson 2013a, p. 494-495
แหล่งอ้างอิงอื่น ๆ
แก้- Krantz, John H. (2012). "12 Skin Senses". Experiencing Sensation and Perception (PDF). Pearson Education. (pre-printed files)
- Saladin, KS (2010). Anatomy and Physiology: The Unity of Form and Function (5th ed.). New York: McGraw-Hill. ISBN 978-0-39-099995-5.
- Neuroscience (2008)
- Purves, Dale; Augustine, George J; Fitzpatrick, David; Hall, William C; Lamantia, Anthony Samuel; McNamara, James O; White, Leonard E, บ.ก. (2008b). "10 - Pain". Neuroscience (4th ed.). Sinauer Associates. pp. 231–251. ISBN 978-0-87893-697-7.
- Purves, Dale; Augustine, George J; Fitzpatrick, David; Hall, William C; Lamantia, Anthony Samuel; McNamara, James O; White, Leonard E, บ.ก. (2008). Neuroscience (4th ed.). Sinauer Associates. ISBN 978-0-87893-697-7.
- Principles of Neural Science (2013)
- Gardner, Esther P; Johnson, Kenneth O (2013a). "22 - The Somatosensory System: Receptors and Central Pathway". ใน Kandel, Eric R; Schwartz, James H; Jessell, Thomas M; Siegelbaum, Steven A; Hudspeth, AJ (บ.ก.). Principles of Neural Science (5th ed.). United State of America: McGraw-Hill. pp. 475–497. ISBN 978-0-07-139011-8.
- Purves, Dale; Augustine, George J; Fitzpatrick, David; Hall, William C; Lamantia, Anthony Samuel; McNamara, James O; White, Leonard E, บ.ก. (2008a). "9 - The Somatic Sensory System: Touch and Proprioception". Neuroscience (4th ed.). Sinauer Associates. pp. 207–229. ISBN 978-0-87893-697-7.
- The Senses: A Comprehensive Reference (2008)
- Beisel, KW; He, D; Hallworth, R; Fritzsch, B (2008). Dallos, Peter; Oertel, Donata (บ.ก.). 3.05 Genetics of Mechanoreceptor Evolution and Development. The Senses: A Comprehensive Reference. Vol. 3: Audition. Elsevier.
- Simons, CT; Carstens, E (2008). Firestein, Stuart; Beauchamp, Gary K (บ.ก.). 4.18 Oral Chemesthesis and Taste. The Senses: A Comprehensive Reference. Vol. 4: Olfaction & Taste. Elsevier.
- Birder, LA (2008). Bushnell, M Catherine; Basbaum, Allan I (บ.ก.). 5.40 Urothelium as a Pain Organ. The Senses: A Comprehensive Reference. Vol. 5: Pain. Elsevier.
- Rice, FL; Albrecht, PJ (2008). Kaas, JH; Gardner, EP (บ.ก.). 6.01 Cutaneous Mechanisms of Tactile Perception: Morphological and Chemical Organization of the Innervation to the Skin. The Senses: A Comprehensive Reference. Vol. 6: Somatosensation. Elsevier.
- Goodwin, AW; Wheat, HE (2008). Kaas, JH; Gardner, EP (บ.ก.). 6.03 Physiological Responses of Sensory Afferents in Glabrous and Hairy Skin of Humans and Monkeys. The Senses: A Comprehensive Reference. Vol. 6: Somatosensation. Elsevier.
- Willis, WD (Jr) (2008). Kaas, JH; Gardner, EP (บ.ก.). 6.06 Physiological Characteristics of Second-Order Somatosensory Circuits in Spinal Cord and Brainstem. The Senses: A Comprehensive Reference. Vol. 6: Somatosensation. Elsevier.
- Johnson, JI (2008). Kaas, JH; Gardner, EP (บ.ก.). 6.16 Specialized Somatosensory Systems. The Senses: A Comprehensive Reference. Vol. 6: Somatosensation. Elsevier.