เมทีนามีน
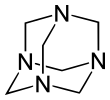
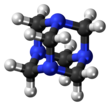
เมทีนามีน หรือ เฮกซะเมทิลีนเตตรามีน (อังกฤษ: Methenamine หรือ Hexamethylenetetramine) เป็นสารประกอบอินทรีย์เฮเทอโรไซคลิก มีสูตรโครงสร้างคือ (CH2)6N4 ลักษณะเป็นผลึกสีขาว ละลายได้ดีในน้ำและตัวทำละลายอินทรีย์ที่มีขั้ว โครงสร้างโมเลกุลมีลักษณะคล้ายกรงเหมือนกับอะดาแมนแทน เมทีนามีนถูกนำมาใช้ประโยชน์ในการสังเคราะห์สารประกอบเคมีอื่น เช่น พลาสติก ยา สารเติมแต่งยาง สารนี้มีจุดระเหิด ณ สภาวะสุญญากาศที่ 280 องศาเซลเซียส[2]
| |||
| ชื่อ | |||
|---|---|---|---|
| Preferred IUPAC name
1,3,5,7-Tetraazaadamantane | |||
| ชื่ออื่น
Hexamine; Methenamine;
Urotropine; Formin, Aminoform | |||
| เลขทะเบียน | |||
3D model (JSmol)
|
|||
| 2018 | |||
| ChEBI | |||
| ChEMBL | |||
| เคมสไปเดอร์ | |||
| ดรักแบงก์ | |||
| ECHA InfoCard | 100.002.642 | ||
| EC Number |
| ||
| เลขอี | E239 (preservatives) | ||
| 26964 | |||
| KEGG | |||
| MeSH | Methenamine | ||
ผับเคม CID
|
|||
| RTECS number |
| ||
| UNII | |||
| UN number | 1328 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| คุณสมบัติ | |||
| C6H12N4 | |||
| มวลโมเลกุล | 140.186 g/mol | ||
| ลักษณะทางกายภาพ | ผลึกของแข็งสีขาว | ||
| กลิ่น | คาว คล้ายแอมโมเนีย | ||
| ความหนาแน่น | 1.33 g/cm3 (ที่ 20 °C) | ||
| จุดหลอมเหลว | 280 องศาเซลเซียส (536 องศาฟาเรนไฮต์; 553 เคลวิน) (sublimes) | ||
| 85.3 g/100 mL | |||
| ความสามารถละลายได้ | ละลายน้ำได้ในคลอโรฟอร์ม, เมทานอล, เอทานอล, แอซีโทน, เบนซีน, ไซลีน, อีเทอร์ | ||
| ความสามารถละลายได้ ใน คลอโรฟอร์ม | 13.4 g/100 g (20 °C) | ||
| ความสามารถละลายได้ ใน เมทานอล | 7.25 g/100 g (20 °C) | ||
| ความสามารถละลายได้ ใน เอทานอล | 2.89 g/100 g (20 °C) | ||
| ความสามารถละลายได้ ใน แอซีโทน | 0.65 g/100 g (20 °C) | ||
| ความสามารถละลายได้ ใน เบนซีน | 0.23 g/100 g (20 °C) | ||
| pKa | 4.89[1] | ||
| เภสัชวิทยา | |||
| J01XX05 (WHO) | |||
| ความอันตราย | |||
| อาชีวอนามัยและความปลอดภัย (OHS/OSH): | |||
อันตรายหลัก
|
ติดไฟได้สูง, เป็นอันตราย | ||
| GHS labelling: | |||
 
| |||
| เตือน | |||
| H228, H317 | |||
| P210, P240, P241, P261, P272, P280, P302+P352, P321, P333+P313, P363, P370+P378, P501 | |||
| NFPA 704 (fire diamond) | |||
| จุดวาบไฟ | 250 องศาเซลเซียส (482 องศาฟาเรนไฮต์; 523 เคลวิน) | ||
| 410 องศาเซลเซียส (770 องศาฟาเรนไฮต์; 683 เคลวิน) | |||
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |||
เมทีนามีนเป็นสารที่ได้จากการเกิดปฏิกิริยาระหว่างงฟอร์มาลดีไฮด์กับแอมโมเนีย[3] ถูกค้นพบโดยอเล็กซานเดอร์ บัทเลรอฟ เมื่อ ค.ศ. 1859[4] มีการนำเมทีนามีนมาใช้ประโยชน์ในหลายวัตถุประสงค์ ทั้งใช้เป็นส่วนผสมในการผลิตวัสดุคอมโพสิต[3] ใช้เป็นยาปฏิชีวนะ[5] เป็นสีย้อมในการศึกษาทางมิญชวิทยา[6] เชื้อเพลิงแข็ง[7] สารกันเสีย[8] ตัวทำปฏิกิริยา[9] รวมไปถึงการผลิตวัตถุระเบิด[3]
ถึงแม้ว่าเมทีนามีนจะสามารถนำไปใช้ประโยชน์ได้อย่างหลากหลาย แต่เนื่องด้วยความต้องการของตลาดที่มีน้อยลง ประกอบกับการมีสารตัวเลือกอื่นที่เพิ่มมากขึ้น ทำให้ปริมาณการผลิตสารนี้ลดลงอย่างต่อเนื่องตั้งแต่ช่วงปี ค.ศ. 1990 เป็นต้นมา ในปัจจุบันยังมีการผลิตสารนี้อยู่ในเยอรมนี เนเธอร์แลนด์ อิตาลี ออสเตรเลีย สหรัฐอเมริกา และเม็กซิโก[7]
ประวัติ
แก้เมทีนามีน หรือที่เรียกกันเป็นทางการว่า เฮกซะเมทิลีนเตตรามีน ถูกค้นพบโดยนักเคมีชาวรัสเซีย อเล็กซานเดอร์ บัทเลรอฟ เมื่อ ค.ศ. 1859[4][10][11] โดยถูกเตรียมขึ้นได้จากการทำปฏิกิริยากันระหว่างฟอร์มาลดีไฮด์กับแอมโมเนีย[3] โดยการเกิดปฏิกิริยาดังกล่าวสามารถถูกเหนี่ยวนำได้ทั้งในกรณีที่สารตั้งต้นทั้งสองอยู่ในสถาะแก๊สและสารละลาย
แผนภาพแสดงกระบวนการสังเคราะห์เฮกซะเมทิลีนเตตรามีน
|
โมเลกุลของเฮกซะเมทิลีนเตตรามีนมีความคล้ายคลึงกันเป็นอย่างมากกับโครงสร้างของอะดาแมนแทน โดยจะมีโครงสร้างเป็นแบบสมมาตรทรงสี่หน้ารูปร่างคล้ายกรง มุมทั้งสี่มุมเป็นอะตอมของไนโตรเจน เชื่อมต่อกับอะตอมไนโตรเจนอื่นในโมเลกุลด้วยสะพานเมทิลีน (methylene bridge) ถึงแม้ว่าโมเลกุลของเฮกซะเมทิลีนเตตรามีนจะมีรูปร่างคล้ายกรง แต่ก็ไม่มีตำแหน่งด้านหน้าใดๆในโมเลกุลที่จะสามารถเข้าจับกับอะตอมหรือโมเลกุลอื่นเพิ่มเติมได้ เช่นที่พบได้ในอีเทอร์มงกุฎ หรือโครงสร้างคริปแทนด์ขนาดใหญ่
โมเลกุลของเฮกซะเมทิลีนเตตรามีนจะแสดงคุณสมบัติคล้ายคลึงกับโมเลกุลของกรดอะมิโน โดยสามารถเกิดโปรโตเนชันและ N-อัลคิเลชันได้ (เช่น ควอเทอร์เนียม-15)
การใช้ประโยชน์
แก้ส่วนใหญ่แล้วเฮกซะเมทิลีนเตตรามีนมักถูกนำมาใช้ในการผลิตผงหรือยางฟีนอลฟอร์มาลดีไฮด์ชนิดเหลว และวัสดุคอมโพสิตชนิดยางฟีนอลิคโดยใช้แม่พิมพ์ (phenolic resin moulding compound) เพื่อเป็นสารทำให้คอมโพสิตแข็งตัว โดยผลิตภัณฑ์ต่างๆที่ผลิตได้เหล่านี้มักเป็นผลิตภัณฑ์ที่ต้องอาศัยการยึดเกาะ เช่น เบรกรถ ผ้าคลัตช์ ผ้าทราย ผ้าใยสังเคราะห์ วัสดุทนไฟ เป็นต้น[3]
นอกจากนี้ยังพบว่าเฮกซะเมทิลีนเตตราอาจสามารถทำหน้าที่เป็นแม่พิมพ์โครงร่างโมเลกุล (molecular building block) สำหรับการสังเคราะห์ผลึกโครงสร้างนาโนโดยจัดวางโมเลกุลอย่างเป็นระเบียบได้ด้วยตนเอง (self-assembly) ได้ด้วย[12][13]
การใช้ประโยชน์ทางการแพทย์
แก้ในวงการแพทย์ได้ริเริ่มการนำเฮกซะเมทิลีนเตตรามีน มาใช้ในการฆ่าเชื้อในระบบทางเดินปัสสาวะเป็นครั้งแรกเมื่อปี ค.ศ. 1899[14] แต่ใช้ได้ผลในผู้ป่วยที่มีค่าพีเอชของสารละลายในทางเดินปัสสาวะเป็นกรดเท่านั้น ส่วนในผู้ป่วยที่มีสารละลายในทางเดินปัสสวะเป็นด่างมักพิจารณาใช้กรดบอริกแทนสำหรับข้อบ่งใช้ข้างต้น[15] โดยนักวิทยาศาสตร์พบว่ามีสหสัมพันธ์แบบแปรผันตรงระหว่าง ความเป็นกรดของสภาพแวดล้อมรอบเฮกซะเมทิลีนเตตรามีนกับการสลายตัวของสารดังกล่าว[14] ดังนั้น ประสิทธิภาพในการรักษาของเฮกซะเมทิลีนเตตรามีนจึงขึ้นอยู่กับความเป็นกรดของปัสสาวะ มากกว่าปริมาณยาทั้งหมดที่ผู้ป่วยได้รับในการรักษา[15] ในทางตรงกันข้าม หากสภาพแวดล้อมภายนอกมีสภาวะเป็นด่างนั้น เฮกซะเมทิลีนเตตรามีนแทบจะไม่สามารถออกฤทธิ์ฆ่าเชื้อก่อโรคใดๆ ได้เลย[15]
นอกจากนี้ เฮกซะเมทิลีนเตตรามีนยังเคยถูกนำมาใช้ในกระบวนการการรักษาทหารได้รับบาดเจ็บจากการสูดก๊าซพิษฟอสจีนในช่วงสงครามโลกครั้งที่ 1 ซึ่งการศึกษาทางคลินิกในภายหลังพบว่า การได้รับเฮกซะเมทิลีนเตตรามีนในขนาดสูงก่อนการสูดดมก๊าซพิษดังกล่าว จะช่วยป้องกันการเกิดพิษจากแก๊สนั้นได้ ในทางตรงกันข้าม การได้รับเฮกซะเมทิลีนเตตรามีนภายหลังจากการสัมผัสก๊าซพิษฟอสจีนแล้ว พบว่าไม่ก่อให้เกิดผลในการรักษาอาการพิษแต่อย่างใด[16]
ในปัจจุบัน เฮกซะเมทิลีนเตตรามีนในรูปแบบเกลือของกรดแมนดีลิค (ชื่อสามัญตามเภสัชตำรับอังกฤษ คือ เมทีนามีน แมนดีเลท[17]) นั้นถูกนำมาใช้ในการรักษาการติดเชื้อแบคทีเรียในระบบทางเดินปัสสาวะ โดยสารดังกล่าวจะสลายตัวในกระเพาะปัสสาวะที่มีสภาวะเป็นกรด ได้ผลิตภัณฑ์เป็นฟอร์มาลดีไฮด์และแอมโมเนีย ซึ่งฟอร์มาลดีไฮด์ที่เกิดขึ้นนี้จะมีคุณสมบัติในการฆ่าแบคทีเรียก่อโรค ส่วนกรดแมนดีลิคที่ถูกเพิ่มเข้ามาในเภสัชตำรับนั้นมีจุดประสงค์เพื่อเสริมฤทธิ์ของฟอร์มาลดีไฮด์ อย่างไรก็ตาม เพื่อให้มั่นใจว่าค่าพีเอชของสารละลายในกระเพาะปัสสาวะนั้นเอื้อต่อการออกฤทธิ์ของเฮกซะเมทิลีนเตตรามีน จึงมักมีการบริหารวิตามินซีหรือแอมโมเนียมคลอไรด์ให้กับผู้ป่วยร่วมด้วย เพื่อเพิ่มความเป็นกรดของสารละลายในกระเพาะปัสสาวะ อย่างไรก็ตาม การใช้เฮกซะเมทิลีนเตตรามีนเพื่อเป็นยาปฏิชีวนะนี้มีปริมาณการใช้ลดลงในช่วงปลายคริสต์ทศวรรตที่ 1990 เนื่องจากอาการไม่พึงประสงค์ที่เกิดขึ้น โดยเฉพาะอย่างยิ่งการเกิดกระเพาะปัสสาวะอักเสบรุนแรงชนิด hemorrhagic cystitis จากการเหนี่ยวนำของสารเคมีในผู้ที่ได้รับยาเกินขนาด[5] แต่ ณ ปัจจุบัน ยาดังกล่าวได้รับการรับรองใหม่อีกครั้งเพื่อใช้สำหรับข้อบ่งใช้ดังข้างต้น อันเป็นมาตรการตอบสนองต่อความชุกของการดื้อยาปฏิชีวนะของแบคทีเรียที่มากขึ้นในปัจจุบัน โดยยานี้มีความเหมาะสมอย่างยิ่งที่จะนำมาใช้ต่อเนื่องระยะยาว เพื่อป้องกันการเกิดการติดเชื้อในระบบทางเดินปัสสาวะ เนื่องจากแบคทีเรียไม่สามารถปรับตัวให้ดื้อต่อฟอร์มาลดีไฮด์ได้ อย่างไรก็ดี ยานี้ไม่สามารถใช้ในผู้ป่วยที่มีการทำงานของไตบกพร่องได้ เนื่องจากจะทำให้อาการชองโรคแย่ลงและเกิดอาการไม่พึงประสงค์จากยาได้มากขึ้น นอกจากนี้แล้วยังมีการพัฒนาเฮกซะเมทิลีนเตตรามีนให้อยู่ในรูปแบบยาครีมและสเปรย์ เพื่อใช้ในการรักษาภาวะที่เหงื่อออกมากและกลิ่นตัวแรงเกินไป[18]
อาการไม่พึงประสงค์ที่อาจเกิดขึ้นได้ในผู้ที่ได้รับการรักษาด้วยเฮกซะเมทิลีนเตตรามีน ได้แก่ เกิดผื่นคันตามผิวหนัง ระคายเคืองทางเดินอาหาร คลื่นไส้ อาเจียน กระเพาะอาหารอักเสบ ท้องเสีย เกิดตะคริวที่ท้อง ปัสสาวะไม่ออกหรือปัสสาวะขัด มีเลือดปนมากับปัสสาวะหรือปัสสาวะเป็นเลือด ปัสสาวะถี่และบ่อย การตรวจปัสสาวะอาจพบมีโปรตีนในปัสสาวะ[11] ซึ่งอาการไม่พึงประสงค์ที่เกิดขึ้นกับระบบทางเดินปัสสาวะ เป็นสาเหตหลักที่ทำให้มีการใช้เฮกซะเมทิลีนเตตรามีนลดน้อยลงในปัจจุบัน[5]
การย้อมสีทางมิญชวิทยา
แก้ในการศึกษาทางมิญชวิทยานั้นมีการนำสีย้อมเมทีนามีนซิลเวอร์หลายชนิดมาใช้เพื่อย้อมติดสีแกรม ได้แก่:
- สีย้อมเมทีนามีนซิลเวอร์ของโกรค็อตต์ ถูกนำมาใช้เพื่อคัดเลือกจุลชีพจำพวกราเส้นไยกันอย่างแพร่หลาย
- สีย้อมโจนส์ เป็นเมทีนามีนซิลเวอร์จำพวก Periodic acid-Schiff สำหรับย้อมเยื่อรองรับพื้นฐาน, หรือย้อมเพื่อดู "spiked" ของเยื่อรองรับพื้นฐานของไต ซึ่งมีความสัมพันธ์กับการเกิด membranous glomerulonephritis[6]
เชื้อเพลิงแข็ง
แก้เช่นเดียวกันกับ 1,3,5-ไตรออกเซน, เฮกซะเมทิลีนเตตรามีนเป็นส่วนประกอบหนึ่งของเชื้อเพลิงเม็ดเฮกซะมีนที่นิยมใช้ในกลุ่มคนตั้งแคมป์, ออกค่าย, หน่วยทหาร เพื่อเป็นแหล่งความร้อนในการประกอบอาหารและการปันส่วนเชื้อเพลิงในหน่วยทหาร เชื้อเพลิงแข็งชนิดนี้มีข้อดีคือไม่ก่อให้เกิดควันเมื่อเกิดการเผาไหม้, มีปริมาณความร้อนจากการเผาไหม้ (Heat of combustion) ที่สูงมากถึง 30.0 เมกะจูลต่อกิโลกรัม (MJ/kg), ไม่กลายเป็นสาเหลวเมื่อเกิดการเผาไหม้ และไม่เหลือเถ้าจากการเผา นอกจากนี้ เชื้อเพลิงเมทีนามีน (เฮกซะมีน) มาตรฐาน 0.149 กรัม ถูกนำมาใช้เป็นแหล่งกำเนิดไฟที่สะอาดและทำซ้ำได้ในห้องปฏิบัติกันไฟเพื่อทดสอบการติดไฟของพรมปูพื้น[7]
วัตถุเจือปนอาหาร
แก้เฮกซะเมทิลีนเตตรามีน หรือเฮกซะมีนยังถูกนำมาใช้เป็นวัตถุเจือปนอาหารเพื่อป้องกันการเน่าเสีย (INS number 239) โดยได้รับการรับรองจากสหภาพยุโรปให้ใช้สารนี้เพื่อจุดประสงค์ดังกล่าวได้[8] ภายใต้เลขอี E239 อย่างไรก็ตาม เฮกซะเมทิลีนเตตรามีนไม่ได้รับการรับรองให้ใช้เป็นวัตถุเจือปนอาหารในสหรัฐอเมริกา, รัสเซีย, ออสเตรเลีย และนิวซีแลนด์[19]
ตัวทำปฏิกิริยาในเคมีอินทรีย์
แก้เฮกซะเมทิลีนเตตรามีนเป็นตัวทำปฏิกิริยาอเนกประสงค์ในการสังเคราะห์อินทรีย์,[9] สารนี้ถูกนำมาใช้ในปฏิกิริยาดัฟฟ์ (ปฏิกิริยาฟอร์มิเลชันของเอรีน),[20] ปฏิกิริยาซอมเมเลต์ (การเปลี่ยนเบนซิลเฮไลด์ไปเป็นอัลดีไฮด์),[21] และปฏิกิริยาดีลีพีน (การสังเคราะห์เอมีนจากอัลคิลเฮไลด์)[22]
วัตถุระเบิด
แก้เฮกซะเมทิลีนเตตรามีนเป็นส่วนประกอบพื้นฐานในการสร้างระเบิด RDX และระเบิด C-4[3] รวมไปถึงระเบิดออคโตเจน, เฮกซามีนไดไนเตรท และ เฮกซะเมทิลีน ไตรเปอร์ออกไซด์ ไดเอมีน (HMTD) ตัวอย่างปฏิกิริยาการสร้างระเบิด RDX ดังแสดงต่อไปนี้[23]
- เฮกซะมีน + 10 กรดไนตริก → RDX + 3 เมทิลีนไดไนเตรท + แอมโมเนียมไนเตรท + 3 น้ำ
- (CH2)6N4 + 10 HNO3 → (CH2-N-NO2)3 + 3 CH2 (NO3)2 + NH4NO3 + 3 H2O
แนวโน้มการผลิต
แก้ตั้งแต่ช่วงปี ค.ศ. 1990 เป็นต้นมา จำนวนผู้ผลิตเฮกซะเมทิลีนเตตรามีนในยุโรปนั้นลดลงอย่างต่อเนื่อง อาทิ โรงงาน SNPE ของฝรั่งเศสที่ปิดกิจการไปในปี 1990, การผลิตในโรงงานที่ลอยนา ประเทศเยอรมนีได้หยุดลงในปี ค.ศ. 1993, ปี ค.ศ. 1996 โรงงานผลิตในอาโกรลิงซ์ได้ปิดกิจการลง, ปี ค.ศ. 2001 บอร์เดนผู้ผลิตเฮกซะเมทิลีนเตตรามีนในสหราชอาณาจักรได้หยุดการดำเนินกิจการ, ปี ค.ศ. 2006 โรงงานเคมโค (Chemko) ในสาธารณรัฐสโลวักได้หยุดการผลิตยานี้ลงเช่นกัน โดยในปัจจุบัน โรงงานที่ยังคงมีการผลิตเฮกซะเมทิลีนเตตรามีนอยู่ ได้แก่ INEOS ของเยอรมนี, Caldic ของเนเธอร์แลนด์, และ Hexion ของอิตาลี ส่วนในสหรัฐอมเริกา Eli Lilly and Company ได้หยุดการผลิตสารนี้ไปเมื่อปี ค.ศ. 2002[7] นอกเหนือจากยุโรปแล้ว ในออสเตรเลียและเม็กซิโกยังมีการผลิตเฮกซะเมทิลีนเตตรามีนเพื่อใช้เป็นเม็ดเชื้อเพลิงซึ่งดำเนินการโดย บริษัทธาลส์ ออสเตรเลีย จำกัด (Thales Australia) และ เอบิยา (Abiya) ตามลำดับ
เฮกซะเมทิลีนเตตรามีนมีจำหน่ายในประเทศไทยภายใต้ชื่อการค้า Hiprex (ฮิปเปร็กซ์) โดยบริษัท Aventis Pharmaceuticals, Urex (ยูเร็กซ์) ของบริษัท Vatring Pharmaceuticals และ Mandelamine (แมนเดลามีน) ของบริษัท Warner Chilcott Laboratories[11]
ดูเพิ่ม
แก้อ้างอิง
แก้- ↑ Cooney, A. P.; Crampton, M. R.; Golding, P. (1986). "The acid-base behaviour of hexamine and its N-acetyl derivatives". J. Chem. Soc., Perkin Trans. 2 (6): 835–839. doi:10.1039/P29860000835.
- ↑ PubChem. "Methenamine". สืบค้นเมื่อ March 28, 2018.
- ↑ 3.0 3.1 3.2 3.3 3.4 3.5 Eller, K.; Henkes, E.; Rossbacher, R.; Höke, H. (2000). "Amines, Aliphatic". Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag GmbH. doi:10.1002/14356007.a02_001. ISBN 9783527306732.
- ↑ 4.0 4.1 Butlerow, A. (1859). "Ueber einige Derivate des Jodmethylens" [On some derivatives of methylene iodide]. Ann. Chem. Pharm. (ภาษาเยอรมัน). 111 (2): 242–252. doi:10.1002/jlac.18591110219. In this paper, Butlerov discovered formaldehyde, which he called "Dioxymethylen" (methylene dioxide) [page 247] because his empirical formula for it was incorrect (C4H4O4). On pages 249–250, he describes treating formaldehyde with ammonia gas, creating hexamine.
- ↑ 5.0 5.1 5.2 Ross, R. R.; Conway, G. F. (1970). "Hemorrhagic cystitis following accidental overdose of methenamine mandelate". Am. J. Dis. Child. 119 (1): 86–87. doi:10.1001/archpedi.1970.02100050088021. PMID 5410299.
- ↑ 6.0 6.1 "Renal Pathology". สืบค้นเมื่อ 2008-11-25.
- ↑ 7.0 7.1 7.2 7.3 Alan H. Schoen (2004), Re: Equialence of methenamine Tablets Standard for Flammability of Carpets and Rugs เก็บถาวร 2008-10-05 ที่ เวย์แบ็กแมชชีน. U.S. Consumer product Safety Commission, Washington, DC, July 29, 2004. Many other countries who still produce this include Russia, Saudi Arabia, China and Australia.
- ↑ 8.0 8.1 UK Food Standards Agency: "Current EU approved additives and their E Numbers". สืบค้นเมื่อ 2011-10-27.
- ↑ 9.0 9.1 Blažzević, N.; Kolbah, D.; Belin, B.; Šunjić, V.; Kajfež, F. (1979). "Hexamethylenetetramine, A Versatile Reagent in Organic Synthesis". Synthesis. 1979 (3): 161–176. doi:10.1055/s-1979-28602.
- ↑ Butlerow, A. (1860). "Ueber ein neues Methylenderivat" [On a new methylene derivative]. Ann. Chem. Pharm. (ภาษาเยอรมัน). 115 (3): 322–327. doi:10.1002/jlac.18601150325.
- ↑ 11.0 11.1 11.2 อภัย ราษฎรวิจิตร (February 13, 2016). "เมทีนามีน (Methenamine)". หาหมอ.com. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ November 14, 2017. สืบค้นเมื่อ April 28, 2018.
- ↑ Markle, R. C. (2000). "Molecular building blocks and development strategies for molecular nanotechnology". Nanotechnology. 11: 89. doi:10.1088/0957-4484/11/2/309.
- ↑ Garcia, J. C.; Justo, J. F.; Machado, W. V. M.; Assali, L. V. C. (2009). "Functionalized adamantane: building blocks for nanostructure self-assembly". Phys. Rev. B. 80: 125421. doi:10.1103/PhysRevB.80.125421.
- ↑ 14.0 14.1 Heathcote, Reginald St. A. (1935). "HEXAMINE AS AN URINARY ANTISEPTIC: I. ITS RATE OF HYDROLYSIS AT DIFFERENT HYDROGEN ION CONCENTRATIONS. II. ITS ANTISEPTIC POWER AGAINST VARIOUS BACTERIA IN URINE". British Journal of Urology. 7 (1): 9–32. doi:10.1111/j.1464-410X.1935.tb11265.x. ISSN 0007-1331.
- ↑ 15.0 15.1 15.2 Elliot (1913). "On Urinary Antiseptics". British Medical Journal. 98: 685–686.
- ↑ Diller, Werner F. (1980). "The methenamine misunderstanding in the therapy of phosgene poisoning (review article)". Archives of Toxicology. 46 (3–4): 199–206. doi:10.1007/BF00310435. ISSN 0340-5761.
- ↑ "Methenamine mandelate, USP". Edenbridge Pharmaceuticals. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2017-05-17. สืบค้นเมื่อ 2018-03-29.
- ↑ D E James-Levi (April 1945). "[Treatment of Excessive Sweating of Feet With Urotropine]". Voenno-meditsinskii zhurnal. 45: 38. ISSN 0026-9050. PMID 20341260.
- ↑ Australia New Zealand Food Standards Code"Standard 1.2.4 - Labelling of ingredients". สืบค้นเมื่อ 2011-10-27.
- ↑ Allen, C. F. H.; Leubne, G. W. (1951). "Syringic Aldehyde". Organic Syntheses. 31: 92. doi:10.15227/orgsyn.031.0092.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Wiberg, K. B. (1963). "2-Thiophenaldehyde". Organic Syntheses. doi:10.15227/orgsyn.000.0000.; Collective Volume, vol. 3, p. 811
- ↑ Bottini, A. T.; Dev, V.; Klinck, J. (1963). "2-Bromoallylamine". Organic Syntheses. 43: 6. doi:10.15227/orgsyn.043.0006.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Luo, K.-M.; Lin, S.-H.; Chang, J.-G.; Huang, T.-H. (2002), "Evaluations of kinetic parameters and critical runaway conditions in the reaction system of hexamine-nitric acid to produce RDX in a non-isothermal batch reactor", Journal of Loss Prevention in the Process Industries, 15 (2): 119–127, doi:10.1016/S0950-4230(01)00027-4.