โรคเมลิออยด์
โรคเมลิออยด์[5] หรือ โรคเมลิออยโดซิส[6] (อังกฤษ: Melioidosis) เป็นโรคติดเชื้อซึ่งเกิดจากเชื้อแบคทีเรียแกรมลบ Burkholderia pseudomallei เชื้อนี้พบได้ในดินและน้ำ โรคนี้มีความสำคัญทางสาธารณสุขโดยเฉพาะในประเทศไทยและทางเหนือของออสเตรเลีย รูปแบบของโรคอาจมีได้ทั้งชนิดเฉียบพลันและเรื้อรัง ผู้ป่วยอาจมีอาการแตกต่างกันมาก เช่น เจ็บหน้าอก กระดูก หรือข้อ ไอ การติดเชื้อที่ผิวหนัง ก้อนในปอด หรือปอดอักเสบ
| โรคเมลิออยด์ (Melioidosis) | |
|---|---|
| ชื่ออื่น | โรคเมลิออยโดซิส, โรคไข้ดิน, โรคฝีดิน, โรคมงคล่อเทียม[1], Whitmore disease[2] |
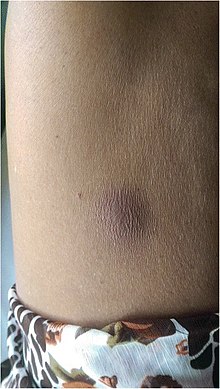 | |
| ฝีเมลิออยโดซิสที่หน้าท้อง | |
| สาขาวิชา | โรคติดเชื้อ (การแพทย์เฉพาะทาง) |
| อาการ | ไม่มีอาการ, ไข้, ปอดบวม, ฝีหลายตำแหน่ง[3] |
| ภาวะแทรกซ้อน | สมองและไขสันหลังอักเสบ, ช็อกเหตุพิษติดเชื้อ, กรวยไตอักเสบเฉียบพลัน, ข้ออักเสบติดเชื้อ, กระดูกอักเสบติดเชื้อ[3] |
| การตั้งต้น | 1–21 วันหลังจากรับสัมผัสเชื้อ[3] |
| สาเหตุ | แบคทีเรีย Burkholderia pseudomallei แพร่กระจายโดยการสัมผัสกับดินหรือน้ำ[3] |
| ปัจจัยเสี่ยง | เบาหวาน, ทาลัสซีเมีย, โรคพิษสุรา, โรคไตเรื้อรัง[3] |
| วิธีวินิจฉัย | การเจริญของแบคทีเรียในอาหารเลี้ยงเชื้อ[3] |
| โรคอื่นที่คล้ายกัน | วัณโรค[4] |
| การป้องกัน | ป้องกันการสัมผัสน้ำที่ปนเปื้อน, ใช้ยาปฏิชีวนะป้องกันการติดเชื้อ[3] |
| การรักษา | เซฟตาซิดิม, เมอโรพีเนม, โคไตรมอกซาโซล[3] |
| ความชุก | 165,000 คนต่อปี[3] |
| การเสียชีวิต | 89,000 คนต่อปี[3] |
ในอดีตเชื้อแบคทีเรีย B. pseudomallei จัดอยู่ในจีนัส Pseudomonas และเคยใช้ชื่อวิทยาศาสตร์ว่า Pseudomonas pseudomallei จนกระทั่งปี ค.ศ. 1992 มีการจำแนกทางวิวัฒนาการพบว่ามีความใกล้ชิดกับเชื้อ Burkholderia mallei ซึ่งก่อโรคแกลนเดอร์ส (Glanders) หรือโรคมงคล่อพิษในม้า ลา และล่อ ชื่อโรคเมลิออยด์นี้มาจากภาษากรีกว่า melis หมายความว่า "โรคติดเชื้อของลา" และคำท้าย -oid หมายถึง "คล้ายคลึง" และ -osis หมายถึง "ภาวะ" ดังนั้นชื่อโรคจึงหมายความว่า ภาวะซึ่งคล้ายกับโรคแกลนเดอร์ส[7]
ระบาดวิทยา
แก้โรคเมลิออยด์เป็นโรคประจำถิ่นในเอเชียตะวันออกเฉียงใต้ (รวมถึงประเทศไทย[8] ลาว[9][10] และตอนใต้ของจีน[11] สิงคโปร์[12] มาเลเซีย พม่า และเวียดนาม) ไต้หวัน[13][14] และตอนเหนือของออสเตรเลีย[15][16] และมีรายงานผู้ป่วยหลายรายในฮ่องกง บรูไน[17] อินเดีย[18][19][20] และมีรายงานผู้ป่วยประปรายในอเมริกากลางและอเมริกาใต้[21] ตะวันออกกลาง แปซิฟิก และประเทศในแอฟริกัน แม้ว่าจะมีรายงานผู้ป่วยเพียงรายเดียวในบังคลาเทศ[22] แต่พบผู้ป่วยอย่างน้อยห้ารายที่เดินทางจากประเทศดังกล่าวเข้ามาในสหราชอาณาจักร ซึ่งแสดงว่าเมลิออยโดซิสเป็นโรคประจำถิ่นในประเทศดังกล่าว แต่กลับมีปัญหาไม่ได้รับการวินิจฉัยหรือปัญหารายงานจำนวนผู้ป่วยน้อยกว่าที่ควรจะเป็น[23] ซึ่งอาจเกิดจากการขาดแคลนอุปกรณ์ปฏิบัติการที่เพียงพอ
ภาคตะวันออกเฉียงเหนือของประเทศไทยมีอุบัติการณ์ของโรคเมลิออยด์สูงที่สุดในโลก (ผู้ป่วยโรคเมลิออยด์ 21.3 รายในประชากร 100,000 รายต่อปี) [24] ร้อยละ 80 ของเด็กในภาคตะวันออกเฉียงเหนือของไทยมีผลแอนติบอดีต่อเชื้อ B. pseudomallei เป็นบวกตั้งแต่อายุ 4 ปี[25] ซึ่งพบว่าในที่อื่น ๆ จะมีจำนวนน้อยกว่านี้[26][27][28][29]
โรคเมลิออยด์เป็นโรคที่พบในสัตว์ อาทิ แมว[30] แพะ แกะ และม้า ส่วนในวัว ควาย และจระเข้ เชื่อว่ามีความต้านทานต่อการติดเชื้อเมลิออยโดซิสทั้งที่สัมผัสกับโคลนอยู่ตลอด[31] การระบาดของโรคในสวนสัตว์ปารีสในทศวรรษที่ 1970 ("L’affaire du jardin des plantes") เชื่อว่ามีต้นเหตุจากแพนด้าที่นำเข้ามา[32]
เชื้อแบคทีเรีย Burkholderia pseudomallei ปกติพบได้ในดินและน้ำผิวดิน ประวัติการสัมผัสดินหรือแหล่งน้ำจึงแทบไม่แตกต่างกันในผู้ป่วยโรคเมลิออยด์[15] นั่นคือผู้ป่วยส่วนใหญ่ที่มีประวัติสัมผัสกับดินที่ปนเปื้อนไม่มีอาการเจ็บป่วย แม้แต่ในแหล่งชุกชุมของโรคการกระจายของเชื้อ B. pseudomallei ในดินก็เป็นอย่างประปราย[33][34] การปนเปื้อนเชื้อของน้ำใต้ดินเป็นสาเหตุของการระบาดครั้งหนึ่งในตอนเหนือของออสเตรเลีย[35]
ปัจจัยเสี่ยงที่สำคัญที่สุดของการเป็นโรคเมลิออยด์อย่างรุนแรงคือเบาหวาน ปัจจัยเสี่ยงอื่นอาทิ ทาลัสซีเมีย โรคไต และอาชีพ (เกษตรกรรม) [36] เชื่อกันว่าเชื้อเข้าสู่ร่างกายทางบาดแผลที่ผิวหนัง หรือผ่านการหายใจเอาเชื้อ B. pseudomallei เข้าไป มีรายงานของการติดต่อจากคนสู่คนแต่ค่อนข้างพบได้ไม่บ่อย[37][38]
นอกจากนี้ยังพบว่าโรคมีความสัมพันธ์กับฝน โดยพบว่าจำนวนและความรุนแรงของผู้ป่วยเพิ่มขึ้นตามปริมาณฝน[39][40][12][41][42]
อาการทางคลินิก
แก้โรคเมลิออยด์เฉียบพลัน
แก้ในผู้ป่วยบางกลุ่มที่สามารถระบุเวลาที่ติดเชื้อได้ พบว่าระยะฟักตัวเฉลี่ยของโรคเมลิออยด์เฉียบพลันคือ 9 วัน (ตั้งแต่ 1-12 วัน) [43] ผู้ป่วยที่ติดเชื้อโรคเมลิออยด์แอบแฝงอาจไม่แสดงอาการเลยได้หลายสิบปี โดยช่วงเวลาตั้งแต่สันนิษฐานว่าติดเชื้อจนถึงระยะปรากฏอาการที่นานที่สุดเท่าที่มีรายงานคือ 62 ปี[44] ระยะฟักตัวที่ยาวนานเริ่มเป็นที่รู้จักกันจากในทหารสหรัฐอเมริกาในสมรภูมิสงครามเวียดนามที่ป่วยและเสียชีวิตจำนวนมากหลังกลับจากสมรภูมิหลายสิบปี จนได้รับสมญานามว่า "ระเบิดเวลาเวียดนาม" (Vietnam time-bomb) ความรุนแรงของโรคเมลิออยด์มีได้หลากหลาย ในผู้ป่วยเรื้อรังอาจแสดงอาการได้นานเป็นเดือน แต่ผู้ป่วยที่ติดเชื้อเร็วร้าย (fulminant infection) โดยเฉพาะภาวะจมน้ำ อาจแสดงอาการรุนแรงได้ภายในไม่กี่ชั่วโมง
ผู้ป่วยโรคเมลิออยด์เฉียบพลันมักมีอาการมาด้วยไข้ อาการปวดหรืออาการอื่น ๆ อาจช่วยบ่งบอกการติดเชื้อเฉพาะที่ได้ โดยพบได้ราวร้อยละ 75 ของผู้ป่วย อาการอื่นเช่นไอหรือเจ็บหน้าอกอาจบ่งถึงภาวะปอดอักเสบ อาการปวดข้อหรือกระดูกอาจบ่งถึงภาวะกระดูกอักเสบหรือข้ออักเสบติดเชื้อ หรือเซลล์เนื้อเยื่ออักเสบ (cellulitis) การติดเชื้อในช่องท้องเช่นฝีในตับ ม้าม หรือต่อมลูกหมาก มักไม่แสดงอาการมาด้วยปวดเฉพาะที่ จึงควรตรวจด้วยการวินิจฉัยทางรังสีเช่นการตรวจด้วยคลื่นเสียงความถี่สูงหรือการตรวจเอกซ์เรย์คอมพิวเตอร์ ในการศึกษาผู้ป่วย 214 ราย พบว่าร้อยละ 27.6 มีฝีที่ตับและม้าม (ช่วงความเชื่อมั่น 95%, 22.0% ถึง 33.9%) ลักษณะของฝีที่เกิดจากเชื้อ B. pseudomallei ในภาพเอกซ์เรย์คอมพิวเตอร์มีลักษณะคล้ายรังผึ้ง (honeycomb) หรือ เนยแข็งสวิส (swiss cheese) คือทึบเสียง มีผนังกั้นหลายอัน และแบ่งเป็นหลายช่อง (hypoechoic, multi-septate, multiloculate) [45][46]
อาการของการติดเชื้อเฉพาะส่วนแสดงอาการได้หลากหลาย เช่น ฝีของต่อมน้ำลายพาโรติด พบในผู้ป่วยเด็กชาวไทย แต่ในผู้ป่วยออสเตรเลียมีรายงานพบเพียงหนึ่งราย[47] ในทางกลับกัน ฝีของต่อมลูกหมากพบได้ถึงร้อยละ 20 ของผู้ป่วยชายชาวออสเตรเลียแต่ไม่พบรายงานในที่อื่น อาการสมองและไขสันหลังอักเสบพบได้ในตอนเหนือของออสเตรเลีย
ผู้ป่วยโรคเมลิออยด์มักมีปัจจัยเสี่ยงร่วมด้วย เช่น เบาหวาน ทาลัสซีเมีย การดื่มแอลกอฮอล์ หรือโรคไต และมักให้ประวัติอาชีพหรืองานที่สัมผัสกับโคลนหรือน้ำใต้ดิน[48] อย่างไรก็ตาม ในผู้ป่วยที่แข็งแรงรวมทั้งเด็กก็อาจเป็นโรคนี้ได้
ร้อยละ 25 ของผู้ป่วยอาจไม่พบอาการของการติดเชื้อและต้องวินิจฉัยโดยการเพาะเชื้อจากเลือดหรือการป้ายคอมาตรวจ อาจกล่าวได้ว่าโรคเมลิออยด์ทำให้เกิดการติดเชื้อได้กับทุกอวัยวะในร่างกาย ยกเว้นลิ้นหัวใจ แม้ว่าจะพบผู้ป่วยเยื่อหุ้มสมองอักเสบจากเชื้อเมลิออยด์ตามหลังฝีในสมองที่แตกออก แต่ไม่เคยมีรายงานการติดเชื้อเยื่อหุ้มสมองโดยตรง อาการแสดงที่พบได้ไม่บ่อยได้แก่การติดเชื้อในหลอดเลือด ฝีของต่อมน้ำเหลือง (1.2-2.2%) [49] เยื่อหุ้มหัวใจเป็นหนอง และกล้ามเนื้อหัวใจอักเสบ การติดเชื้อในประจันอก (mediastinum) ฝีในต่อมไทรอยด์และถุงอัณฑะ และการติดเชื้อในดวงตา
โรคเมลิออยด์เรื้อรัง
แก้โรคเมลิออยด์เรื้อรังส่วนมากหมายถึงมีอาการยาวนานกว่า 2 เดือน พบได้ในผู้ป่วยราวร้อยละ 10[50] อาการแสดงทางคลินิกของโรคเมลิออยด์เรื้อรังมีการเปลี่ยนแปลงได้ โดยอาจมาด้วยการติดเชื้อที่ผิวหนังเรื้อรัง แผลที่ผิวหนัง ก้อนในปอด หรือปอดอักเสบเรื้อรัง โดยแสดงอาการเลียนแบบวัณโรค บางครั้งอาจเรียกโรคนี้ว่า "วัณโรคเวียดนาม" (Vietnamese tuberculosis) [51] โรคเมลิออยด์เรื้อรังอาจแสดงอาการเลียนแบบวัณโรคเยื่อหุ้มหัวใจ (tuberculous pericarditis) ได้[52]
การวินิจฉัย
แก้การวินิจฉัยยืนยันของโรคเมลิออยด์นั้นทำโดยการเพาะเชื้อจากร่างกาย เนื่องจากโดยปกติแล้วจะไม่พบเชื้อดังกล่าวในร่างกายมนุษย์
ประวัติการสัมผัสดินอาจไม่สามารถซักจากผู้ป่วยได้ เนื่องจากโรคเมลิออยด์อาจแฝงอยู่เป็นเวลาหลายปีกว่าจะแสดงอาการ[53] สำหรับผู้ที่อยู่นอกแหล่งที่โรคเมลิออยด์เป็นโรคประจำถิ่นควรซักประวัติการเดินทางไปยังบริเวณที่พื้นที่เฉพาะถิ่นของโรคเมลิออยด์ บางแหล่งข้อมูลแนะนำให้คิดถึงความเป็นไปได้ที่จะติดเชื้อเมลิออยด์ ในผู้ป่วยทุกรายที่มีประวัติเดินทางไปยังหรืออาศัยอยู่ในแหล่งที่โรคเมลิออยด์เป็นโรคประจำถิ่น
การตรวจคัดกรองการติดเชื้อทุกส่วน ไม่ว่าจะเป็นการเพาะเชื้อจากเลือด เพาะเชื้อจากปัสสาวะ การป้ายคอมาตรวจ และการเพาะเชื้อจะหนองที่ดูดมาได้ ควรทำในผู้ป่วยทุกรายที่สงสัยการติดเชื้อโรคเมลิออยด์ (โดยเพาะเชื้อใน blood agar หรือ Ashdown's medium) ซึ่งสามารถยืนยันการวินิจฉัยโดยการเพาะเชื้อพบ B. pseudomallei จากตัวอย่างใดก็ได้ที่เก็บมา การป้ายคออาจไม่มีความไว (sensitivity) แต่ให้ความจำเพาะ (specificity) ถึง 100% หากให้ผลบวก โดยเฉพาะอย่างยิ่งหากผลเพาะเชื้อจากเสมหะเป็นบวกด้วย[54] ความไวของการเพาะเชื้อจากปัสสาวะจะยิ่งเพิ่มขึ้นหากเพาะเชื้อจากปัสสาวะที่ปั่นเหวี่ยง (centrifuged) และหากผลเพาะเชื้อขึ้นก็นับเป็นผลบวกไม่ว่าจะมีปริมาณเชื้อเท่าใดก็ตาม (ไม่จำเป็นต้องใช้เกณฑ์ทั่วไปที่ปริมาณเชื้อมากกว่า 104 ต่อมิลลิลิตร) [55] ในบางครั้งการเพาะเชื้อจากไขกระดูกอาจให้ผลบวกในผู้ป่วยที่ผลเพาะเชื้อ B. pseudomallei เป็นลบ แต่ก็ไม่แนะนำให้ทำ[56] ข้อผิดพลาดของแพทย์ที่อาจไม่คุ้นเคยกับโรคนี้คือ การส่งตัวอย่างเฉพาะจากอวัยวะที่ติดเชื้อไปตรวจเท่านั้น แทนที่จะส่งตัวอย่างคัดกรองทุกส่วนดังที่กล่าวมาตอนต้น
ตัวกลางเพาะเชื้อ Ashdown's medium เป็นตัวกลางที่มียาปฏิชีวนะเจนตามัยซิน (gentamicin) ซึ่งจำเป็นในการเพาะเชื้อจากส่วนที่ไม่ปราศจากเชื้อ (non-sterile sites) ตัวกลางเพาะเชื้อ Burkholderia cepacia medium อาจเป็นตัวเลือกที่ใช้เพาะเชื้อได้ในบริเวณที่ไม่ใช่พื้นที่โรคเมลิออยด์เป็นโรคประจำถิ่นหากไม่มี Ashdown's medium ให้ใช้ ตัวกลางเพาะเชื้อชนิดใหม่ซึ่งพัฒนามาจาก Ashdown's medium ชื่อว่า Francis medium อาจช่วยในการแยกระหว่างเชื้อ B. pseudomallei กับ B. cepacia และอาจช่วยในการวินิจฉัยโรคเมลิออยด์ได้ในระยะแรก[57] แต่ก็ยังไม่มีการยอมรับกันทางคลินิกอย่างกว้างขวาง ชุดตรวจเพื่อยืนยันเชื้อแบคทีเรียสำเร็จรูปหลายตัวอาจไม่สามารถระบุเชื้อ B. pseudomallei ได้อย่างถูกต้อง
การทดสอบทางวิทยาน้ำเหลือง (serology) สำหรับเชื้อเมลิออยด์ เช่น การทดสอบปริมาณการเกาะกลุ่มของเม็ดเลือดแดงทางอ้อม (indirect haemagglutination assay) แต่อาจไม่สามารถทำได้ในหลายประเทศ ในประเทศที่โรคนี้เป็นโรคประจำถิ่นประชากรมี titre สูงอยู่แล้วทำให้ค่าพยากรณ์ผลบวก (positive predictive value) ลดลง การทดสอบเชื้อที่นิยมกันแพร่หลายในประเทศไทยคือการทดสอบอิมมูโนฟลูออเรสเซนต์โดยตรงจำเพาะ (direct immunofluorescent test) และการเกาะกลุ่มลาเท็กซ์ (latex agglutination) โดยอาศัยสารภูมิต้านทานโมโนโคลน (monoclonal antibodies) แต่การทดสอบนี้ไม่มีที่ใช้ในประเทศอื่น อิมมูโนฟลูออเรสเซนต์โดยตรงมีปฏิกิริยาข้าม (cross-reactivity) เกือบสมบูรณ์กับ B. thailandensis[58]
การวินิจฉัยโรคเมลิออยด์ไม่สามารถทำได้โดยอาศัยวิธีทางรังสี (เอกซเรย์และสแกน) เท่านั้น[59] แต่วิธีการทางรังสีมักถูกใช้เป็นประจำเพื่อประเมินความรุนแรงของโรค[60] แนะนำให้ทำภาพรังสีของช่องท้องโดยเอกซเรย์คอมพิวเตอร์หรือตรวจคลื่นเสียงความถี่สูง เนื่องจากฝีของอวัยวะภายในอาจไม่ได้แสดงอาการทางคลินิกออกมาชัดเจน และอาจพบฝีเกิดร่วมกับโรคที่บริเวณอื่น ในประเทศออสเตรเลียแนะนำให้ทำภาพรังสีเพื่อตรวจต่อมลูกหมากเนื่องจากมีอุบัติการณ์ของฝีที่ต่อมลูกหมากสูงในผู้ป่วยทางตอนเหนือของออสเตรเลีย การทำเอกซเรย์ทรวงอกแนะนำให้ทำเป็นประจำ ร่วมกับการตรวจเพิ่มเติมอื่น ๆ ตามอาการแสดงทางคลินิก การปรากฏฝีที่ตับลักษณะเป็นรังผึ้ง (honeycomb abscesses) เป็นลักษณะของการติดเชื้อเมลิออยด์ที่ตับ แต่ภาพที่เห็นไม่ได้บ่งถึงการวินิจฉัย[59][60]
การวินิจฉัยแยกโรคนั้นมีได้กว้างเนื่องจากโรคเมลิออยด์อาจแสดงลักษณะทางคลินิกเลียนแบบการติดเชื้ออื่น ๆ รวมทั้งวัณโรค[51]
การรักษา
แก้การรักษาปัจจุบัน
แก้การรักษาโรคเมลิออยด์แบ่งได้เป็น 2 ระยะ คือระยะที่ต้องรักษาด้วยยาปฏิชีวนะทางหลอดเลือดดำ และระยะการรักษาต่อเนื่องด้วยยาปฏิชีวนะชนิดรับประทาน
ระยะที่ต้องรักษาด้วยยาปฏิชีวนะทางหลอดเลือดดำ
แก้ยาปฏิชีวนะเซฟตาซิดิม (Ceftazidime) ทางหลอดเลือดดำเป็นยาที่ควรเลือกใช้อันดับแรกเพื่อรักษาโรคเมลิออยด์เฉียบพลันในปัจจุบัน[61][62] ส่วนเมอโรเพเนม (meropenem) [63] ไอมิเพเนม (imipenem) [43] และเซโฟพีราโซน-ซัลแบคแทม (cefoperazone-sulbactam) (หรือ ซัลพีราโซน (Sulperazone)) [64] ก็มีประสิทธิภาพใช้ได้[65] ยาปฏิชีวนะอะม็อกซีซิลลิน-คลาวูลาเนต (amoxicillin-clavulanate) (หรือโคอะม็อกซีคลาฟ (co-amoxiclav)) อาจเลือกใช้ได้หากไม่มียาปฏิชีวนะ 4 ชนิดที่กล่าวมาข้างต้น แต่อาจให้ผลด้อยกว่า[66] ควรให้ยาปฏิชีวนะทางหลอดเลือดดำอย่างน้อย 10 ถึง 14 วัน และไม่ควรหยุดให้จนกว่าอุณหภูมิร่างกายผู้ป่วยลดกลับมาเป็นปกติอย่างน้อย 48 ชั่วโมง โดยส่วนใหญ่แล้วผู้ป่วยมักไม่จำเป็นต้องได้ยาปฏิชีวนะทางหลอดเลือดติดต่อกันนานเกินหนึ่งเดือน
ในประเทศออสเตรเลีย มีการใช้ยาเมอโรเพเนมเพื่อรักษาโรคเมลิออยด์เป็นประจำ[67] ซึ่งให้ผลลัพธ์ที่ดี และในปัจจุบันกำลังมีการวิจัยทดสอบเปรียบเทียบประสิทธิภาพระหว่างเมอโรเพเนมและเซฟตาซิดิมในการรักษาโรคเมลิออยด์ในประเทศไทย โดยใช้ชื่องานวิจัยว่า ATOM[68]
ในทางทฤษฎีแล้วเชื่อว่าอัตราตายในผู้ป่วยโรคเมลิออยด์ที่ได้รับการรักษาด้วยยาไอมิเพเนมจะน้อยกว่าผู้ที่ได้รับยาอื่น เนื่องจากยาไอมิเพเนมทำให้แบคทีเรียที่ตายปล่อยชีวพิษภายในตัวออกมาน้อยกว่า [69] และค่าความเข้มข้นน้อยที่สุดที่ยับยั้งการเจริญเติบโตของเชื้อ (mean inhibitory concentration; MIC) ของยาไอมิเพเนมก็น้อยกว่าเซฟตาซิดิม แต่อย่างไรก็ตามก็ไม่พบความแตกต่างกันระหว่างอัตราตายของผู้ป่วยที่ได้รับยาไอมิเพเนมและเซฟตาซิดิม[43] ค่าความเข้มข้นน้อยที่สุดที่ยับยั้งการเจริญเติบโตของเชื้อ (MIC) ของเมอโรเพเนมต่อเชื้อ B. pseudomallei มีค่าสูงกว่าเชื้ออื่นๆ และผู้ป่วยที่ต้องเข้ารับการกรองเลือด (haemofiltration) อาจต้องได้รับยาบ่อยขึ้นหรือปริมาณสูงขึ้น[70]
เซฟีพิม (cefepime) และเออตาเพเนม (ertapenem) ไม่มีประสิทธิภาพในการทดลองนอกร่างกาย (in vitro) [71] พิเพอราซิลลิน-ซัลแบคแทม (piperacillin-sulbactam) [71] โดริเพเนม (doripenem) และไบอะเพเนม (biapenem) [72] มีประสิทธิภาพในการทดลองนอกร่างกาย แต่ไม่มีการวิจัยทางคลินิกเพื่อยืนยันประสิทธิภาพการรักษาจริง
การให้การรักษาเสริมด้วย Granulocyte colony-stimulating factor (GCSF) [73] หรือโค-ไตรม็อกซาโซล (co-trimoxazole) [74][75] พบว่าไม่ช่วยลดอัตราการเสียชีวิตจากการศึกษาในประเทศไทย
ระยะการรักษาต่อเนื่องด้วยยาปฏิชีวนะชนิดรับประทาน
แก้หลังจากการรักษาในระยะเฉียบพลัน แนะนำให้รักษาต่อเนื่องหรือกำจัดเชื้อด้วยยาโค-ไตรม็อกซาโซล (co-trimoxazole) ร่วมกับดอกซีไซคลีน (doxycycline) เป็นเวลา 12 ถึง 20 สัปดาห์เพื่อลดอัตราการกลับเป็นซ้ำ[76] ปัจจุบันไม่แนะนำให้ใช้คลอแรมเฟนิคอลเพื่อวัตถุประสงค์นี้แล้ว โค-อะม็อกซีคลาฟ (co-amoxiclav) เป็นยาปฏิชีวนะทางเลือกสำหรับผู้ป่วยที่ไม่สามารถใช้ยาโค-ไตรม็อกซาโซลและดอกซีไซคลีน (เช่นผู้ป่วยหญิงตั้งครรภ์ และเด็กอายุต่ำกว่า 12 ปี) [77][78] แต่อาจให้ประสิทธิผลดีไม่เท่า การใช้ยาปฏิชีวนะชนิดรับประทานกลุ่มฟลูออโรควิโนโลน (fluoroquinolone) เพียงชนิดเดียว[79] หรือดอกซีไซคลีนเพื่อการรักษาระยะต่อเนื่องนั้นไม่มีประสิทธิผล[80]
ในออสเตรเลียมีการใช้ยาโค-ไตรม็อกซาโซลชนิดเดียวในการรักษาเพื่อกำจัดเชื้อ[67] โดยมีอัตราการกลับเป็นซ้ำต่ำกว่าที่พบในประเทศไทย นอกจากนี้ยังมีหลักฐานการทดลองนอกร่างกายพบว่าโค-ไตรม็อกซาโซลและดอกซีไซคลีนออกฤทธิ์ต้านกัน และโค-ไตรม็อกซาโซลตัวเดียวน่าจะให้ผลดีกว่า[81] มีการวิจัยเชิงทดลองแบบสุ่มและมีกลุ่มควบคุม (MERTH) เพื่อเปรียบเทียบการรักษาด้วยโค-ไตรม็อกซาโซลชนิดเดียวกับการรักษามาตรฐานด้วยโค-ไตรม็อกซาโซลร่วมกับดอกซีไซคลีนเริ่มในปี ค.ศ. 2006 และเสร็จสิ้นในปี ค.ศ. 2008 การศึกษาสนับสนุนความจำเป็นในการติดตามการรักษาให้เพียงพอและความร่วมมือปฏิบัติตามของผู้ป่วยอย่างดีในการรักษาระยะนี้ ปริมาณยาโค-ไตรม็อกซาโซลต้องคำนวณตามน้ำหนัก (<40 กิโลกรัม: 160/800 มิลลิกรัม ทุก 12 ชั่วโมง; 40–60 กิโลกรัม: 240/1200 มิลลิกรัม ทุก 12 ชั่วโมง, >60 กิโลกรัม: 320/1600 มิลลิกรัม ทุก 12 ชั่วโมง) [82]
การรักษาด้วยการผ่าตัด
แก้การรักษาด้วยการระบายหนองออกใช้เพื่อรักษาฝีในต่อมลูกหมากและข้ออักเสบติดเชื้อ อาจใช้ในการรักษาฝีในต่อมน้ำลายพาโรติด แต่ไม่แนะนำให้ใช้ในการรักษาฝีในตับหรือม้าม ในภาวะที่มีการติดเชื้อเมลิออยด์ในกระแสเลือดที่ไม่ตอบสนองต่อการรักษาด้วยยาปฏิชีวนะทางหลอดเลือดดำอาจพิจารณารักษาด้วยการตัดม้ามแต่มีหลักฐานเพียงเล็กน้อยที่สนับสนุนการรักษาด้วยวิธีนี้[83]
การรักษาในอดีต
แก้ก่อนปี ค.ศ. 1989 การรักษามาตรฐานของโรคเมลิออยด์เฉียบพลันประกอบด้วยยาสามชนิดรวมกัน ได้แก่ คลอแรมเฟนิคอล โค-ไตรม็อกซาโซล และดอกซีไซคลีน การรักษาด้วยสูตรนี้มีอัตราเสียชีวิตถึงร้อยละ 80 และไม่แนะนำให้ใช้สูตรนี้หากมียาชนิดอื่นให้เลือกรักษา[61] ยาทั้งสี่ชนิดเป็นยาปฏิชีวนะชนิดยับยั้งการเจริญของแบคทีเรียแต่ไม่ได้ฆ่าเชื้อแบคทีเรีย นอกจากนี้โค-ไตรม็อกซาโซลยังทำงานต้านกับคลอแรมเฟนิคอลและดอกซีไซคลีนอีกด้วย[84]
พยากรณ์โรค
แก้หากไม่ได้รับการรักษาด้วยยาปฏิชีวนะที่เหมาะสม (โดยหลักแล้วคือเซฟตาซิดิมหรือเมอโรเพเนม) การติดเชื้อเมลิออยด์ในกระแสเลือดมีอัตราการเสียชีวิตสูงมากกว่าร้อยละ 90[85][86] แต่หากได้รับยาปฏิชีวนะที่เหมาะสม อัตราการเสียชีวิตในผู้ป่วยที่ไม่มีภาวะแทรกซ้อนอยู่ที่ประมาณร้อยละ 10 แต่หากผู้ป่วยมีภาวะแบคทีเรียในกระแสเลือดหรือภาวะพิษเหตุติดเชื้อรุนแรงมีอัตราเสียชีวิตถึงร้อยละ 80 การเข้าถึงการดูแลรักษาอภิบาลมีความสำคัญซึ่งอาจอธิบายสาเหตุที่อัตราเสียชีวิตรวมในตอนเหนือของออสเตรเลียอยู่ที่ร้อยละ 20 แต่อัตราเสียชีวิตในภาคอีสานของไทยอยู่ที่ร้อยละ 40 การตอบสนองของผู้ป่วยต่อยาปฏิชีวนะเป็นไปอย่างช้าโดยมีระยะเวลาเฉลี่ยของไข้ภายหลังจากการรักษาที่ 5-9 วัน[15][87]
การกลับเป็นซ้ำอยู่ร้อยละ 10 ถึง 20 ของผู้ป่วยทั้งหมด การศึกษาทางโมเลกุลพบว่าการกลับเป็นโรคซ้ำส่วนใหญ่ขึ้นกับสายพันธุ์ของเชื้อที่ติดในตอนแรก แต่อัตราการกลับเป็นโรคส่วนใหญ่ (มากถึงสามในสี่) ในบริเวณที่โรคเมลิออยด์เป็นโรคประจำถิ่นเกิดจากการติดเชื้อซ้ำภายหลัง 2 ปี[88] ปัจจัยเสี่ยงของการกลับเป็นซ้ำขึ้นกับความรุนแรงของโรค (ผู้ป่วยที่ผลเพาะเชื้อเป็นบวกหรือมีโรคหลายตำแหน่งจะมีอัตราการกลับเป็นซ้ำสูงกว่า) ยาปฏิชีวนะที่ใช้รักษาเพื่อกำจัดเชื้อ (โดยการใช้ยาดอกซีไซคลินเพียงชนิดเดียวหรือยากลุ่มฟลูออโรควิโนโลนไม่มีประสิทธิผลเพียงพอ) ความร่วมมือของผู้ป่วยในการรักษากำจัดเชื้อต่ำ และระยะเวลาในการรักษาเพื่อกำจัดเชื้อน้อยกว่า 8 สัปดาห์ทำให้มีโอกาสกลับเป็นซ้ำได้สูง[80][89]
การป้องกัน
แก้พบว่ามีรายงานน้อยมากเกี่ยวกับการติดต่อระหว่างคนสู่คน ผู้ป่วยโรคเมลิออยด์จึงไม่จัดว่าแพร่กระจายเชื้อได้ง่าย สำหรับผู้ทำงานในห้องปฏิบัติการควรถือว่าตัวอย่างเชื้อ Burkholderia pseudomallei ภายใต้ระดับความปลอดภัยทางชีวภาพที่ระดับ 3 (BSL-3) [90] หลังจากการได้รับเชื้อในห้องปฏิบัติการ แนะนำให้ใช้โค-ไตรม็อกซาโซล (cotrimoxazole) ในการป้องกันโรคหลังได้รับเชื้อแม้ว่าจะยังไม่มีการทดลองทางคลินิก[91]
ในพื้นที่ที่โรคเมลิออยด์เป็นโรคประจำถิ่น เกษตรกรที่ทำนาควรหลีกเลี่ยงการสัมผัสกับดิน โคลน หรือแหล่งน้ำหากเป็นไปได้ พบว่ามีผู้ป่วยจำนวนมากตามหลังเหตุการณ์น้ำท่วมและพายุไซโคลน และเชื่อว่าเกี่ยวข้องกับการสัมผัสดินหรือน้ำที่ปนเปื้อน นอกจากนี้มีผู้ป่วยกลุ่มหนึ่งที่สัมพันธ์กับการบริโภคน้ำที่ปนเปื้อน ประชากรกลุ่มเสี่ยงของโรคเมลิออยด์ได้แก่ผู้ป่วยเบาหวาน โรคไตเรื้อรัง โรคปอดเรื้อรัง หรือผู้ป่วยภูมิคุ้มกันบกพร่องชนิดใดก็ตาม ยังไม่มีการศึกษาถึงประสิทธิผลของการหลีกเลี่ยงการสัมผัสจุลชีพก่อโรค และยังไม่มีวัคซีนในการป้องกันโรคนี้
การป้องกันโรคหลังการสัมผัสเชื้อ
แก้หลังจากการสัมผัสเชื้อแบคทีเรีย B. pseudomallei ซึ่งมักเกิดจากอุบัติเหตุในห้องปฏิบัติการ แนะนำให้รักษาด้วยโค-ไตรม็อกซาโซลร่วมกับดอกซีไซคลีน[92][93] โทรวาฟลอกซาซิน (trovafloxacin) และเกรพพาฟลอกซาซิน (grepafloxacin) มีประสิทธิภาพในการป้องกันจากการทดลองในสัตว์[94]
การใช้เป็นอาวุธชีวภาพ
แก้โรคเมลิออยด์ได้รับความสนใจมากขึ้นเนื่องจากมีประสิทธิภาพในการพัฒนาเป็นอาวุธชีวภาพได้ ศูนย์ควบคุมและป้องกันโรค สหรัฐอเมริกา (Centers for Disease Control) หรือ CDC จัดให้เชื้อโรคเมลิออยด์เป็นอาวุธชีวภาพหมวด B[95] สหรัฐอเมริกาได้เคยทำการศึกษาเชื้อ B. pseudomallei รวมทั้ง B. mallei ซึ่งก่อโรคแกลนเดอร์ส (Glanders) ถึงประสิทธิภาพในการทำอาวุธชีวภาพ แต่ไม่เคยถูกใช้ทำเป็นอาวุธจริง[96] เคยมีรายงานว่าสหภาพโซเวียตเคยทดลองเชื้อ B. pseudomallei เพื่อใช้เป็นอาวุธชีวภาพเช่นกัน
อ้างอิง
แก้- ↑ "ความรู้เรื่องโรคเมลิออยด์ (Melioidosis หรือ เมลิออยโดสิส)" (PDF). Mahidol Oxford Tropical Medicine Research Unit. 2016.
- ↑ "melioidosis". Encyclopædia Britannica.
- ↑ 3.00 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 Wiersinga WJ, Virk HS, Torres AG, Currie BJ, Peacock SJ, Dance DA, Limmathurotsakul D (กุมภาพันธ์ 2018). "Melioidosis". Nature Reviews. Disease Primers. 4: 17107. doi:10.1038/nrdp.2017.107. PMC 6456913. PMID 29388572.
- ↑ Foong YC, Tan M, Bradbury RS (30 ตุลาคม 2014). "Melioidosis: a review". Rural and Remote Health. 14 (4): 2763. doi:10.22605/RRH2763. PMID 25359677.
- ↑ ศัพท์บัญญัติราชบัณฑิตยสถาน เก็บถาวร 15 กรกฎาคม 2017 ที่ เวย์แบ็กแมชชีน ข้อมูลปรับปรุงวันที่ 6 สิงหาคม พ.ศ. 2544 เรียกดูเมื่อ 29 มีนาคม พ.ศ. 2554
- ↑ บัญชีจำแนกโรคระหว่างประเทศ ฉบับประเทศไทย (อังกฤษ-ไทย) ฉบับปี 2009. สำนักนโยบายและยุทธศาสตร์ สำนักงานปลัดกระทรวงสาธารณสุข, 2552.
- ↑ Stanton AT; Fletcher W (1921). "Melioidosis, a new disease of the tropics". Far Eastern Association of Tropical Medicine: Transactions of the Fourth Congress. Batavia, Dutch East Indies: Javasche Boekhandel en Drukkerij.
- ↑ V Vuddhakul; Tharavichitkul P; และคณะ (1999). "Epidemiology of Burkholderia pseudomallei in Thailand". Am J Trop Med Hyg. 60 (3): 458–461.
- ↑ Wuthiekanun V; Mayxay M; Chierakul W; Phetsouvanh R; Cheng AC; White NJ; Day NP; Peacock SJ (2005). "Detection of Burkholderia pseudomallei in soil within the Lao People's Democratic Republic". J Clin Microbiol. 43 (2): 923–4. PMID 15695707.
- ↑ Rattanavong S; Wuthiekanun V; Langla S; Amornchai P; Sirisouk J; Phetsouvanh R; Moore CE; Peacock SJ; Buisson Y; Newton PN (2010). "A randomized soil survey of the distribution of Burkholderia pseudomallei in rice fields in Laos". Appl Environ Microbiol. doi:10.1128/AEM.01822-10. PMID 21075883.
- ↑ Yang S (2000). "Melioidosis research in China". Acta Tropica. 77 (2): 157–165. doi:10.1016/s0001-706x(00)00139-x. PMID 11080506.
- ↑ 12.0 12.1 Lo TJ; Ang LW; James L; Goh KT (2009). "Melioidosis in a tropical city state, Singapore". Emerg Infect Dis. 15 (10): 1645–7. PMC 2866399. PMID 19861063.
- ↑ Ko WC; Cheung, BM; Tang, HJ; Shih, HI; Lau, YJ; Wang, LR; Chuang, YC (2007). "Melioidosis outbreak after typhoon, southern Taiwan". Emerg Infect Dis. 13 (6): 896–8. PMC 2792857. PMID 17553230.
- ↑ Chen YS; Lin HH; Mu JJ; Chiang CS; Chen CH; Buu LM; Lin YE; Chen YL (2010). "Distribution of melioidosis cases and viable Burkholderia pseudomallei in soil: Evidence for emerging melioidosis in Taiwan". J Clin Microbiol. 48 (4): 1432–4. doi:10.1128/JCM.01720-09. PMC 2849618. PMID 20147639.
- ↑ 15.0 15.1 15.2 White NJ (2003). "Melioidosis". Lancet. 361 (9370): 1715–22. doi:10.1016/S0140-6736(03)13374-0. PMID 12767750.
- ↑ Cheng AC; Currie BJ (2005). "Melioidosis: epidemiology, pathophysiology, and management". Clin Microbiol Rev. 18 (2): 383–416. doi:10.1128/CMR.18.2.383-416.2005. PMC 1082802. PMID 15831829.
- ↑ Chong VH (2010). "Changing spectrum of microbiology of liver abscess: Now Klebsiella, next Burkholderia pseudomallei". J Emerg Med. doi:10.1016/j.jemermed.2009.10.027. PMID 20079999.
- ↑ Chugh TD (2008). "Emerging and re-emerging bacterial diseases in India". J Biosci. 33 (4): 549–55. doi:10.1007/s12038-008-0073-0. PMID 19208980.
- ↑ Antony B; Pinto H; Dias M; Shetty AK; Scaria B; Kuruvilla T; Boloor R (2010). "Spectrum of melioidosis in the suburbs of Mangalore, S West Coast of India". Southeast Asian J Trop Med Public Health. 41 (1): 169–74.
- ↑ Vidyalakshmi K; Chakrapani M; Shrikala B; Damodar S; Lipika S; Vishal S (2008). "Tuberculosis mimicked by melioidosis". Int J Tuberc Lung Dis. 12 (10): 1209–15.
- ↑ Inglis TJ; Rolim DB; De Queroz Sousa A (2006). "Melioidosis in the Americas". Am J Trop Me Hyg. 75 (5): 947–954. PMID 17123994.
- ↑ Struelens MJ; Mondol G; Bennish M; Dance DAB (1998). "Melioidosis in Bangladesh: a case report". Trans R Soc Trop Med Hygiene. 82: 777–78. doi:10.1016/0035-9203(88)90234-9.
- ↑ Dance DAB; Smith MD; Aucken HM; Pitt TL (1999). "Imported melioidosis in England and Wales". Lancet. 353: 208. doi:10.1016/S0140-6736(05)77217-2. PMID 9923882.
- ↑ Limmathurotsakul D; Wongratanacheewin S; Teerawattanasook N (2010). "Increasing incidence of human melioidosis in Northeast Thailand". Am J Trop Med Hyg. 82 (6): 1113-7. PMID 20519609.
- ↑ Kanaphun P; Thirawattanasuk N; และคณะ (1993). "Serology and carriage of Pseudomonas pseudomallei: a prospective study in 1000 hospitalized children in northeast Thailand". J infect Dis. 167: 230–3. PMID 7678106.
- ↑ Vuddhakul V; Tharavichitkul P; และคณะ (March 1999). "Epidemiology of Burkholderia pseudomallei in Thailand". Am. J. Trop. Med. Hyg. 60 (3): 458–61. PMID 10466977.
- ↑ Kanai K; Dejsirilert S (August 1988). "Pseudomonas pseudomallei and melioidosis, with special reference to the status in Thailand". Jpn. J. Med. Sci. Biol. 41 (4): 123–57. doi:10.7883/yoken1952.41.123. PMID 3075004.
- ↑ Yang S; Tong S; และคณะ (1998). "Prevalence of human melioidosis on Hainan Island in China". Microbiol. Immunol. 42 (9): 651–4. doi:10.1111/j.1348-0421.1998.tb02335.x. PMID 9802565.
- ↑ Chen YS; Chen SC; Wu TR; Kao CM; Chen YL (October 2004). "Seroprevalence of anti-flagellin antibody against Burkholderia pseudomallei in Taiwan". Jpn. J. Infect. Dis. 57 (5): 224–5. PMID 15507783. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2008-06-19. สืบค้นเมื่อ 2011-03-28.
- ↑ Parkes, Helen M.; Shilton, Catherine M.; Jerrett, Ian V.; Benedict, Suresh; Spratt, Brian G.; Godoy, Daniel; O'Brien, Carolyn R.; Krockenberger, Mark B.; Mayo, Mark. (2009). "Primary ocular melioidosis due to a single genotype of Burkholderia pseudomallei in two cats from Arnhem Land in the Northern Territory of Australia". J Feline Med Surg. 11 (10): 856–63. doi:10.1016/j.jfms.2009.02.009. PMID 19428280.
- ↑ Sprague LD; Neubauer H (2004). "Melioidosis in Animals: A review on epizootiology, diagnosis and clinical presentation". J Vet Med B. 51 (7): 305–20. doi:10.1111/j.1439-0450.2004.00797.x. PMID 15525357.
- ↑ Mollaret HH (1988). "«L'affaire du Jardin des plantes» ou comment le mélioïdose fit son apparition en France". Médecine et maladies infectieuses. 18 (Suppl 4): 643–54. doi:10.1016/S0399-077X(88)80175-6.
- ↑ Corkeron ML; Norton R; Nelson PN (2010). "Spatial analysis of melioidosis distribution in a suburban area". Epidemiol Infect. 22 (9): 1–7. doi:10.1017/S0950268809991634. PMID 20092666.
- ↑ Chantratita N; Wuthiekanun V; และคณะ (2008). "Genetic diversity and microevolution of Burkholderia pseudomallei in the environment". PLoS Negl Trop Dis. 2008. 2 (2): e182. doi:10.1371/journal.pntd.0000182. PMC 2254201. PMID 18299706.
- ↑ Inglis TJ; Garrow SC; Henderson M; Clair A; Sampson J; O'Reilly L; Cameron B (2000). "Burkholderia pseudomallei traced to water treatment plant in Australia". Emerg Infect Dis. 6 (1): 56–59. PMC 2627980. PMID 10653571.
- ↑ Suputtamongkol Y; Chaowagul W; และคณะ (1999). "Risk factors for melioiosis and bacteremic melioidosis". Clin Infect Dis. 29 (2): 408–13. doi:10.1086/520223. PMID 10476750.
- ↑ McCormick J B (1975). "Human-to-human transmission of Pseudomonas pseudomallei". Ann Int Med. 83 (4): 512–513.
- ↑ Holland DJ; Wesley A; Drinkovic D; Currie BJ (2002). "Cystic fibrosis and Burkholderia pseudomallei infection: an emerging problem?". Clin Infect Dis. 35 (12): e138-40. PMID 12471591.
- ↑ Suputtamongkol Y; Hall AJ; และคณะ (1994). "The epidemiology of melioidosis in Ubon Ratchatani, Northeast Thailand". Int J Epidemiol. 23 (5): 1082–89. doi:10.1093/ije/23.5.1082. PMID 7860160.
- ↑ Currie BJ; Jacups SP (December 2003). "Intensity of rainfall and severity of melioidosis, Australia". Emerging Infect. Dis. 9 (12): 1538–42. doi:10.3201/eid0912.020750. PMID 14720392.
- ↑ Liu Y; Loh JP; Aw LT; Yap EPH; Lee MA; Ooi EE (2006). "Rapid molecular typing of Burkholderia pseudomallei, isolated in an outbreak of melioidosis in Singapore in 2004, based on variable-number tandem repeats". Trans Roy Soc Trop Med Hyg. 100 (7): 687–92. doi:10.1016/j.trstmh.2005.08.017. PMID 16343569.
- ↑ Sam I-C; Puthucheary SD (2007). "Melioidosis and rainfall in Kuala Lumpur, Malaysia". J Infect. 54 (5): 519–20. doi:10.1016/j.jinf.2006.07.007. PMID 16965821.
- ↑ 43.0 43.1 43.2 A J Simpson; Suputtamongkol Y; และคณะ (1999). "Comparison of imipenem and ceftazidime as therapy for severe melioidosis". Clin Infect Dis. 29 (2): 381–387. doi:10.1086/520219. PMID 10476746.
- ↑ Ngauy V; Lemeshev Y; Sadkowski L; Crawford G (2005). "Cutaneous melioidosis in a man who was taken as a prisoner of war by the Japanese during World War II". J Clin Microb. 43 (2): 970–2. doi:10.1128/JCM.43.2.970-972.2005. PMC 548040. PMID 15695721.
- ↑ Apisarnthanarak A; Apisarnthanarak P; Mundy LM (2006). "Computer tomography characteristics of Burkholderia pseudomallei liver abscess". Clin Infect Dis. 42 (7): 989–93. doi:10.1086/501017. PMID 16511765.
- ↑ Laopaiboon V; Chamadol N; Buttham H; Sukeepaisarnjareon W (2009). "CT findings of liver and splenic abscesses in melioidosis: comparison with those in non-melioidosis". J Med Assoc Thai. 92 (11): 1476–84. PMID 19938740.
- ↑ Dance DA; Davis TM; และคณะ (1989). "Acute suppurative parotitis caused by Pseudomonas pseudomallei in children". J Infect Dis. 159 (4): 654–60. PMID 2926159.
- ↑ Raja, NS; Ahmed MZ; Singh NN (1 April 2005). "Melioidosis: an emerging infectious disease". Journal of Postgraduate Medicine. 51 (2): 140–45. PMID 16006713.
- ↑ Chlebicki, MP; Tan BH (2006). "Six cases of suppurative lymphadenitis caused by Burkholderia pseudomallei infection". Trans R Soc Trop Med Hyg. 100 (8): 798–801. doi:10.1016/j.trstmh.2005.10.004. PMID 16542691.
- ↑ Currie BJ; Fisher DA; และคณะ (2000). "Endemic melioidosis in tropical northern Australia: a 10-year prospective study and review of the literature". Clin Infect Dis. 31 (4): 981–986. PMID 11049780.
- ↑ 51.0 51.1 Falade OO; Antonarakis ES; Kaul DR; Saint S; Murphy PA (2008). "Clinical problem-solving. Beware of first impressions". N Engl J Med. 359 (6): 628–634. doi:10.1056/NEJMcps0708803. PMID 18687644.
- ↑ Chetchotisakd, P; Anunnatsiri, S; Kiatchoosakun, S; Kularbkaew, C (2010). "Melioidosis pericarditis mimicking tuberculous pericarditis". Clin Infect Dis. 51 (5): e46–9. doi:10.1086/655699. PMID 20645861.
- ↑ Ngauy V; Lemeshev Y; Sadkowski L; Crawford G (2005). "Cutaneous melioidosis in a man who was taken as a prisoner of war by the Japanese during World War II". J Clin Microbiol. 43 (2): 970–972. doi:10.1128/JCM.43.2.970-972.2005. PMC 548040. PMID 15695721.
- ↑ Wuthiekanun V; Suputtamongkol Y; Simpson AJH; Kanaphun P; White NJ (2001). "Value of throat swab in the diagnosis of melioidosis". J Clin Microbiol. 39 (10): 3801–02. doi:10.1128/JCM.39.10.3801-3802.2001. PMC 88440. PMID 11574624.
- ↑ Limmathurotsakul D; Wuthiekanun V; และคณะ (2005). "Role and significance of quantitative urine cultures in diagnosis of melioidosis". J Clin Microb. 43 (5): 2274–76. doi:10.1128/JCM.43.5.2274-2276.2005. PMC 1153798. PMID 15872255.
- ↑ Dance DA; White NJ; Suputtamongkol Y; Wattanagoon Y; Wuthiekanun V; Chaowagul W (1990). "The use of bone marrow culture for the diagnosis of melioidosis". Trans R Soc Trop Med Hyg. 84 (4): 585–7. doi:10.1016/0035-9203(90)90050-O. PMID 2091358.
- ↑ Francis A; Aiyar S; Yean C; Naing L; Ravichandran M (2006). "An improved selective and differential medium for the isolation of Burkholderia pseudomallei from clinical specimens". Diagn Microbiol Infect Dis. 55 (2): 95–99. doi:10.1016/j.diagmicrobio.2005.11.008. PMID 16626918.
- ↑ Puthucheary SD; Anuar AS; Tee TS (2010). "Burkholderia thailandensis whole cell antigen cross-reacts with B. pseudomallei antibodies from patients with melioidosis in an immunofluorescent assay". The Southeast Asian journal of tropical medicine and public health. 41 (2): 397–400. PMID 20578523.
- ↑ 59.0 59.1 Lim KS, Chong VH (2010). "Radiological manifestations of melioidosis". Clin Radiol. 65 (1): 66–72. doi:10.1016/j.crad.2009.08.008. PMID 20103424.
- ↑ 60.0 60.1 Muttarak M; Peh WC; Euathrongchit J; Lin SE; Tan AG; Lerttumnongtum P; Sivasomboon C (2008). "Spectrum of imaging findings in melioidosis". Br J Radiol. 82 (978): 514–21. doi:10.1259/bjr/15785231. PMID 19098086.
- ↑ 61.0 61.1 White NJ; Dance DA; และคณะ (1989). "Halving of mortality of severe melioidosis by ceftazidime". Lancet. 2 (8665): 697–701. doi:10.1016/S0140-6736(89)90768-X. PMID 2570956.
- ↑ Chierakul W; Anunnatsiri S; และคณะ (2007). "Addition of trimethoprim-sulfamethoxazole to ceftazidime during parenteral treatment of melioidosis is not associated with a long-term outcome benefit". Clin infect Dis. 45 (4): 521–523. doi:10.1086/520010. PMID 17638209.
- ↑ Cheng AC; Fisher DA; และคณะ (2004). "Outcomes of patients with melioidosis treated with meropenem". Antimicrob Agents Chemother. 48 (5): 1763–65. doi:10.1128/AAC.48.5.1763-1765.2004. PMC 400582. PMID 15105132.
- ↑ Chetchotisakd P; Porramatikul S; Mootsikapun P; Anunnatsiri S; Thinkhamrop B (2001). "Randomized, double-blind, controlled study of cefoperazone-sulbactam plus cotrimoxazole versus ceftazidime plus cotrimoxazole for the treatment of severe melioidosis". Clin Infect Dis. 33 (1): 29–3. doi:10.1086/320878. PMID 11389491.
- ↑ Dance DA; Wuthiekanun V; White NJ; Chaowagul W (1988). "Antibiotic resistance in Pseudomonas pseudomallei". Lancet. 1 (8592): 994–5. doi:10.1016/S0140-6736(88)91810-7. PMID 2896855.
- ↑ Suputtamongkol Y; Rajchanuwong A; และคณะ (1994). "Ceftazidime vs. amoxicillin/clavulanate in the treatment of severe melioidosis". Clin Infect Dis. 19: 846–53. PMID 7893868.
- ↑ 67.0 67.1 Currie BJ; Fisher DA; และคณะ (2000). "Endemic melioidosis in tropical Northern Australia: a 10-year prospective study and review of the literature". Clin Infect Dis. 31: 981–86. doi:10.1086/318116. PMID 11049266.
- ↑ University of Oxford (18 December 2007). "A randomized double blinded comparison of ceftazidime and meropenem in severe melioidosis (ATOM)". ClinicalTrials.gov. National Institutes of Health. สืบค้นเมื่อ 27 Jan 2011.
- ↑ Simpson, A. J. H.; Opal, S. M.; Angus, B. J.; Prins, J. M.; Palardy, J. E.; Parejo, N. A.; Chaowagul, W.; White, N. J. (2000). "Differential antibiotic-induced endotoxin release in severe melioidosis". J Infect Dis. 181 (3): 1014–9. doi:10.1086/315306. PMID 10720525.
- ↑ I Bilgrami; J A Roberts; S C Wallis; J Thomas; J Davis; S Fowler; P B Goldrick; J Lipman (July 2010). "Meropenem Dosing in Critically Ill Patients With Sepsis Receiving High-Volume Continuous Venovenous Hemofiltration". Antimicrobial Agents and Chemotherapy. 54 (7): 2974–8. doi:10.1128/AAC.01582-09. PMID 20479205.
- ↑ 71.0 71.1 Shih H-I; Chuang Y-C; และคณะ (February 2008). "Sporadic and outbreak cases of melioidosis in southern Taiwan: clinical features and antimicrobial susceptibility". Infection. 37 (1): 9–15. doi:10.1007/s15010-008-7324-8. PMID 18854938.
- ↑ Thamlikitkul V; Trakulsomboon S (2010). "In vitro activity of biapenem against Burkholderia pseudomallei". International journal of antimicrobial agents. 35 (5): 514. doi:10.1016/j.ijantimicag.2010.01.002. PMID 20188524.
- ↑ Cheng AC; Limmathurotsakul D; และคณะ (2007). "A randomized controlled trial of granulocyte colony-stimulating factor for the treatment of severe sepsis due to melioidosis in Thailand". Clin Infect Dis. 45 (3): 308–14. doi:10.1086/519261. PMID 17599307.
- ↑ Chierakul W; Anunnatsiri S; และคณะ (2005). "Two randomized controlled trials of ceftazidime alone versus ceftazidime in combination with trimethoprim-sulfamethoxazole for the treatment of severe melioidosis". Clin Infect Dis. 41 (8): 1105–13. doi:10.1086/444456. PMID 16163628.
- ↑ Chierakul W; Anunnatsiri S; Chaowagul W; Peacock SJ; Chetchotisakd P; Day NP (2007). "Addition of trimethoprim-sulfamethoxazole to ceftazidime during parenteral treatment of melioidosis is not associated with a tong-term outcome benefit". Clin Infect Dis. 45 (4): 521–3. doi:10.1086/520010. PMID 17638209.
- ↑ Chaowagul W; Simpson AJ; และคณะ (1999). "A comparison of chloramphenicol, trimethoprim-sulfamethoxazole, and doxycycline with doxycycline alone as maintenance therapy for melioidosis". Clin Infect Dis. 29 (2): 375–80. doi:10.1086/520218. PMID 10476745.
- ↑ Rajchanuvong A; Chaowagul W; Suputtamongkol Y; Smith MD; Dance DA; White NJ (1995). "A prospective comparison of co-amoxiclav and the combination of chloramphenicol, doxycycline, and co-trimoxazole for the oral maintenance treatment of melioidosis". Trans R Soc Trop Med Hyg. 89 (5): 546–9. doi:10.1016/0035-9203(95)90104-3. PMID 8560537.
- ↑ Cheng AC; Chierakul W; และคณะ (2008). "Consensus guidelines for dosing of amoxicillin-clavulanate in melioidosis". Am J Trop Med Hyg. 78 (2): 208–9. PMID 18256414.
- ↑ Chaowagul W; Supputtamongkul Y; Smith MD; White NJ (1997). "Oral fluoroquinolones for maintenance treatment of melioidosis". Trans R Soc Trop Med Hyg. 91: 599–601. doi:10.1016/S0035-9203(97)90044-4.
- ↑ 80.0 80.1 Limmathurotsakul D; Chaowagul W; และคณะ (2006). "Risk factors for recurrent melioidosis in Northeastern Thailand". Clin Infect Dis. 43 (8): 979–86. doi:10.1086/507632. PMID 16983608.
- ↑ Dance DA; Wuthiekanun V; Chaowagul W; White NJ (1989). "Interactions in vitro between agents used to treat melioidosis". J Antimicrob Chemother. 24 (3): 311–6. doi:10.1093/jac/24.3.311. PMID 2681117.
- ↑ Cheng AC; McBryde ES; Wuthiekanun V; Chierakul W; Amornchai P; Day NPJ; Peacock SJ (2009). "Dosing regimens of cotrimoxazole (trimethoprim-sulfamethoxazole) for melioidosis". Antimicrob Agents Chemother. 53 (10): 4193–9. doi:10.1128/AAC.01301-08. PMC 2764189. PMID 19620336.
- ↑ TJ Inglis; CL Golledge; A Clair; J Harvey (2001). "Case report: recovery from persistent septicemic melioidosis". Am J Trop Med Hyg. 65 (1): 76–82. PMID 11504412.
- ↑ Dance DA; Wuthiekanun V; Chaowagul W; White NJ (1989). "Interactions in vitro between agents used to treat melioidosis". J Antimicrob Chemother. 24 (3): 311–6. doi:10.1093/jac/24.3.311. PMID 2681117.
- ↑ Couture E (1935),Rev Hyg Méd prèv, 57: 190
- ↑ Warner JM; Pelowa DB; Currie BJ; Hirst RG (2007). "Melioidosis in a rural community of Western Province, Papua New Guinea". Trans R Soc Trop Med Hyg. 101 (8): 809–13. doi:10.1016/j.trstmh.2007.02.024. PMID 17499321.
- ↑ Chaowagul W; White NJ; และคณะ (1989). "Melioidosis: a major cause of community-acquired septicemia in northeastern Thailand". J Infect Dis. 159 (5): 890–9. PMID 2708842.
- ↑ Maharjan B; Chantratita N; และคณะ (2005). "Recurrent melioidosis in patients in northeast Thailand is frequently due to reinfection rather than relapse". J Clin Microbiol. 43 (12): 6032–4. doi:10.1128/JCM.43.12.6032-6034.2005. PMC 1317219. PMID 16333094.
- ↑ Chaowagul W; Suputtamongkol Y; Dance DA; Rajchanuvong A; Pattara-arechachai J; White NJ (1993). "Relapse in melioidosis: incidence and risk factors". J Infect Dis. 168 (5): 1181–85. PMID 8228352.
- ↑ Centers for Disease Control and Prevetion (2009). Biosafety in Microbiological and Biomedical Laboratories (PDF) (5th ed.). Atlanta, Georgia: National Institutes of Health.
- ↑ Peacock SJ; Schweizer HP; และคณะ (2008). "Management of accidental laboratory exposure to Burkholderia pseudomallei and B. mallei". Emerg Infect Dis. 14 (7): e2. doi:10.3201/eid1407.071501. PMID 18598617.
- ↑ Sivalingam SP; Sim SH; และคณะ (2008). "Pre- and post-exposure prophylaxis of experimental Burkholderia pseudomallei infection with doxycycline, amoxicillin/clavulanic acid and co-trimoxazole". J Antimicrob Chemother. 61 (3): 674–8. doi:10.1093/jac/dkm527. PMID 18192684.
- ↑ Peacock SJ; Schweizer HP; และคณะ (2008). "Management of accidental laboratory exposure to Burkholderia pseudomallei and B.-mallei". Emerg Infect Dis. 14 (7): e2. doi:10.3201/eid1407.071501. PMC 2600349. PMID 18598617.
- ↑ Kenny DJ; Sefton AM; Brooks TJ; Laws TR; Simpson AJ; Atkins HS (2010). "Evaluation of azithromycin, trovafloxacin and grepafloxacin as prophylaxis for experimental murine melioidosis". Int J Antimicrob Agents. 36 (1): 87–9. doi:10.1016/j.ijantimicag.2010.03.019. PMID 20462743.
- ↑ ศูนย์ควบคุมและป้องกันโรค สหรัฐอเมริกา. melioidosis
- ↑ Woods JB, บ.ก. (2005). USAMRIID's Medical Management of Biological Casualties Handbook (PDF) (6th ed.). Fort Detrick, Maryland: U.S. Army Medical Institute of Infectious Diseases. p. 67. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 9 มิถุนายน 2007. สืบค้นเมื่อ 4 เมษายน 2011.
แหล่งข้อมูลอื่น
แก้- Melioidosis ที่ WikiJournal of Medicine
- "เมลิออยด์ โรคติดเชื้อที่คนไทยต้องรู้" ที่เฟซบุ๊ก
- Raising awareness of Melioidosis ความรู้เกี่ยวกับโรคเมลิออยด์โดย หน่วยวิจัยโรคเขตร้อนมหิดล-อ๊อกซ์ฟอร์ด
- Melioidosis ข้อมูลจากศูนย์ควบคุมและป้องกันโรค สหรัฐอเมริกา
- Virginia Tech pathogen database - Burkholderia pseudomallei เก็บถาวร 1 กันยายน 2006 ที่ เวย์แบ็กแมชชีน
- Center for Biosecurity Agent Fact Sheet เก็บถาวร 31 พฤษภาคม 2009 ที่ เวย์แบ็กแมชชีน
- Burkholderia pseudomallei เก็บถาวร 24 สิงหาคม 2011 ที่ เวย์แบ็กแมชชีน จีโนมและข้อมูลที่เกี่ยวข้องที่ PATRIC, ศูนย์ทรัพยากรชีวสารสนเทศ สนับสนุนโดย NIAID
| การจำแนกโรค | |
|---|---|
| ทรัพยากรภายนอก |