ฟลูออรีน (พีเอเอช)
สำหรับความหมายอื่นดู ฟลูออรีน
| |

| |

| |
| ชื่อ | |
|---|---|
| Preferred IUPAC name
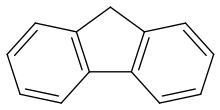
9H-Fluorene[2] | |
| Systematic IUPAC name
Tricyclo[7.4.0.02,7]trideca-2,4,6,9,11,13-hexaene | |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| เคมสไปเดอร์ | |
| ECHA InfoCard | 100.001.541 |
| EC Number |
|
| KEGG | |
ผับเคม CID
|
|
| RTECS number |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| C13H10 | |
| มวลโมเลกุล | 166.223 g·mol−1 |
| ความหนาแน่น | 1.202 g/mL |
| จุดหลอมเหลว | 116 ถึง 117 องศาเซลเซียส (241 ถึง 243 องศาฟาเรนไฮต์; 389 ถึง 390 เคลวิน) |
| จุดเดือด | 295 องศาเซลเซียส (563 องศาฟาเรนไฮต์; 568 เคลวิน) |
| 1.992 mg/L | |
| ความสามารถละลายได้ | organic solvents |
| log P | 4.18 |
| pKa | 22.6 |
| -110.5·10−6 cm3/mol | |
| ความอันตราย | |
| NFPA 704 (fire diamond) | |
| จุดวาบไฟ | 152 องศาเซลเซียส (306 องศาฟาเรนไฮต์; 425 เคลวิน) |
| ปริมาณหรือความเข้มข้น (LD, LC): | |
LD50 (median dose)
|
16000 mg/kg (oral, rat) |
| เอกสารข้อมูลความปลอดภัย (SDS) | Sigma-Aldrich |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
ฟลูออรีนหรือ 9H-Fluorene เป็นสารประกอบโพลีไซคลิกอะโรมาติกไฮโดรคาร์บอน ลักษณะเป็นผลึกสีขาว ระเหิดได้เช่นเดียวกับแนฟทาลีน เรืองแสงสีม่วงใต้แสงยูวี ไม่ละลายในน้ำแต่ละลายได้ในเบนซีน และอีเทอร์
การสังเคราะห์ โครงสร้างและปฏิกิริยา
แก้แหล่งที่มาสำคัญของฟลูออรีนคือน้ำมันถ่านหิน แต่สามารถสังเคราะห์ได้ด้วยปฏิกิริยาดีไฮโดรจีเนสของไดฟีนิลมีเทน[3] โมเลกุลของฟลูออรีน มีลักษณะเกือบเป็นแนวระนาบ ,[4] แม้ว่าแต่ละวงเบนซีนที่อยู่ด้านข้างมีลักษณะเป็นระนาบร่วมกับคาร์บอนตัวที่ 9 ที่อยู่ตรงกลาง [5]
ความเป็นกรด
แก้ตำแหน่ง C9-H ของวงแหวนของฟลูออรีนเป็นกรดอย่างอ่อน (pKa = 22.6 ใน DMSO)[6] การเสียโปรตรอนทำให้ได้แอนไอออนฟลูออรีนิลที่เสถียร มีสูตรโครงสร้างเป็น C13H9 -, ซึ่งมีกลิ่นหอมและมีสีส้มเข้ม แอนไอออนนี้มีคุณสมบัติเป็นนิวคลีโอไฟล์ และทำปฏิกิริยากับอิเล็กโตรไฟล์ได้โดยปฏิกิริยาการเติมที่ตำแหน่งที่ 9 การทำฟลูออรีนให้บริสุทธิ์ใช้คุณสมบัติความเป็นกรดและการที่อนุพันธ์โซเดียมของฟลูออรีนละลายในตัวทำละลายไฮโดรคาร์บอนได้ต่ำ
สามารถทำให้ฟลูออรีนเสียโปรตอนทั้งสองที่ตำแหน่ง C9 ได้ ตัวอย่างเช่น 9,9 - ฟลูออรีนิลไดโพแทสเซียม สามารถสังเคราะห์ได้โดยให้ฟลูออรีนทำปฏิกิริยากับโลหะโพแทสเซียมในไดออกเซนที่เดือด [7]
การใช้ประโยชน์
แก้ฟลูออรีนเป็นสารตั้งต้นของสารอนุพันธ์ของฟลูออรีนอื่น ๆ กรดฟลูออรีน - 9 - คาร์บอกซิลิก เป็นสารตั้งต้นของการผลิตยา 2 - อะมิโนฟลูออรีน, 3,6 -บิส - (ไดเมทิลอะมิโนฟลูออรีน) และ 2,7 - ไดไอโอโดฟลูออรีน เป็นสารตั้งต้นของการผลิตสีย้อมปฏิกิริยาออกซิเดชันของฟลูออรีนให้ ฟลูออรีโนน ซึ่งเป็นอนุพันธ์ที่มีประโยชน์ในเชิงพาณิชย์ 9 - ฟลูออรีนิลเมทิลคลอโรฟอร์เมต ใช้ในการผลิต 9 - ฟลูออรีนิลเมทิลคาร์บาเมต (Fmoc) ซึ่งเป็นสารป้องกันหมู่เอมีนในการสังเคราะห์เปปไทด์ [3]
พอลิเมอร์ พอลีฟลูออรีน (คาร์บอนตัวที่ 7 ของหน่วยหนึ่งสร้างพันธะกับคาร์บอนตัวที่ 2 ของหน่วยถัดไป โดยแทนที่ไฮโดรเจนสองอะตอม)ใช้เป็นสื่อกระแสไฟฟ้าและสารเรืองแสงทางไฟฟ้า และได้รับการศึกษามากสำหรับใช้เป็น หมู่ให้ความเรืองแสงในไดโอดเปล่งแสงแบบใช้สารอินทรีย์
อ้างอิง
แก้- ↑ Merck Index, 11th Edition, 4081
- ↑ International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. p. 207. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ↑ 3.0 3.1 Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke “Hydrocarbons” in Ullmann's Encyclopedia of Industrial Chemistry 2002 Wiley-VCH, Weinheim. doi:10.1002/14356007.a13_227
- ↑ D. M. Burns, John Iball (1954), Molecular Structure of Fluorene Nature volume 173, p. 635. doi:10.1038/173635a0
- ↑ R. E. Gerkin, A. P. Lundstedt and W. J. Reppart (1984) Structure of fluorene, C13H10, at 159 K Acta Crystallographica, volume C40, pp. 1892–1894 doi:10.1107/S0108270184009963
- ↑ F. G. Bordwell (1988). "Equilibrium acidities in dimethyl sulfoxide solution". Acc. Chem. Res. 21: 456–463. doi:10.1021/ar00156a004.
- ↑ G. W. Scherf and R. K. Brown (1960), POTASSIUM DERIVATIVES OF FLUORENE AS INTERMEDIATES IN THE PREPARATION OF C9-SUBSTITUTED FLUORENES. I. THE PREPARATION OF 9-FLUORENYL POTASSIUM AND THE INFRARED SPECTRA OF FLUORENE AND SOME C9-SUBSTITUTED FLUORENES เก็บถาวร 2012-12-16 ที่ archive.today. Canadian Journal of Chemistry, Vol. 38, p. 697.
แหล่งข้อมูลอื่น
แก้- National Pollutant Inventory - Polycyclic Aromatic Hydrocarbon Fact Sheet เก็บถาวร 2006-05-18 ที่ เวย์แบ็กแมชชีน
- Fluorene in the National Institute of Standards and Technology database.
