กลูตาไธโอน
บทความนี้ยังต้องการเพิ่มแหล่งอ้างอิงเพื่อพิสูจน์ความถูกต้อง |
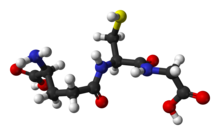
กลูตาไธโอน (อังกฤษ: glutathione, GSH) เป็นสารต้านอนุมูลอิสระที่สำคัญในพืช สัตว์ เห็ดราและแบคทีเรียและอาร์เคียบางชนิด ทำหน้าที่ป้องกันองค์ประกอบสำคัญของเซลล์ที่เกิดจากออกซิเจนที่ไวต่อปฏิกิริยา (reactive oxygen species) เช่น อนุมูลอิสระหรือเปอร์ออกไซด์[2] กลูตาไธโอนประกอบด้วยเพปไทด์สามโมเลกุล (tripeptide) คือ ซีสเตอีน กรดกลูตามิก และไกลซีน มีพันธะเพปไทด์แกมมาระหว่างหมู่คาร์บอกซิลของหมู่ข้างกลูตาเมตและหมู่เอมีนของซิสทีน และพันธะเพปไทด์ธรรมดาระหว่างซีสทีนกับไกลซีน

| |
| |
| ชื่อ | |
|---|---|
| Preferred IUPAC name
(2S)-2-Amino-5-({(2R)-1-[(carboxymethyl)amino]-1-oxo-3-sulfanylpropan-2-yl}amino)-5-oxopentanoic acid | |
| ชื่ออื่น
γ-L-Glutamyl-L-cysteinylglycine
(2S)-2-Amino-4-({(1R)-1-[(carboxymethyl)carbamoyl]-2-sulfanylethyl}carbamoyl)butanoic acid | |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| ตัวย่อ | GSH |
| ChEBI | |
| ChEMBL | |
| เคมสไปเดอร์ | |
| ดรักแบงก์ | |
| ECHA InfoCard | 100.000.660 |
| KEGG | |
| MeSH | Glutathione |
ผับเคม CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| C10H17N3O6S | |
| มวลโมเลกุล | 307.32 g·mol−1 |
| จุดหลอมเหลว | 195 องศาเซลเซียส (383 องศาฟาเรนไฮต์; 468 เคลวิน)[1] |
| ละลายน้ำได้[1] | |
| ความสามารถละลายได้ ใน เมทานอล, ไดเอทิลอีเทอร์ | ละลายไม่ได้[1] |
| เภสัชวิทยา | |
| V03AB32 (WHO) | |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
หมู่ไธออลเป็นตัวรีดิวซ์ ซึ่งมีอยู่ที่ความเข้มข้นประมาณ 5 มิลลิโมลาร์ในเซลล์สัตว์ กลูตาไธโอนรีดิวซ์พันธะไดซัลไฟด์ที่เกิดขึ้นในโปรตีนไซโทพลาสซึมไปยังซีลเตอีนโดยทำหน้าที่เป็นตัวให้อิเล็กตรอน ในกระบวนการนี้ กลูตาไธโอนจะถูกเปลี่ยนเป็นรูปออกซิไดซ์ กลูตาไธโอนไดซัลไฟด์ (GSSG) หรืออีกชื่อหนึ่งว่า แอล-(–)-กลูตาไธโอน
เมื่อถูกออกซิไดซ์แล้ว กลูตาไธโอนสามารถถูกรีดิวซ์กลับได้โดยกลูตาไธออนรีดักเทส (glutathione reductase) โดยอาศัย NADPH เป็นตัวให้อิเล็กตรอน[3] อัตรากลูตาไธโอนรูปรีดิวซ์ต่อกลูตาไธโอนรูปออกซิไดซ์มักใช้เป็นการวัดความเป็นพิษของเซลล์[4]
นอกจากนี้ กลูตาไธโอนช่วยให้ตับขจัดสารพิษออกจากร่างกาย และยังนำมารักษาโรคมะเร็ง โรคหัวใจ ข้ออักเสบ โรคพาร์กินสัน โรคตับ โรคไต โรคเอดส์ ภาวะเป็นหมันในเพศชาย และภาวะหูตึงจากเสียงดัง ผลข้างเคียงยับยั้งการสังเคราะห์เมลานิน
อ้างอิง
แก้- ↑ 1.0 1.1 1.2 1.3 Haynes, William M., บ.ก. (2016). CRC Handbook of Chemistry and Physics (97th ed.). CRC Press. p. 3.284. ISBN 9781498754293.
- ↑ Pompella, A; Visvikis, A; Paolicchi, A; Tata, V; Casini, AF (2003). "The changing faces of glutathione, a cellular protagonist". Biochemical Pharmacology. 66 (8): 1499–503. doi:10.1016/S0006-2952(03)00504-5. PMID 14555227.
- ↑ Couto, Narciso; Malys, Naglis; Gaskell, Simon; Barber, Jill (2013). "Partition and Turnover of Glutathione Reductase from Saccharomyces cerevisiae: a Proteomic Approach". Journal of Proteome Research. 12 (6): 2885–94. doi:10.1021/pr4001948. PMID 23631642.
- ↑ Pastore, Anna; Piemonte, Fiorella; Locatelli, Mattia; Lo Russo, Anna Lo; Gaeta, Laura Maria; Tozzi, Giulia; Federici, Giorgio (2003). "Determination of blood total, reduced, and oxidized glutathione in pediatric subjects". Clinical Chemistry. 47 (8): 1467–9. PMID 11468240.