การม้วนพับโปรตีน
การม้วนพับโปรตีน เป็นกระบวนการทางกายภาพที่สายโปรตีนกลายสภาพเป็นโครงสร้างสามมิติ อันเป็นรูปแบบที่เกิดขึ้นอย่างรวดเร็วและทำซ้ำได้ที่มีความสำคัญทางชีววิทยา กระบวนการนี้เกิดขึ้นหลังชีวสังเคราะห์โปรตีน ในการถอดรหัส ยีนหรือส่วนของดีเอ็นเอที่เข้ารหัสโปรตีนจะแปลงเป็นเอ็มอาร์เอ็นเอ[1] ซึ่งต่อมาเอ็มอาร์เอ็นเอจะถูกแปลรหัสโดยใช้สายนิวคลีโอไทด์ที่ไรโบโซมเพื่อกำหนดสายกรดอะมิโน จากนั้นไรโบโซมจะเร่งปฏิกิริยาในการสร้างพันธะเพปไทด์ระหว่างหมู่อะมิโนจนได้สายพอลิเพปไทด์[2] หมู่อะมิโนแต่ละหมู่ในสายพอลิเพปไทด์จะจับกันเป็นโครงสร้างที่กำหนดตามลำดับกรดอะมิโนและโครงสร้างปฐมภูมิ (หลักของแอนฟินเซน)[3] โดยมีโปรตีนที่เรียกว่าแชเพอโรนช่วยในการม้วนพับและทำให้คงตัว[4] โปรตีนที่ม้วนพับแล้วจะเรียกว่าสภาพดั้งเดิม (native state)
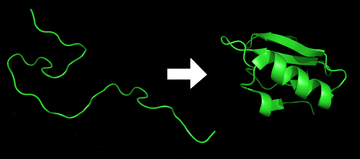
โครงสร้างสามมิติที่ถูกต้องมีความสำคัญยิ่งต่อการทำงานของโปรตีน อย่างไรก็ตามบางส่วนของโปรตีนจะยังคงสภาพไม่ม้วนพับ[5] การม้วนพับโปรตีนเกี่ยวข้องกับการจับกันของกรดอะมิโนอย่างสุ่ม[6] และเชื่อว่าพลวัตโปรตีนมีผลต่อการเปลี่ยนแปลงของโครงสร้าง[7] การม้วนพับที่ล้มเหลวก่อให้เกิดโปรตีนที่ไม่ทำงาน และบางกรณีเหนี่ยวนำให้เกิดความผิดปกติ โรคและการเสื่อมของระบบประสาทหลายชนิดเชื่อว่าเป็นผลมาจากการสะสมของเส้นใยแอมีลอยด์ที่เกิดจากโปรตีนที่ม้วนพับผิดปกติ[8] ภูมิแพ้หลายชนิดมีสาเหตุจากโปรตีนบางชนิดที่ม้วนพับไม่ถูกต้อง ทำให้ระบบภูมิคุ้มกันไม่สามารถผลิตสารภูมิต้านทาน ซึ่งเป็นโปรตีนที่ใช้ตรวจจับและทำลายสิ่งแปลกปลอมในร่างกาย[9]
การเสียสภาพธรรมชาติ (denaturation) เป็นกระบวนการที่ทำให้โปรตีนสูญเสียโครงสร้างจตุรภูมิ โครงสร้างตติยภูมิ และโครงสร้างทุติยภูมิในสภาพดั้งเดิม กลายเป็นโครงสร้างปฐมภูมิที่เป็นสายยาว การเสียสภาพธรรมชาติเกิดจากโปรตีนทำปฏิกิริยากับกรด–เบสแก่ เกลืออนินทรีย์เข้มข้น ตัวทำละลายอินทรีย์ การแผ่รังสี และความร้อน[10] หากโปรตีนเสียสภาพธรรมชาติในเซลล์สิ่งมีชีวิตจะส่งผลต่อการทำงานของเซลล์และอาจนำไปสู่การตายของเซลล์[11]
ระยะเวลาในกระบวนการม้วนพับแตกต่างไปตามชนิดโปรตีน เมื่อศึกษาภายนอก (in vitro) การม้วนพับอาจใช้เวลานานหลายนาทีหรือหลายชั่วโมงเนื่องจากต้องผ่านกระบวนการเปลี่ยนไอโซเมอร์ของโพรลีนและขั้นตอนอื่น ๆ ก่อนจะเสร็จสมบูรณ์[12] แต่ในทางตรงกันข้าม โดเมนโปรตีนขนาดเล็กมากที่ประกอบด้วยกรดอะมิโนร้อยหมู่สามารถม้วนพับได้ภายในขั้นตอนเดียว[13] โดยหน่วยเวลามาตรฐานในการม้วนพับอยู่ที่หลักมิลลิวินาที และเคยมีการพบโปรตีนที่เสร็จสิ้นการม้วนพับภายในเวลาไม่กี่ไมโครวินาที[14]
ทั้งนี้ การทำนายโครงสร้างโปรตีนที่ม้วนพับอย่างถูกต้องเป็นเป้าหมายหลักของสาขาวิชาชีววิทยาเชิงคำนวณมาตั้งแต่ปลายคริสต์ทศวรรษที่ 1960
อ้างอิง
แก้- ↑ "Transcription - Genetics". Britannica. สืบค้นเมื่อ December 3, 2020.
- ↑ "Translation - Genetics". Britannica. สืบค้นเมื่อ December 3, 2020.
- ↑ Anfinsen CB (July 1972). "The formation and stabilization of protein structure". The Biochemical Journal. 128 (4): 737–49. doi:10.1042/bj1280737. PMC 1173893. PMID 4565129.
- ↑ Saibil, Helen (October 2013). "Chaperone machines for protein folding, unfolding and disaggregation". Nature Reviews Molecular Cell Biology. 14 (10): 630–642. doi:10.1038/nrm3658. สืบค้นเมื่อ December 3, 2020.
- ↑ Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert (2002). "3. Protein Structure and Function". Biochemistry. San Francisco: W. H. Freeman. ISBN 978-0-7167-4684-3.
- ↑ Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walters, Peter (2002). "The Shape and Structure of Proteins". Molecular Biology of the Cell; Fourth Edition. New York and London: Garland Science. ISBN 978-0-8153-3218-3.
- ↑ Zhao, Qinyi (2013). "Nature of Protein Dynamics and Thermodynamics" (PDF). Reviews in Theoretical Science. 1: 1–19. สืบค้นเมื่อ December 3, 2020.
- ↑ Selkoe DJ (December 2003). "Folding proteins in fatal ways". Nature. 426 (6968): 900–4. Bibcode:2003Natur.426..900S. doi:10.1038/nature02264. PMID 14685251. S2CID 6451881.
- ↑ Alberts, Bruce; Bray, Dennis; Hopkin, Karen; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2010). "Protein Structure and Function". Essential cell biology (Third ed.). New York, NY: Garland Science. pp. 120–70. ISBN 978-0-8153-4454-4.
- ↑ Mosby's Medical Dictionary (8th ed.). Elsevier. 2009. สืบค้นเมื่อ 1 October 2013.
- ↑ Samson, Andre L.; Ho, Bosco; Au, Amanda E.; Schoenwaelder, Simone M.; Smyth, Mark J.; Bottomley, Stephen P.; Kleifeld, Oded; Medcalf, Robert L. (2016-11-01). "Physicochemical properties that control protein aggregation also determine whether a protein is retained or released from necrotic cells". Open Biology. 6 (11): 160098. doi:10.1098/rsob.160098. ISSN 2046-2441. PMC 5133435. PMID 27810968.
- ↑ Kim PS, Baldwin RL (1990). "Intermediates in the folding reactions of small proteins". Annual Review of Biochemistry. 59: 631–60. doi:10.1146/annurev.bi.59.070190.003215. PMID 2197986.
- ↑ Jackson SE (1998). "How do small single-domain proteins fold?". Folding & Design. 3 (4): R81-91. doi:10.1016/S1359-0278(98)00033-9. PMID 9710577.
- ↑ Kubelka J, Hofrichter J, Eaton WA (February 2004). "The protein folding 'speed limit'". Current Opinion in Structural Biology. 14 (1): 76–88. doi:10.1016/j.sbi.2004.01.013. PMID 15102453.
แหล่งข้อมูลอื่น
แก้- วิกิมีเดียคอมมอนส์มีสื่อเกี่ยวกับ การม้วนพับโปรตีน
- "Protein Folding and Processing". National Center for Biotechnology Information, U.S. National Library of Medicine.