ไนตรัสออกไซด์
ลิงก์ข้ามภาษาในบทความนี้ มีไว้ให้ผู้อ่านและผู้ร่วมแก้ไขบทความศึกษาเพิ่มเติมโดยสะดวก เนื่องจากวิกิพีเดียภาษาไทยยังไม่มีบทความดังกล่าว กระนั้น ควรรีบสร้างเป็นบทความโดยเร็วที่สุด |
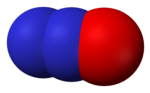
ไนตรัสออกไซด์ หรือ แก๊สหัวเราะ (อังกฤษ: Nitrous oxide หรือ laughing gas) คือสารประกอบทางเคมีที่มีสูตรทางเคมีว่า N2O ที่อุณหภูมิห้อง ไนตรัสออกไซด์จะไม่มีสี และเป็นแก๊สไม่ติดไฟ ไนตรัสออกไซด์มีกลิ่นหอมและมีรสหวานเล็กน้อย[4] มีการนำไนตรัสออกไซด์ไปใช้ในการผ่าตัดและทางทันตกรรมเพื่อให้เกิดอาการชาและเพื่อการระงับความปวด โดยทั่วไปรู้จักกันในชื่อ “แก๊สหัวเราะ” เนื่องจากเมื่อสูดดมแล้วจะให้ความรู้สึกเคลิ้มสุขหรือครึ้มใจ เป็นคุณสมบัติที่ทำให้มีการใช้ในเชิงนันทนาการโดยการใช้เป็นยาดม และยังมีการนำไปใช้ในการแข่งรถยนต์โดยให้เป็นตัวเติมออกซิเจนเพื่อเพิ่มกำลังให้เครื่องยนต์อีกด้วย

| |
| |
| ชื่อ | |
|---|---|
| IUPAC names | |
| Systematic IUPAC name
Oxodiazen-2-ium-1-ide | |
| ชื่ออื่น
Laughing gas, sweet air, nitrous, nos, protoxide of nitrogen, hyponitrous oxide, dinitrogen oxide, dinitrogen monoxide
| |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| 8137358 | |
| ChEBI | |
| ChEMBL | |
| เคมสไปเดอร์ | |
| ดรักแบงก์ | |
| ECHA InfoCard | 100.030.017 |
| เลขอี | E942 (glazing agents, ...) |
| 2153410 | |
| KEGG | |
ผับเคม CID
|
|
| RTECS number |
|
| UNII | |
| UN number | 1070 (compressed) 2201 (liquid) |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| N 2O | |
| มวลโมเลกุล | 44.013 g/mol |
| ลักษณะทางกายภาพ | colourless gas |
| ความหนาแน่น | 1.977 g/L (gas) |
| จุดหลอมเหลว | −90.86 องศาเซลเซียส (−131.55 องศาฟาเรนไฮต์; 182.29 เคลวิน) |
| จุดเดือด | −88.48 องศาเซลเซียส (−127.26 องศาฟาเรนไฮต์; 184.67 เคลวิน) |
| 1.5 g/L (15 °C) | |
| ความสามารถละลายได้ | soluble in alcohol, ether, sulfuric acid |
| log P | 0.35 |
| ความดันไอ | 5150 kPa (20 °C) |
| −18.9·10−6 cm3/mol | |
ดัชนีหักเหแสง (nD)
|
1.000516 (0 °C, 101.325 kPa) |
| ความหนืด | 14.90 μPa·s[3] |
| โครงสร้าง | |
| linear, C∞v | |
| 0.166 D | |
| อุณหเคมี | |
Std molar
entropy (S⦵298) |
219.96 J/(K·mol) |
Std enthalpy of
formation (ΔfH⦵298) |
+82.05 kJ/mol |
| เภสัชวิทยา | |
| N01AX13 (WHO) | |
| Inhalation | |
| เภสัชจลนศาสตร์: | |
| 0.004% | |
| 5 นาที | |
| ระบบทางเดินหายใจ | |
| ความอันตราย | |
| GHS labelling: | |
 
| |
| อันตราย | |
| H270, H280, H281 | |
| P220, P244, P282, P317, P336, P370+P376, P403, P410+P403 | |
| NFPA 704 (fire diamond) | |
| จุดวาบไฟ | ไม่ติดไฟ |
| เอกสารข้อมูลความปลอดภัย (SDS) | Ilo.org, ICSC 0067 |
| สารประกอบอื่นที่เกี่ยวข้องกัน | |
| ไนตริกออกไซด์ ไดไนโตรเจนไตรออกไซด์ ไนโตรเจนไดออกไซด์ ไดไนโตรเจน เทโตรไซด์ ไดไนโตรเจนเพนทอกไซด์ | |
สารประกอบที่เกี่ยวข้อง
|
Ammonium nitrate Azide |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |


การเกิด แก้
ไนตรัสออกไซด์ต่างกับไนโตรเจนออกไซด์ตรงที่มันเป็นแก๊สเรือนกระจกที่สำคัญ ถึงแม้มันจะมีการแผ่รังสีความร้อนน้อยกว่า CO2 ก็ตาม แต่ แก๊ส ไนตรัสออกไซด์ปริมาณ 1 หน่วยน้ำหนักกลับ มีผลกระทบต่อภาวะโลกร้อน มากกว่าแก๊สคาร์บอนไดออกไซด์ (CO2) ปริมาณเท่ากันถึง 298 เท่า ในระยะเวลา 100 ปี[5] แต่เนื่องจากในชั้นบรรยากาศมีปริมาณแก๊สในตรัสออกไซด์สะสมอยู่ไม่มาก มันจึงเป็นแก๊สเรือนกระจกที่มีส่วนในการก่อให้เกิดภาวะโลกร้อนน้อยกว่าคาร์บอนไดออกไซด์ที่สะสมในชั้นบรรยากาศเป็นปริมาณมากกว่า โดยไนตรัสออกไซด์เป็นแก๊สเรือนกระจกที่ก่อให้เกิดภาวะ โลกร้อนมากเป็นอันดับที่ 4 ต่อจากคาร์บอนไดออกไซด์ มีเทนและไอน้ำ (ไนโตรเจนออกไซด์ชนิดอื่นก่อภาวะโลกร้อนโดยตรง โดยเป็นตัวสร้างโอโซนในบรรยากาศชั้นโทรโปสเฟียร์ในช่วงที่เกิดหมอกปนควัน (smog) ) การควบคุมไนตรัสออกไซด์จึงนับเป็นมาตรการหนึ่งเพื่อลดการปล่อยแก๊สเรือนกระจก เช่นในพิธีสารเกียวโต
ไนตรัสออกไซด์เกิดจากแบคทีเรียในดินและมหาสมุทร มันจึงเป็นส่วนของบรรยากาศของโลกมานับหลายบรมยุค (eon) มาแล้ว เกษตรกรรมเป็นแหล่งเกิดไนตรัสออกไซด์โดยฝีมือมนุษย์โดยการพรวนดินและการใช้ปุ๋ยไนโตรเจน ของเสียจากสัตว์ก็มีส่วนช่วยเพิ่มแบคทีเรียที่ให้เกิดไนตรัสออกไซด์เพิ่มขึ้นอีกด้วย ภาคปศุสัตว์ (ส่วนใหญ่คือโคกระบือ ไก่และสุกร) ปล่อยไนตรัสออกไซด์ที่ถือเป็นกิจกรรมมนุษย์มากถึงร้อยละ 65[6] แหล่งที่มาจากอุตสาหกรรมมีเพียงประมาณร้อยละ 20 และรวมถึงการผลิตไนลอนและกรดไนตริกและการเผาผลาญเชื้อเพลิงซากดึกดำบรรพ์ในเครื่องยนตร์สันดาปภายใน
คาดกันว่ากิจกรรมมนุษย์ปล่อยไนโตรเจนออกไซด์ออกมาน้อยกว่า 2 เทระกรัม (teragram หรือ 1012 กรัม) ต่อปี ธรรมชาติปล่อยมากกว่า 15 เทระกรัม.[7] ฟลักซ์ (flux) ของไนตรัสออกไซด์ที่เกิดโดยกิจกรรมมนุษย์มีประมาณ 1 เพตะกรัม (1015 กรัม) ของคาร์บอนไดออกไซด์เทียบเท่าคาร์บอนสมมูล (carbon dioxide carbon-equivalents) ต่อปี หรือเท่ากับ 2 เพตะกรัมของมีเทนเทียบเท่าคาร์บอนสมมูลต่อปี และมีการปล่อยสู่บรรยากาศ (atmospheric loading) ในอัตราเท่ากับ 3.3 เพตะกรัมของคาร์บอนไดออกไซด์เทียบเท่าคาร์บอนสมมูลต่อปี
ไนตรัสออกไซด์ทำปฏิกิริยากับโอโซนในบรรยากาศชั้นสตราโตสเฟียร์ ส่วนไนโตรเจนออกไซด์เป็นตัวควบคุมตามธรรมชาติของโอโซนในบรรยากาศ
งานวิจัยของ พอล ครัทเซน (Paul Crutzen) ซึ่งเป็นนักวิทยาศาสตร์รางวัลโนเบลเสนอว่า การปล่อยไนตรัสออกไซด์ในการผลิตเชื้อเพลิงชีวภาพ (biofuel) มีปริมาณมากพอที่จะหักล้างข้อได้เปรียบของไบโอดีเซลที่หวังกันว่าจะช่วยลดการปล่อยคาร์บอนไดออกไซด์ได้[8]
การผลิต แก้
การเตรียมไนตรัสออกไซด์โดยทั่วไปทำโดยการให้ความร้อนแอมโมเนียมไนเตรทอย่างระมัดระวัง ซึ่งจะสลายตัวเป็นไนตรัสออกไซด์และไอน้ำ[9]
- NH4NO3 (s) → 2 H2O (g) + N2O (g)
ความปลอดภัย แก้
ความเสี่ยงหลักในด้านความปลอดภัยของไนตรัสออกไซด์มาจากความจริงที่ว่ามันถูกอัดด้วยความดันอยู่ในรูปก๊าซเหลว ความเสี่ยงจากการขาดอากาศหายใจ และทำให้หมดสติ การได้รับสัมผัสก๊าซไนตรัสออกไซด์จะทำให้สติสัมปชัญญะ ความสามารถในการรับรู้รับฟัง และความคล่องแคล่วของร่างกายลดลงชั่วขณะ จากการศึกษาโดยการใช้สัตว์ทดลองหลายครั้งและจากผู้ปฏิบัติงานหลายคน ชี้ให้เห็นว่าการได้รับสัมผัสก๊าซไนตรัสออกไซด์ติดต่อกันเป็นประจำอาจส่งผลร้ายต่อระบบสืบพันธุ์ของหญิงตั้งครรภ์ได้ สถาบันอาชีวอนามัยและความปลอดภัยแห่งชาติให้คำแนะนำว่าการได้รับสัมผัสก๊าซไนตรัสออกไซด์ของผู้ปฏิบัติงานควรได้รับการควบคุมการจัดการในระหว่างการใช้ก๊าซเพื่อทำให้หมดสติโดยผู้ปฏิบัติงานทางการแพทย์ ทันตกรรม และสัตวแพทย์
อ้างอิง แก้
- ↑ "[Nitrous oxide]". Degruyter.com. สืบค้นเมื่อ 24 July 2022.
- ↑ IUPAC nomenclature of inorganic chemistry 2005. PDF, p. 317.
- ↑ Takahashi, Mitsuo; Shibasaki-Kitakawa, Naomi; Yokoyama, Chiaki; Takahashi, Shinji (1996). "Viscosity of Gaseous Nitrous Oxide from 298.15 K to 398.15 K at Pressures up to 25 MPa". Journal of Chemical & Engineering Data. 41 (6): 1495–1498. doi:10.1021/je960060d. ISSN 0021-9568.
- ↑ สต๊อคเลย์, คอริน; ออกเลด, คริส; เวิร์ธเฮม, เจน (2003). โรเจอร์, เคิรสทีน (บ.ก.). พจนานุกรมวิทยาศาสตร์ ฉบับภาพประกอบ. พูนเพิ่มผลิตผล. p. 181. ISBN 974-90062-1-6.
- ↑ "Climate Change 2001: Working Group I: The Scientific Basis :". Intergovernmental Panel on Climate Change. สืบค้นเมื่อ 2008-02-02.
- ↑ H. Steinfeld, P. Gerber, T. Wassenaar, V. Castel, M. Rosales, C. de Haan (2006). "Livestock's long shadow -- Environmental issues and options". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2014-08-06. สืบค้นเมื่อ 2008-02-02.
{{cite web}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Sources and Emissions -- Where Does Nitrous Oxide Come From?". U. S. Environmental Protection Agency. 2006. สืบค้นเมื่อ 2008-02-02.
- ↑ P. J. Crutzen, A. R. Mosier, K. A. Smith, and W. Winiwarter (2007). "N2O release from agro-biofuel production negates global warming reduction by replacing fossil fuels" (PDF). Atmos. Chem. Phys. Discuss.,. 7: 11191–11205. สืบค้นเมื่อ 2008-02-02.
{{cite journal}}: CS1 maint: extra punctuation (ลิงก์) CS1 maint: multiple names: authors list (ลิงก์) - ↑ Holleman, A. F.; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 978-0-12-352651-9.
แหล่งข้อมูลอื่น แก้
- Occupational Safety and Health Guideline for Nitrous Oxide
- Paul Crutzen Interview Freeview video of Paul Crutzen Nobel Laureate for his work on decomposition of ozone talking to Harry Kroto Nobel Laureate by the Vega Science Trust.
- National Pollutant Inventory – Oxide of nitrogen fact sheet
- National Institute for Occupational Safety and Health – Nitrous Oxide
- CDC – NIOSH Pocket Guide to Chemical Hazards – Nitrous Oxide
- Nitrous Oxide FAQ
- Erowid article on Nitrous Oxide
- Nitrous oxide fingered as monster ozone slayer เก็บถาวร 29 กันยายน 2012 ที่ เวย์แบ็กแมชชีน, Science News
- Dental Fear Central article on the use of nitrous oxide in dentistry
- Altered States Database
